Гидролиз
По катиону, по аниону или нет гидролиза?
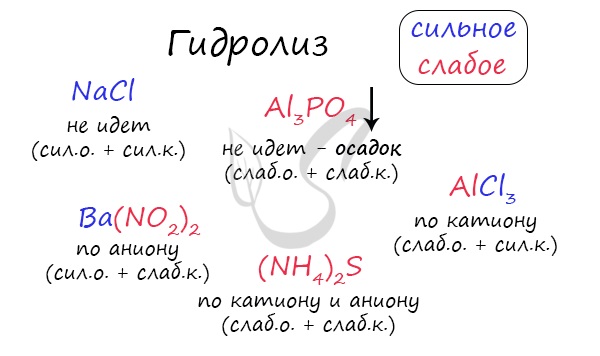
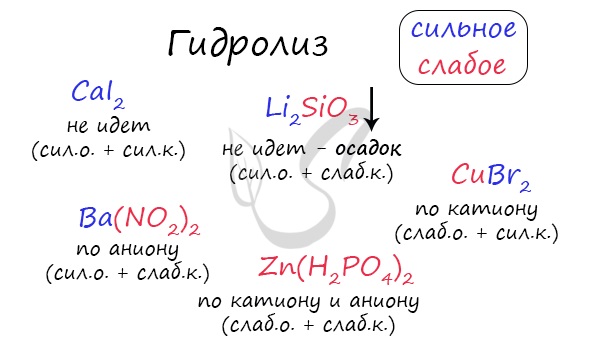
Если в состав соли входит остаток сильного основания и остаток слабой кислоты, то гидролиз идет по аниону. Примеры: K3PO4, NaNO2, Ca(OCl)2, Ba(CH3COO)2, Li2SiO3.
Если соль образована остатком слабого основания и слабой кислоты, то гидролиз идет и по катиону, и по аниону. Примеры: Mg(NO2)2, Al2S3, Cr2(SO3)3, CH3COONH4.
Среда раствора
Среда раствора может быть нейтральной, кислой или щелочной. Определяется типом гидролиза. Некоторые задания могут быть построены так, что, увидев соль, вы должны будете определить ее тип раствора.
Однако замечу, что в дигидрофосфатах, гидросульфитах и гидросульфатах среда всегда кислая из-за особенностей диссоциации. Примеры: NH4H2PO4, LiHSO4. В гидрофосфатах среда щелочная из-за того, что константа диссоциации по третьей ступени меньше, чем константа гидролиза. Примеры: K2HPO4, Na2HPO4.
Попробуйте определить среду раствора для соединений из самостоятельного задания, которое вы только что решили. Ниже будет располагаться решение.
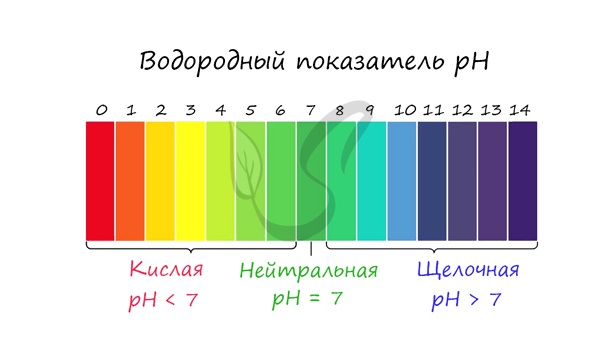
С целью запутать в заданиях часто бывают даны синонимы. Так «среду раствора» могут заменить водородным показателем pH.
Запомните, что кислая среда характеризуется pH 7.
Фосфат аммония гидролиз по чему
Установите соответствие между названием соли и отношением ее к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Соль, образованная слабым основанием и слабой кислотой подвергается полному гидролизу, гидролизуется по катиону и аниону — фосфат аммония.
Соль,образованная слабым основанием и сильной кислотой гидролизуется по катиону, среда раствора кислая — нитрат цинка.
Соль, образованная сильным основанием и слабой кислотой гидролизуется по аниону, среда раствора щелочная — карбонат калия.
Соль, образованная сильным основанием и сильной кислотой не подвергается гидролизу — сульфат натрия.
Фосфорная кислота относится к слабым кислотам, (тем более по третьей ступени диссоциации)
Установите соответствие между названием соли и типом гидролиза водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ | ||||||||||||||
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
A) стеарат натрия — соль сильного основания и слабой кислоты, гидролиз по аниону (2).
Б) фосфат аммония — соль слабого основания и слабой кислоты, гидролиз по катиону и аниону (3).
B) сульфид натрия — соль сильного основания и слабой кислоты, гидролиз по аниону (2).
Г) сульфат бериллия — соль слабого основания и сильной кислоты, гидролиз по катиону (1).
H3PO4 кислота средней силы. Гидролиз и по катион и по аниону.
Это слабая кислота.
Его гидроксид нерастворим.
сульфат бериллия нерастворимая соль
Он растворим в воде.
Установите соответствие между названием соли и её отношением к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
А) фосфат аммония — соль слабого основания и слабой кислоты, гидролиз по катиону и аниону.
Б) ацетат калия — соль слабой кислоты, гидролиз по аниону.
В) ортофосфат натрия — соль слабой кислоты, гидролиз по аниону.
Г) нитрат железа (III) — соль слабого основания, гидролиз по катиону.
По идее, фосфат аммония в водной среде разлагается или не существует, тогда гидролиза быть не должно.
В данном случае фраза «в водной среде разлагается» и означает, что идет полный гидролиз.
Установите соответствие между названием соли и отношением этой соли к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
А) стеарат натрия — соль сильного основания и слабой кислоты — 2) гидролиз по аниону.
Б) фосфат аммония — соль слабого основания и слабой кислоты — 3) гидролиз по катиону и аниону.
В) сульфид натрия — соль сильного основания и слабой кислоты — 2) гидролиз по аниону.
Г) сульфат бериллия — соль слабого основания и сильной кислоты — 1) гидролиз по катиону.
Установите соответствие между названием соли и отношением этой соли к гидролизу.
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
Запишите в таблицу выбранные цифры под соответствующими буквами.
А) карбонат кальция — нерастворимая соль, не гидролизуется вариант ответа № 3;
Б) фосфат аммония — соль слабого основания и слабой кислоты, гидролиз по катиону и по аниону, вариант ответа № 4;
В) нитрат магния — соль слабого основания и сильной кислоты, гидролиз по катиону, вариант ответа № 1;
Г) сульфид калия — соль сильного основания и слабой кислоты, гидролиз по аниону, вариант ответа № 2.
Нерастворимое соединение образуется в результате взаимодействия
1) хлорида калия и гидроксида бария
2) хлорида цинка и гидроксида натрия
3) фосфата аммония и гидроксида калия
4) сульфида калия и гидроксида кальция
Нерастворимое соединение образуется в результате взаимодействия хлорида цинка и гидроксида натрия:
Нерастворимое основание образуется в результате взаимодействия
1) сульфата натрия и гидроксида бария
2) хлорида железа (II) и гидроксида натрия
3) фосфата аммония и гидроксида калия
4) сульфида калия и гидроксида кальция
По таблице растворимости определяем что в данном случае происходит реакция:
сульфата натрия и гидроксида бария
с каких пор сульфат бария не выпадает в осадок?
А с каких пор сульфат бария стал основанием?
Читайте вопрос внимательно.
3) нитрат железа(III)
4) сульфат алюминия
В зависимости от стехиометрического соотношения анионов и катионов при диссоциации солей будет образовываться разное их количество. Например, при диссоциации соли XY соотношение катионов и анионов 1:1, соли XY2 1:2, соли X2Y3 1:1,5, XY3 1:3 и так далее. Видно что при диссоциации нитрата железа(III) образуется в 3 раза больше отрицательных ионов, чем положительных.
Разве фосфат аммония не диссоциирует в отношении 1:3?
Фосфат аммония диссоциирует в отношении 1:3, но только в нем положительных ионов в три раза больше, а не отрицательных (как указано в условии)
Фосфат аммония реагирует в водном растворе с:
1)
2)
3)
4)
5)
Запишите номера выбранных ответов.
Установите соответствие между названием соли и способностью ее к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | СПОСОБНОСТЬ К ГИДРОЛИЗУ |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Соль сильного основания и сильной кислоты гидролизу не подвергается; соль слабого основания и сильной кислоты — гидролиз по катиону; соль сильного основания и слабой кислоты — гидролиз по аниону; соль слабого основания и слабой кислоты — гидролиз по катиону и аниону.
A) карбонат калия — соль сильного основания и слабой кислоты — гидролиз по аниону (3).
Б) иодид кальция — соль сильного основания и сильной кислоты гидролизу не подвергается (1).
B) сульфид аммония — соль слабого основания и слабой кислоты — гидролиз по катиону и аниону (4).
Г) фосфат натрия — соль сильного основания и слабой кислоты — гидролиз по аниону (3).
Или как нужно рассуждать.?
Карбонат кальция гидролизу не подвергается.
А в ответе указано, что гидролиз идёт по аниону, потому, что в условии дан карбонат калия
Установите соответствие между соли и способностью ее к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | СПОСОБНОСТЬ К ГИДРОЛИЗУ | ||
| НАЗВАНИЕ СОЛИ | ХАРАКТЕР СРЕДЫ |
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
А. Фосфат натрия — соль сильного основания и слабой кислоты, гидролиз по аниону, вариант ответа №2.
Б. Бромид алюминия — соль слабого основания и сильной кислоты, гидролиз по катиону, вариант ответа №1.
В. Бромат калия — соль сильного основания и сильной кислоты, не гидролизуется, вариант ответа №3.
Г. Ацетат аммония — соль слабого основания и слабой кислоты, гидролиз и по катиону, и по аниону, вариант ответа №4.
Для выполнения задания используйте следующий перечень веществ: фосфат кальция, сульфит натрия, соляная кислота, хлорид железа(III), гидрокарбонат натрия, сульфат аммония. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена, не приводящая к выделению газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Для выполнения задания используйте следующий перечень веществ: фосфат кальция, сульфит натрия, соляная кислота, хлорид железа(III), гидрокарбонат натрия, сульфат аммония. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна окислительно-восстановительная реакция, и запишите уравнение этой реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
Для начала запишем молекулярные формулы данных веществ:
1) Уравнение реакции:
2) Электронный баланс:
2 | →
1 | →
3) Железо в степени окисления +3 (или хлорид железа(III) за счёт железа в степени окисления +3) является окислителем. Сера в степени окисления +4 (или сульфит натрия за счёт серы в степени окисления +4) — восстановителем.
Фосфат аммония: состав, свойства, получение, применение
Содержание:
Именно это и происходит с NH4 + собственной структуры. Следовательно, фосфат аммония нестабилен, разлагается на NH.4ЧАС2PO4 и NH3. Поэтому эта соль источает сильный запах аммиака.
Другие соли фосфата аммония более стабильны и полезны. Например, они используются в сельском хозяйстве в качестве удобрений, а кристаллы некоторых из них даже имеют оптическое и физическое применение.
Это семейство солей простое, но разнообразное при изменении кислотности среды, в которой они находятся.
Состав
То же самое происходит частично и с другими солями этого фосфата: (NH4)2HPO4 и NH4ЧАС2PO4, в котором ПО4 3- выиграл один или два H + соответственно. В его кристаллах, в основном тетрагональных, электростатические взаимодействия слабее из-за меньшего ионного заряда.
Однако они более энергетически устойчивы, особенно NH4ЧАС2PO4, так как он имеет самую высокую температуру плавления.
С другой стороны, соли фосфата аммония также могут образовывать гидраты, включая молекулы воды в свои кристаллические структуры.
Свойства фосфата аммония
Имена
(NH4)3PO4
Эта формула, строго следуя неорганической номенклатуре, соответствует соли фосфата аммония. Другие допустимые имена:
-Тиблоосновный фосфат аммония
-Триаммоний или триаммоний фосфат
(NH4)2HPO4
У этой соли есть несколько наименований согласно номенклатуре предпочтений. Наиболее распространенными, помимо диаммонийфосфата, являются:
-Фосфат аммонийной кислоты
-Двухосновной фосфат аммония
В отличие от (NH4)3PO4, состоит из ионов NH4 + и HPO4 2- в соотношении 2: 1.
NH4ЧАС2PO4
-Одноосновной фосфат аммония (потому что в нем почти нет кислорода, способного принимать протоны)
-Диацид фосфат аммония
Некоторые из приведенных выше имен также можно изменить на:
Как видно, возможных названий много. Важно знать, как соотнести их непосредственно с формулами любой из трех солей, соответствующих семейству фосфатов аммония.
Молярные массы
Внешность
Соли фосфата аммония объединяет то, что все они белые. За исключением триаммонийного или трехосновного фосфата аммония, другие соли не выделяют запаха аммиака при нормальных условиях.
Точки плавления
(NH4)3PO4 он ломается, прежде чем сможет расплавиться. Между тем, (NH4)2HPO4 плавится при 155 ºC, а NH4ЧАС2PO4 при 190 ° С. Самая высокая температура плавления NH4ЧАС2PO4 указывает на большую стабильность и более прочную ионную связь.
Точки кипения
Безмерно, так как они разлагаются при плавлении.
Растворимость
Соли фосфата аммония хорошо растворимы в воде, так как (NH4)3PO4 гигроскопичное твердое вещество. Однако они нерастворимы в этаноле, ацетоне и жидком аммиаке.
Разложение
Все соли фосфата аммония могут выделять аммиак при разложении. Кроме того, в зависимости от интенсивности тепла они разлагаются на фосфорную кислоту, в конечном итоге выделяя вредные газы оксидов азота и фосфора.
Получение
Соли фосфата аммония получают в результате реакции нейтрализации между фосфорной кислотой и аммиаком:
Как можно видеть, если желательно получить «менее основные» фосфаты аммония, что означает то же самое, что и «более кислые», необходимо изменять пропорции реагентов, которые добавляют в реактор. Обычно оксид фосфора, P2ИЛИ5, как источник фосфора для соответствующей кислоты.
На самом деле они NH4ЧАС2PO4 (MAP, аббревиатура на английском языке: моноаммонийфосфат) и (NH4)2HPO4 (DAP) соли фосфата аммония, имеющие самую высокую коммерческую ценность. Между тем, (NH4)3PO4 он наименее коммерциализирован именно потому, что он наиболее нестабилен и, возможно, самый дорогой в приготовлении.
Приложения
Одним из непосредственных последствий предыдущего абзаца является то, что большинство случаев использования солей фосфата аммония связано с NH4ЧАС2PO4 и (NH4)2HPO4. (NH4)3PO4С другой стороны, от него почти нет никакой пользы, так как он быстро разлагается.
Удобрения
Антипирены
При разложении солей фосфата аммония выделяются различные газы, которые, хотя и вредны, вытесняют кислород из воздуха при полном пожаре. Именно поэтому их используют как антипирены. Таким образом, распространение пламени замедляется или замедляется.
Оптика и физика
NH4ЧАС2PO4 Он используется в оптических приложениях, потому что его кристаллы демонстрируют двойное лучепреломление, то есть имеют двойное лучепреломление. Они также обладают пьезоэлектрическими свойствами, поэтому используются в преобразователях.
Ссылки
Зурисадай: происхождение и значение
9 самых популярных типичных танцев и танцев Веракруса