Фенотип опухоли со стабильной системой репарации mss что это
Микросателлитная нестабильность характеризует генетическую изменчивость многих опухолей. Определение данного показателя используется в процессе диагностики рака толстого кишечника, а также для назначения химиотерапевтического лечения.
Исследования при колоректальном раке.
Microsatellite instability, MSI; high level microsatellite instability, MSI-H; replication error phenotype, RER+.
Какой биоматериал можно использовать для исследования?
Венозную кровь, образец ткани, образец ткани в парафиновом блоке.
Общая информация об исследовании
Гены, которые восстанавливают мутации в ДНК, известны как гены репарации ошибочно спаренных нуклеотидов (mismatch repair, MMR). Существует четыре различных гена репарации, которые отвечают за исправление мутаций в ДНК. Если один из этих четырех генов мутирован, небольшие ошибки в ДНК остаются неисправленными. Эти ошибки приводят к расширению или уменьшению повторяющихся последовательностей в ДНК, что и называется микросателлитной нестабильностью (MSI).
Если человек рождается с мутацией в одном из четырех генов репарации (то есть мутация присутствует во всех клетках его тела), это приводит к синдрому Линча. Синдром Линча является наиболее распространенной наследственной формой рака толстой кишки, на его долю приходится 3 % всех случаев рака толстой кишки.
Тем не менее только небольшая часть опухолей с положительным результатом MSI обусловлена синдромом Линча. Это означает, что большинство MSI-позитивных опухолей возникают спорадически и не обусловлены наследственной мутацией в гене репарации.
Для чего используется исследование?
Микросателлитная нестабильность чаще всего обнаруживается при раке толстого кишечника и является важным прогностическим показателем. Опухоли с высокой степенью MSI не склонны к метастазированию, и их прогноз благоприятный.
Определение MSI проводят при скрининге пациентов, у которых подозревают синдром Линча – наследственный колоректальный рак, который часто сочетается с другими онкозаболеваниями: раком желудка, мочевыводящих путей, яичника, кожи, поджелудочной железы, опухолей головного мозга.
Выявление MSI высокой степени становится показанием для назначения таргетной терапии, то есть влияющей на конкретную генетическую мишень, которая стала причиной онкопроцесса. Этими препаратами являются ингибиторы рецептора PD-1, пембролизумаб и ниволумаб.
Также исследование микросателлитной нестабильности играет роль в определении потенциальной чувствительности опухолей к препаратам из группы 5-фторурацила, простым алкилирующим агентам и производным платины.
Когда назначается исследование?
Что означают результаты?
В результате исследования отмечается выявление или невыявление микросателлитной нестабильности.
Микросателлитную нестабильность (MSI) обнаруживают примерно в 15 % от всех раков толстого кишечника. Причем частота выявления MSI при колоректальном раке зависит от стадии заболевания, составляя до 22 % при II стадии, до 12 % при III стадии и не более 3-4 % при IV стадии.
Если колоректальный рак или другие опухоли связаны с синдромом Линча, то в 90 % случаев будет обнаружена микросателлитная нестабильность.
Высокий уровень микросателлитной нестабильности MSI означает:
данная опухоль не склонна к образованию метастазов и пациентам со II стадией заболевания можно не проводить адъювантную химиотерапию;
у пациента высока вероятность наличия синдрома Линча;
пациенту показано назначение таргетной химиотерапии (ингибиторы рецептора PD-1, пембролизумаб и ниволумаб).
Фенотип опухоли со стабильной системой репарации mss что это
Рак толстой кишки (РТК) остается одним из самых частых злокачественных новообразований в структуре как мужской, так и женской онкологической заболеваемости. Снижения абсолютного числа вновь выявленных случаев РТК, отмеченного за последние годы, удалось достичь благодаря скрининговым программам, позволяющим своевременно диагностировать и успешно излечивать предопухолевую патологию толстой кишки, особенно в группе больных старше 50 лет [1, 2]. Отрицательная динамика заболеваемости РТК регистрируется среди пациентов средней возрастной группы, для которой нет регламентированных скрининговых программ [1]. По данным американского статистического центра эпидемиологии у 15% больных РТК заболевание диагностируется в возрасте до 50 лет со средним значением манифестации заболевания 45,2 года [1]. По предварительным расчетам, учитывая существующие тенденции, показатель заболеваемости раком ободочной и прямой кишки к 2030 году вырастет на 90% и 124,2% соответственно для возрастной группы 20–34 года и на 46% – для лиц 35–49 лет [1, 3].
РТК с ранним возрастом манифестации заболевания (здесь и далее – молодой РТК, МРТК, early onset colorectal cancer, EOCRC) представляет собой гетерогенную группу злокачественных опухолей толстой кишки у пациентов с манифестацией заболевания в возрасте до 50 лет [1, 2]. На сегодняшний день нет единого консенсусного мнения относительно точной возрастной отметки, позволяющей разделить больных РТК на «молодых» и пациентов старшей возрастной группы [3]. Большинство авторов считают пограничным значением 50-летие больных, что обусловлено общепопуляционными скрининговыми наблюдениями, однако данная цифра продолжает варьировать в различных исследованиях [3].
Лишь незначительная часть МРТК обусловлена наследственной синдромальной патологией и/или может быть отнесена к так называемой семейной форме РТК, подавляющее же большинство случаев МРТК характеризуются отличительной молекулярной природой и остаются на сегодня предметом возрастающего числа научно-клинических исследований.
Цель исследования: представить современное состояние проблемы изучения молекулярно-генетических особенностей колоректального рака у больных молодого возраста.
Факторы риска развития МРТК. Канцерогенез РТК является многофакторным и многоступенчатым процессом, на каждом этапе которого возможна реализация как экзо-, так и эндогенных рисков, ассоциированных с РТК, однако ни один из таких факторов не является избирательно специфичным только для МРТК [4]. Табакокурение и употребление алкоголя, питание с высоким содержанием красного мяса и полуфабрикатов, малоактивный образ жизни являются универсальными признанными факторами риска развития РТК. Сахарный диабет повышает вероятность опухолей ободочной кишки на 38%, при этом каждое 5-е значение увеличения индекса массы тела ассоциировано с 13–18%-ным повышением риска развития РТК [4]. Хроническое воспаление наряду с гастроинтестинальным дисбиозом также являются триггерами онкогенеза в толстокишечном эпителии.
Отягощенный семейный анамнез остается одной из строгих детерминант, определяющих риск развития РТК. Так, наличие родственника первой степени родства (ПСР) с РТК повышает риск развития злокачественных новообразований (ЗНО) толстой кишки в 2–3 раза, двух пораженных родственников второй степени родства (ВСР) или одного родственника ПСР с РТК в возрасте до 50 лет ассоциировано с трехкратным и более увеличением риска РТК [5]. Наличие родственников с аденоматозными полипами также повышает эмпирический риск РТК. Возраст манифестации ЗНО в семье является другим прогностическим показателем. Так, постановка диагноза на девятом десятилетии жизни определяет 1,5-кратное повышение риска РТК для родственника ПСР, на пятом – 4-кратное и более повышение вероятности ЗНО толстой кишки [5].
Большинство больных МРТК, однако, характеризуются отсутствием семейного накопления ЗНО как в первом, так и во втором поколениях [4], что в целом является отличительной чертой МРТК. При исключении наследственной принадлежности и отягощенного анамнеза по хроническим воспалительным заболеваниям толстой кишки подавляющее число пациентов с МРТК могли бы быть отнесены в когорту больных с общепопуляционным риском ЗНО толстой кишки [4].
Негативный семейный анамнез в свою очередь не исключает наличия синдромальной патологии у пациентов с МРТК [4]. Так, только менее половины больных синдромом Линча удовлетворяют критериям «Амстердам», патологический MSH6- и PMS2-генотип характеризуется неполной пенетрантностью, а синдром семейного аденоматозного полипоза (реже – синдром Линча) ассоциирован с носительством значимых патогенных герминальных мутаций de-novo примерно в 15% случаев. По данным секвенирования герминального генома с применением таргетных панелей частота патогенных мутаций среди больных МРТК составляет 15–20%. По данным Chang et al., около 22% случаев РТК, диагностированного у больных моложе 40 лет, может быть обусловлено наследственной онкологической патологией [6]. В проспективном исследовании Pearlman et al. 16% больных МРТК (72/450) явились носителями патогенных мутаций, при этом в 10% случаев герминальные мутации выявлены в генах с высокой пенетрантностью (генах системы репарации неспаренных оснований, APC, MUTYH, BRCA1/2, CDKN2A и др.) и у 6% пациентов – в генах с промежуточным риском развития заболевания (ATM, PALB, CHEK2 и др.) [7]. При этом значительная часть пациентов в таких исследованиях не соответствовали как клинически, так и анамнестически диагностированному синдрому.
Несмотря на успехи современной молекулярной диагностики, ДНК-тестирование остается неинформативным у большинства пациентов с РТК в молодом возрасте. Расширение диагностической панели, особенно за счет генов-кандидатов со средней пенетрантностью, вероятно, позволит расширить наше представление о молекулярной природе МРТК.
Молекулярный патогенез МРТК. В канцерогенезе РТК задействованы три ведущих генетических механизма: хромосомная нестабильность (chromosomal instability (CIN)), микросателлитная нестабильность (microsatellite instability (MSI)) и CIMP-фенотип (CpG-island methylator phenotype) [8]. Патогенез МРТК в составе синдромальной патологии (синдрома Линча, САП и др.) является хорошо изученной парадигмой, в то время как определение драйверных этапов спорадического МРТК остается предметом научного поиска. В целом для «молодого» ненаследственного РТК характерны стабильный MSI-фенотип (80%) [4], низкий уровень метилирования и/или отсутствие CIMP, а также эуплоидия опухолевых клеток.
MSI-High-МРТК. Высокий показатель микросателлитной нестабильности диагностируется в 21% случаев МРТК, при этом практически у всех больных в дальнейшем подтверждается синдром Линча. Метилирование промотерной области гена MLH1 c наличием или отсутствием BRAF-мутаций у молодых пациентов с MSI-High является крайне редким событием (p=0,006 [4]). В двух крупных исследованиях данное сочетание было выявлено лишь однажды, при этом в одной работе возраст пациента составил 49 лет [9, 10]. Примерно в 50% случаев MSI-High-ассоциированного МРТК выявляется та или иная степень хромосомной нестабильности, что демонстрирует молекулярную гетерогенность MSI-High-РТК [9].
Микросателлитно-стабильный (MSS)-РТК и хромосомно-нестабильный пути канцерогенеза. CIN является ведущим патогенетическим путем в канцерогенезе МРТК и выявляется в 50–80% случаев [11]. Данные опухоли характеризуются стабильной системой репарации неспаренных нуклеотидов, хромосомными мутациями, приводящими к изменению их числа, а также хромосомными реаранжировками, амплификацией или потерей экспрессии онкогенов / генов – супрессоров опухолевого роста. Чаще всего в патологический процесс вовлекаются WNT— и MAPK-сигнальные пути, гены TP53, DCC, SMAD2/4 и др. [12].
Хромосомный дисбаланс в опухолях РТК с поздним возрастом начала болезни чаще всего ассоциирован с потерями хромосомных локусов, включающих гены SMAD4, DCC и APC [Bardhan]. МРТК в свою очередь отличается амплификацией участков, содержащих гены BMPR1A и AMP, а также утратой локусов с генами TJP2 и кодирующими FOX-транскрипционные факторы [13].
Активирующие мутации в гене KRAS определяются в 35–40% случаев РТК и являются предикторами резистентности к анти-EGFR-таргетной терапии. Частота KRAS-патологического генотипа в группах «молодого» РТК и РТК, диагностированного после 50 лет, варьирует в различных исследованиях и зависит от выборки больных, локализации опухоли, стадии процесса [14, 15].
Соматическая мутация V600E в гене BRAF встречается в 4 раза чаще у больных с MSS-МРТК по сравнению с «поздним» MSS-РТК (12% vs 3%, p 17 мутаций/Mb) наблюдался чаще у пациентов с МРТК (9,7% vs 2,8%, p
Микросателлитная нестабильность: что в действительности определяет развитие опухоли?
Безусловно, молекулярно-биологический механизм формирования опухоли в теле человека еще не изучен во всех деталях. Однако современные данные позволяют с уверенностью утверждать: многие моменты онкогенеза помогает прояснить явление микросателлитной нестабильности. Данный материал о том, что представляет из себя этот процесс, и как он связан с развитием опухоли.
Микросателлиты — это короткие последовательности в структуре ДНК, состоящие из 2–9 пар нуклеотидов. Они располагаются в эухроматиновой части генома, чаще — в некодирующих, регуляторных его участках. На сегодняшний день изучение последовательностей микросателлитов имеет массу вариантов практического применения. Так, длину микросателлитных участков и количество повторов в их структуре изучают в контексте диагностики некоторых наследственных заболеваний. К ним относятся атаксия Фридриха, миотонические дистрофии и другие неврологические патологии. При помощи исследования микросателлитных последовательностей проводится генотипическое картирование, необходимое для расшифровки генома. Нашли применение микросателлиты и в диагностике наследственных опухолевых синдромов и спорадических случаев рака.
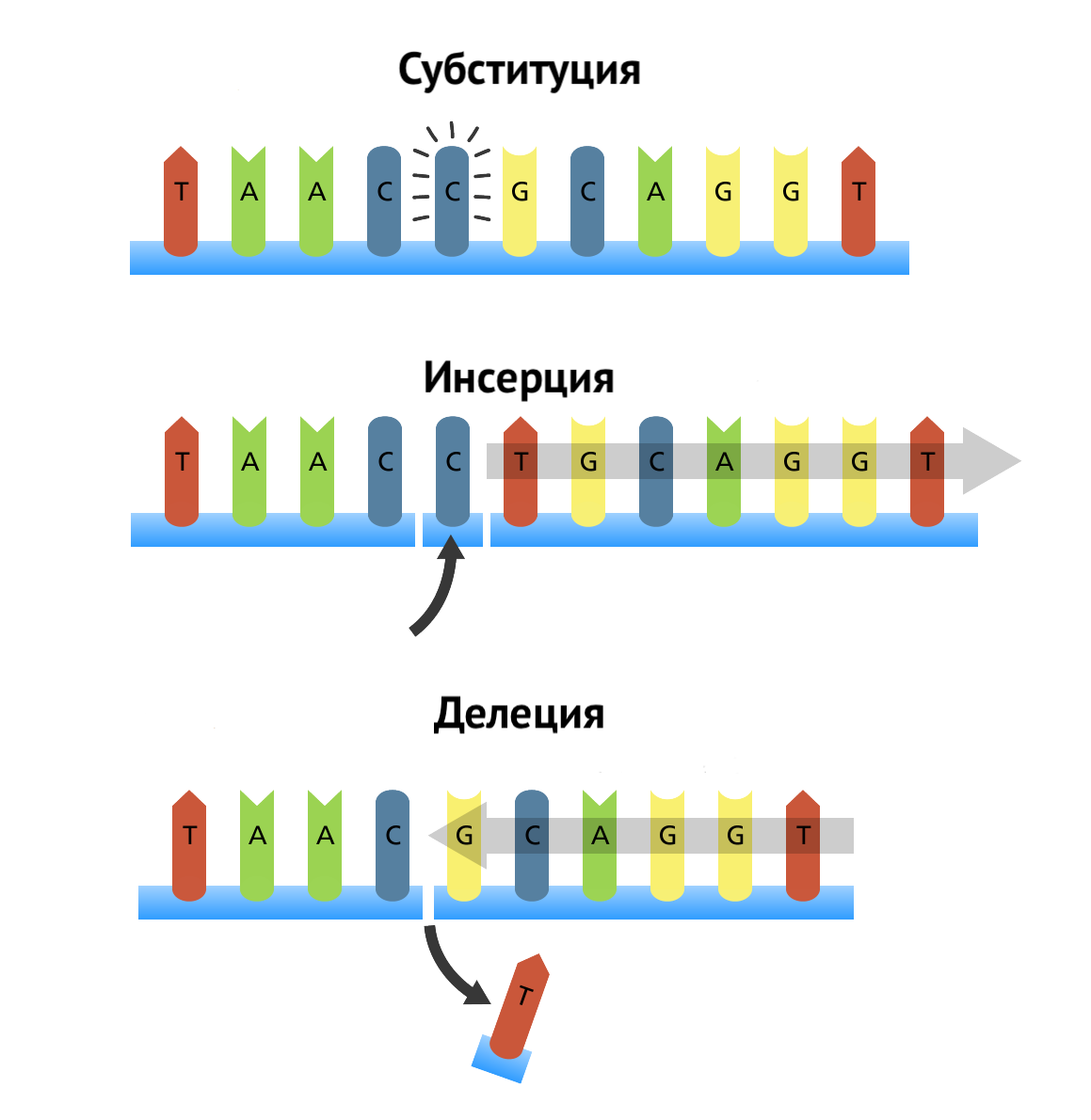
Понятие микросателлитной нестабильности отражает изменения в геноме, связанные со структурой микросателлитов. Выделяют несколько вариантов такой нестабильности. Например, вариант EMAST подразумевает повышение частоты альтерации микросателлитов, состоящих из повторов четырех нуклеотидов. В случае различных спорадических опухолей человека микросателлиты демонстрируют тенденцию к значительному увеличению их числа, более частому мутационному повреждению, возникновению делеций и инсерций (точечных мутаций, связанных с выпадением или вставкой нуклеотидов соответственно) [1]
Рисунок 1 | Основные виды точечных мутаций в геноме человека.
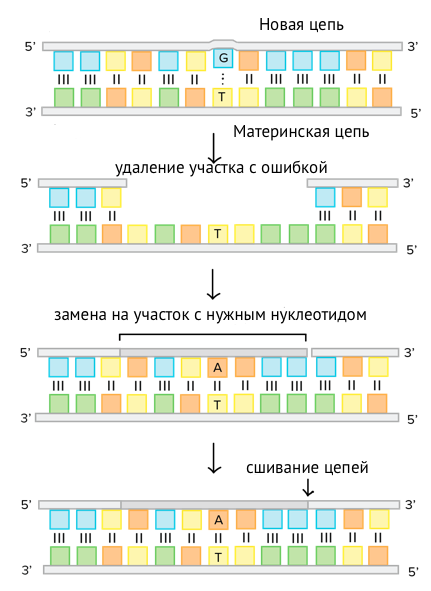
Наиболее тесным образом микросателлитная нестабильность связана с нарушениями в системе репарации ДНК, а именно — с вариантом mismatch-репарации. Этот процесс как вариант репарации неспаренных оснований в структуре ДНК способствует исправлению тысяч мутаций, возникающих в геноме каждого человека ежедневно. Систему mismatch-репарации составляют шесть генов, продукты которых ответственны за обнаружение неспаренных участков — пар нуклеотидов, созданных не по принципу комплементарности. После выявления таких участков продукты системы mismatch-репарации производят удаление определенного участка цепи, включающего неспаренные нуклеотиды, и замену вырезанных участков новыми в правильной последовательности.
Рисунок 2 | Упрощенный принцип работы системы mismatch-репарации.
Наследственные дефекты любого гена системы mismatch-репарации приводят к развитию наследственных опухолевых синдромов — например, синдрома Линча (о нем мы писали в этом материале). Приобретенные в течение жизни мутации в этих же генах могут приводить к формированию дефицита их продуктов. Дефицит компонентов системы mismatch-репарации условно ведет к сохранению множества неисправленных мутаций в генах соматических клеток (условно, поскольку помимо системы mismatch функционируют и другие репаративные системы). Однако уже доказанным является тот факт, что в конечном итоге наличие дефекта системы mismatch-репарации может приводить к формированию злокачественного новообразования, в основном колоректальной локализации [2].
Дефекты системы репарации ДНК отражаются в том числе и в увеличении числа микросателлитов генома — так формируется H-фенотип (high phenotype) микросателлитной нестабильности, обозначаемый как MSI-H. Данный фенотип является определенного рода маркером злокачественных новообразований, а именно — маркером наличия дефекта в системе репарации генома.
Интерес для современных ученых представляет и другой фенотип микросателлитной нестабильности, обозначаемый буквой L (low). Он отражает, напротив, снижение количества микросателлитных последовательностей в геноме, что встречается при наследственном неполипозном раке прямой кишки в ранних ее формах. Патогенез снижения уровня микросателлитов при наличии такой опухоли неясен, однако оно также может являться маркером, используемым при выявлении данного типа новообразований [3].
Классическим способом диагностики любой из форм микросателлитной нестабильности является полимеразная цепная реакция (ПЦР). Амплификация микросателлитных последовательностей позволяет установить их количество и структуру, и таким образом косвенно судить о дефиците компонентов системы репарации и отобразить фенотип нестабильности. Заключением такого анализа является либо выявление факта микросателлитной нестабильности с указанием фенотипического варианта, либо MSS — то есть стабильность микросателлитных участков генома.
Определенное значение имеет и выявление тканевого уровня самих белков-компонентов системы mismatch-репарации методом иммуногистохимии. В этом случае препараты исследуемой ткани обрабатываются специальными растворами, позволяющими по степени яркости окрашивания установить уровень того или иного белка и принцип его клеточного распределения. Метод иммуногистохимии позволяет точнее определить характер дефекта и используется, как правило, после проведения автоматизированного анализа методом ПЦР для определения наличия и характера микросателлитной нестабильности. Кроме того, перед проведением исследования необходимо удостовериться в наличии положительной корреляции между частотой возникновения дефицита системы mismatch-репарации и развитием исследуемой опухоли, так как в случае некоторых онкопатологий (например, при раке тела матки) ИГХ-исследование таких дефектов неэффективно [4].
Важно отметить, что исходя из определений разобранных терминов, этиология злокачественных новообразований действительно связана с мутациями, но чаще — не в самих соматических клетках, а в участках, кодирующих компоненты систем репарации. Именно нарушение репаративных процессов, отвечающих за сохранность структуры ДНК (в том числе в варианте mismatch-репарации), в конечном итоге приводит к формированию некоторых опухолей, а выявить эту закономерность позволяет такое исследование, как ПЦР для определения микросателлитной нестабильности генома.
Источники:
Микросателлитная нестабильность (MSI) – тест в израильской клинике за 1 день
В клинике Hadassah Moscow проводится быстрое молекулярно-генетическое тестирование микросателлитной стабильности опухоли (MSI) с возможным назначением иммунотерапии в тот же день у пациентов с метастазами вне зависимости от типа рака. Данное направление в онкологии является инновационным подходом персонализированной терапии.
Микросателлитная нестабильность — что это?
Опухолевые клетки активно делятся, что приводит к появлению нарушений в их геноме, в том числе появлению новых микросателлитных повторов. Если система репарации клетки не устраняет эти ошибки, такое состояние называется микросателлитной нестабильностью. Оценка микросателлитной нестабильности проводится с использованием теста полимеразной цепной реакции (ПЦР) или иммуногистохимического исследования.
Имеет ли оценка микросателлитной нестабильности клиническое значение?
В нескольких клинических исследованиях было показано, что у онкологических пациентов с микросателлитной нестабильностью такие иммунные препараты как пембролизумаб или ниволумаб продемонстрировали позитивные результаты. На этом основании регуляторные органы различных стран одобрили применение этих ингибиторов контрольных точек (пембролизумаб, ниволумаб) вне зависимости от типа опухоли у пациентов с микросателлитной нестабильностью. Кроме того, наличие или отсутствие этого маркера может иметь значение для назначения таргетной и адъювантной терапии, чему посвящены последние исследования.
Микросателлитная нестабильность не обнаружена — что это значит? Это означает, что опухоль стабильна (MSS) по нескольким мутациям, иммунотерапия может быть не показана. Однако, для определенной группы опухолей иммунотерапия назначается даже несмотря на результат MSS. Например, иммунотерапия используется у больных раком легкого с экспрессией другого маркера – PD-L1. То есть лечащий врач-онколог подходит к оценке всех молекулярно-генетических изменений комплексно и индивидуально.
Каким пациентам может быть рекомендована оценка микросателлитной нестабильности и назначение иммунных препаратов?
Пациенты, которые имеют любой метастатический рак и уже получили стандартное лечение, не оказавшееся эффективным, являются кандидатами для оценки микросателлитной нестабильности, и в положительном случае – кандидатами для назначения ингибиторов контрольных точек.
Большое значение имеет микросателлитная нестабильность при колоректальном раке. Для этой опухоли необходимо определять микросателлитную нестабильность до какого-либо лекарственного лечения.
Тимофеев Илья Валерьевич, директор Института онкологии Хадасса Москва, член Правления RUSSCO: «Тестирование микросателлитной нестабильности в клетках опухолей и доказанная эффективность терапии пембролизумабом привели к появлению нового направления в современной онкологии, так называемой tumor-agnostic therapy – терапии, не привязанной к виду рака, а назначаемой в случае выявления молекулярного маркера. Пациенты, уже исчерпавшие лечебные опции, стандартные для конкретного типа опухоли, получили еще одну надежду в виде иммунотерапии при позитивном статусе MSI».
Какие преимущества имеет определение микросателлитной нестабильности в клинике Хадасса Москва?
Благодаря современным последним технологиям, ПЦР нового поколения, в клинике Хадасса Москва (Hadassah Medical Moscow) весь процесс тестирования займёт 2,5 часа в отличие от 10-15 дней в других лабораториях, что существенно сокращает время до назначения лекарственной терапии. Для тестирования требуется опухолевый материал (парафиновый блок), содержащий всего 10% опухолевых клеток.
В случае получения позитивного результата, при наличии данных инструментальных исследований, ингибитор контрольных точек может быть назначен пациенту в тот же день.
Станкевич Любовь Ивановна, кандидат медицинских наук, руководитель лабораторной службы Хадасса Москва, вице-президент Российской Ассоциации медицинской лабораторной диагностики (РАМЛД): «Произошел сдвиг парадигмы от лечения типа онкологического заболевания к лечению конкретного пациента и конкретной опухоли. Чтобы предлагаемая программа тестирования микросателлитной нестабильности и индивидуального подбора терапии для онкологических пациентов стала возможной мы стерли границы между патоморфологическими исследованиями, генетическими, инструментальными и другими методами анализа и построили эффективное взаимодействие врачей-онкологов и специалистов лабораторной медицины в едином диагностическом пространстве»
Этапы программы
Сколько стоит тестирование?
Стоимость анализа составляет – 35 000 руб. (результат в течение 3 часов с момента получения материала) или 25 000 руб. (результат на следующий день с момента получения материала).
Микросателлитная нестабильность MSI
Микросателлитная нестабильность не обнаружена. Что это значит? Что такое MSI и MSS? Объясняет специалист
Что такое MSI и MSS?
Микросателлитная нестабильность чаще всего встречается при колоректальном раке, раке желудка и раке эндометрия, но может также обнаруживаться при многих других типах рака. Знание результата анализа на msi при онкологии поможет спланировать лучшее лечение.
Анализ на определение микросателлитной нестабильности MSI
Если у вас или вашего близкого человека диагностирован колоректальный рак, то важно знать опухолевый статус MSI-H. Чтобы его определить, необходимо направить опухолевый материал на молекулярно-генетическое исследование. Забор материала часто происходит во время операции по удалению опухоли, но это может быть сделано и с помощью биопсии. Результат вашего теста покажет статус MSI как MSI-H, или MSS (microsatellite stability, «микросателлитная нестабильность не обнаружена»).
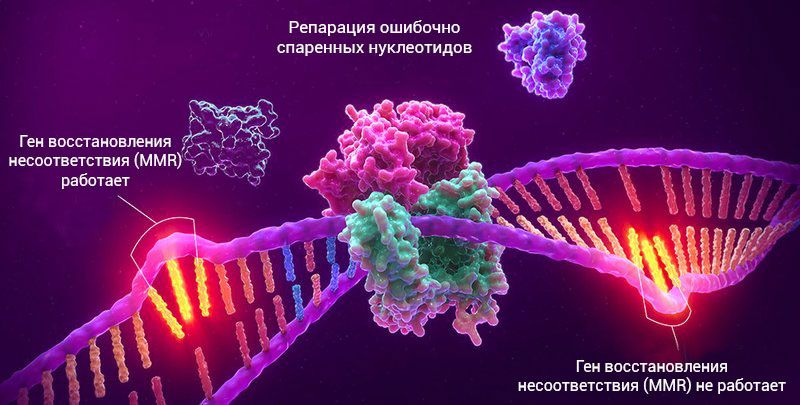
MSI-H приводит к тому, что гены, регулирующие ДНК (называемые генами восстановления несоответствия), не работают правильно. Гены восстановления несоответствия (MMR – mismatched repair) работают как генетические “проверки орфографии”, исправляя ошибки в ДНК по мере деления клеток, подобно тому, как исправляются опечатки в тексте.
Когда гены MMR перестают функционировать, то некоторые области ДНК могут стать нестабильными из-за накопления ошибок. Скрининговый тест MSI ищет изменения в последовательности ДНК между нормальной тканью и опухолевой тканью и может определить, существует ли высокая степень микросателлитной нестабильности, которая встречается примерно в 15% опухолей колоректального рака. Это часто происходит в опухолях, связанных с наследственным синдромом, синдромом Линча, хотя многие опухоли с высоким уровнем MSI являются спорадическими.
Дополнительный иммуногистохимический тест часто используется, чтобы сделать различие между наследственным и ненаследственным положительным анализом на микросателлитную нестабильность. Если MSI-H наследственная, то есть риск, что члены семьи онкологического больного также могут иметь синдром Линча, поэтому повышается вероятность развития колоректальных или других опухолей.
MSI-Н опухоли могут привлечь внимание иммунной системы. Под микроскопом в этих опухолях часто можно увидеть большое количество клеток иммунной системы. Иммунные клетки просто блокируются от полного выполнения своей работы. Поэтому пациенты с высоким уровнем микросателлитной нестабильности имеют положительный ответ на иммунотерапию. Таким образом, знание вашего состояния MSI чрезвычайно важно для выбора тактики противоопухолевого лечения.
MSS или микросателлитная стабильность обнаруживается приблизительно у 80-85% пациентов с колоректальным раком. Опухоли с мутацией MSS называются” холодными» и с точки зрения количества опухолевых генетических мутаций являются одним из наиболее сильно мутированных типов опухолей.