Злокачественный нейролептический синдром что это такое симптомы лечение
а) Этиология. В таблице ниже представлен перечень этиологических агентов, обусловливающих развитие нейролептического злокачественного синдрома (НЗС) (см. также «Галоперидол»).
Галоперидол, фенотиазины, бутирофеноны и тиоксантины — средства, которые наиболее часто ассоциируются с развитием этого синдрома. Критерии диагностики перечислены в таблице ниже.
б) Симптомы. Нейролептический синдром — это тетрада симптомов, включающая высокую температуру, ригидность, измененный сенсориум и автономную дисфункцию. Температура обычно варьирует в пределах от 38,5 до 42 °С.
Лихорадка может отсутствовать. Ригидность классически описывается как свинцовая труба. Другие нарушения включают тремор, гиперсаливацию, брадикинезию, семенящую походку, дистонию, хорею, тризм, опистотонус и дисфагии. Психическое состояние варьирует от легкой спутанности сознания и возбуждения до летаргии, ступора и комы.
Автономная дисфункция проявляется тахикардией, недержанием мочи, респираторным стридором, потоотделением, бледностью и остановкой сердца. На ранних стадиях заболевания у пациентов могут не обнаруживаться все классические симптомы.
Нейролептический злокачественный синдром часто проявляется в период 3—9 сут после начала лечения нейролептиками или после добавления второго нейролептического средства. Симптомы НЗС обычно развиваются через 24—72 ч и длятся 5—10 сут после прекращения приема нейролептического лекарственного средства.
г) Лабораторные исследования. Диагностические лабораторные данные по нейролептическому злокачественному синдрому (НЗС) отсутствуют.
Сообщалось о случаях околосуставного окостенения после нейролептического злокачественного синдрома (НЗС) и других нарушениях центральной нервной системы, но точный механизм этого явления неизвестен. Антихолинергические свойства нейролептических средств и ТЦА вызывают непроходимость кишечника, что приводит к некротическому энтероколиту.
е) Дифференциальная диагностика. Дифференциальная диагностика нейролептического злокачественного синдрома (НЗС) включает выявление причин лихорадки, лейкоцитоза и ригидности. У пациента с лихорадкой, ригидностью затылочных мышц и нарушенным процессом мышления необходимо исключить менингит.
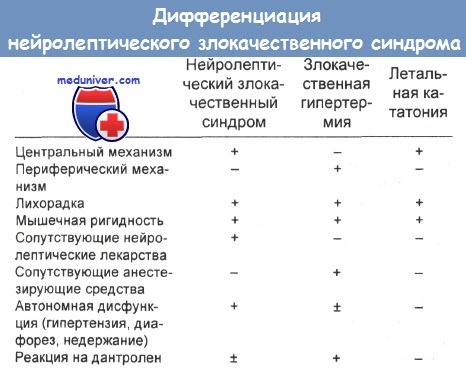
В таблицах ниже демонстрируется дифференцирование нейролептического злокачественного синдрома (НЗС) от злокачественной гипертермии и летальной кататонии, в отдельной статье сопоставлены серотониновый синдром, нейролептический злокачественный синдром и воздействие Экстази [3,4-метилендиоксиметамфетамина (МДМА)].
Нейролептический злокачественный синдром представляет собой критическое состояние, опасное для жизни. Пациентов необходимо наблюдать в отделениях интенсивной терапии.
Лечение нейролептического злокачественного синдрома
а) Прекращение приема антагониста дофамина
б) Поддерживающая терапия:
Снижение температуры тела
Лечение вторичных инфекций
Поддержание легочной, сердечно-сосудистой и почечной функций
Седативные средства
в) Дантролен-натрий:
1—3 мг/кг/сут внутривенно, введение в 4 приема
Можно увеличить до 10 мг/кг/сут внутривенно, введение в 4 приема
Пероральные поддерживающие дозы в пределах от 50 до 200 мг/сут
г) Бромокриптин: 2,5—10 мг перорально, сначала 3 раза в день
Если в течение 24 ч нет улучшения, увеличить до 20 мг перорально, 4 раза в день
д) Терапия с применением дантролена или бромокриптина или обоими препаратами начинается немедленно и продолжается до клинического улучшения состояния пациента или до нормализации уровня креатининкиназы
е) Обсуждение возможности применения электрошока

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Злокачественный нейролептический синдром
Несмотря на то, что я работал в больших психиатрических больницах, мне крайне редко приходилось встречаться со злокачественным нейролептическим синдромом. В нашей клинике за 10 лет я был свидетелем всего одного случая, закончившегося, к счастью, выходом из этого тяжелого и опасного состояния.
Впервые этот синдром был описан знаменитыми французами Delay, Deniker (1960, 1965), которые выделили его клинические симптомы. В настоящее время считается, что данный синдром может быть чаще всего вызван как классическими, так и атипичными антипсихотиками, однако, описаны случаи его появления в процессе терапии литием и некоторыми антидепрессантами. По мнению ряда неврологов злокачественный нейролептический синдром может возникнуть при резкой отмене агонистов дофамина в процессе лечения болезни Паркинсона.
По моему опыту, диагностика данного синдрома нередко бывает трудной, что обусловлено его вариабельностью, в частности, проявляющей себя в расширенном или узком спектре симптомов, нечеткости диагностических критериев. По отдельным литературным данным, максимальная частота встречаемости злокачественного нейролептического синдрома соответствует 2,4% случаев терапии антипсихотиками (Addonozio et.al., 1986), однако, чаще всего в источникам приводятся значительно меньшие цифры его распространенности (0,15-0,07%) (Keck et.al., 1991). Для развития злокачественного нейролептического синдрома у мужчин требуются более высокие дозы нейролептиков, чем у женщин, 80% случаев этого синдрома приходится на возраст старше 40 лет, причем смертность здесь достигает 30%.
Основными симптомами злокачественного нейролептического синдрома являются: помрачение сознания (от легкой обнубиляции до комы), выраженная дисфункция вегетативной нервной системы, подъем температуры и значительная мышечная ригидность. В дифференциально-диагностическом плане важно различать сонливость и седацию после введения антипсихотиков от изменения сознания при злокачественном нейролептическом синдроме. Вегетативная дисфункция проявляется колебаниями артериального давления, тахикардией, потливостью, гиперсаливацией. Недержание мочи может быть первым признаком синдрома у молодых пациентов, а повышение артериального давления более часто наблюдается в более старшем возрасте особенно если пациент до этого в течение длительного времени получал терапию нейролептиками. Подъем температуры наблюдается практически во всех случаях злокачественного нейролептического синдрома и может носить как умеренный, так и значительно выраженный характер, достигая 42 градусов. Подобная температура на фоне выраженной ригидности мышц считается неблагоприятным признаком в плане прогноза выхода из синдрома (коагулопатия, ацидоз, почечная недостаточность). Мышечная ригидность присутствует почти постоянно и не отвечает на терапию антихолинергическими препаратами, иногда ригидность даже захватывает лицевые мышцы и даже мышцы языка, что приводит к дисфагии и дизартрии. Некоторые авторы полагают, что изменения речи и способности к самостоятельному питанию могут быть первыми симптомами злокачественного нейролептического синдрома.
Лабораторным признаком синдрома считается подъем креатинфосфокиназы (от 2000 до 15000), что отчасти отражает большое содержание этого фермента в скелетных мышцах. Значительное снижение концентрации дофамина в центральной нервной системе считается основным патофизиологическим механизмом развития злокачественного нейролептического синдрома.
Перед началом его лечения, в первую очередь, необходима отмена нейролептиков, также прекращается терапия препаратами лития, антидепрессантами и антихолинергическими препаратами. Трициклические антидепрессанты и ингибиторы обратного захвата серотонина могут редуцировать дофаминергическую трансмиссию и тем самым усилить выраженность клинической симптоматики синдрома. Каждый два часа наблюдения за пациентом необходимо отслеживать динамику артериального давления, частоты пульса, измерять температуру. Несмотря на то, что купирование синдрома с помощью электросудорожной терапии в литературе оценивается неоднозначно, этот метод терапии в ряде случаев показал достаточно высокую эффективность. Из фармакологических средств для купирования мышечной ригидности и борьбы с ажиатацией применяются бензодиазепины, но последние, к сожалению, не останавливают прогрессирования патологического состояния. Бромокриптин (агонист дофамина) рекомендуют применять в течении короткого отрезка времени. Одним из эффективных препаратов, предложенных для купирования синдрома, считается мышечный релаксант ингибитор кальция — дантролен. Профилактика злокачественного нейролептического синдрома предполагает ограниченное использование депо-нейролептиков.
Нейролептический синдром
Общие сведения
Нейролептический синдром (нейролептические экстрапирамидные расстройства) – неврологические расстройства, возникающие при лечении антипсихотиками. Отличаются большим разнообразием, могут быть острыми или хроническими. В первые годы применения нейролептиков (в основном – аминазина) экстрапирамидные расстройства были настолько распространенными, что специалисты даже считали их обязательным следствием фармакотерапии и признаком, по которому можно оценивать эффективность того или иного препарата. В последующем, после более детального изучения принципов действия антипсихотиков и появления лекарственных средств нового поколения (атипичных нейролептиков) эта точка зрения была признана неверной.
Несмотря на уменьшение распространенности данного синдрома, проблема возникновения экстрапирамидных расстройств при лечении антипсихотиками не теряет своей актуальности. Исследователи утверждают, что каждый третий случай развития паркинсонизма обусловлен приемом лекарственных средств. Нейролептический синдром ухудшает качество жизни больных, влечет за собой снижение или утрату трудоспособности и негативно влияет на социализацию. Лечение нейролептического синдрома осуществляют специалисты в области психиатрии и неврологии.
Причины и классификация нейролептического синдрома
Причины развития нейролептического синдрома окончательно не выяснены. С учетом свойств антипсихотиков психиатры и неврологи предполагают, что неврологические расстройства провоцируются блокадой дофаминовых рецепторов и последующими компенсаторными реакциями, обуславливающими нарушение баланса нейротрансмиттеров и разрушение связей между таламусом и подкорковыми структурами. Нейролептический синдром может возникать при использовании любых нейролептиков, однако некоторые нарушения чаще выявляются при терапии типичными антипсихотиками.
С учетом времени появления различают три разновидности нейролептического синдрома: ранний, затяжной и хронический. Ранние экстрапирамидные расстройства появляются в первые дни лечения и исчезают после прекращения приема антипсихотиков. Затяжной нейролептический синдром диагностируется при продолжительной лекарственной терапии, нарушения исчезают в течение нескольких месяцев. Хронические экстрапирамидные расстройства развиваются при многолетней терапии и иногда сохраняются на протяжении всей жизни. С учетом преобладающей симптоматики выделяют пять видов нейролептического синдрома: нейролептический паркинсонизм, острая дистония, акатизия, поздняя дискинезия и злокачественный нейролептический синдром.
Клинические формы нейролептического синдрома
Нейролептический паркинсонизм
Является самой распространенной разновидностью нейролептического синдрома. Выявляется у 15-60% больных, получающих антипсихотические средства. Обычно возникает на начальном этапе лечения. Чаще наблюдается у пожилых женщин. Факторами риска являются когнитивные расстройства, курение, ЧМТ, сахарный диабет, органические поражения ЦНС и наличие случаев болезни Паркинсона в семье.
Нейролептический лекарственный паркинсонизм проявляется замедлением движений, мышечной скованностью, прерывистостью движений, дрожанием конечностей, оскудением мимики и гиперсаливацией. У многих больных выявляются характерные эмоциональные, когнитивные и социальные расстройства: безразличие, утрата способности получать удовольствие, замедление мышления, трудности при попытке сконцентрировать внимание, уменьшение количества социальных связей.
Дифференциальный диагноз проводят с другими формами паркинсонизма. В пользу нейролептического синдрома свидетельствует подострое начало, симметричность неврологических нарушений и незначительность постуральных расстройств. Симптомы не прогрессируют. Лечение – отмена, уменьшение дозы препарата или его замена другим антипсихотиком в сочетании с приемом холинолитиков. Обычно все проявления нейролептического синдрома исчезают в течение нескольких недель. При резистентных формах требуется увеличение дозы холинолитиков и экстракорпоральная детоксикация (гемосорбция, плазмаферез).
Острая дистония
Острая дистония возникает сразу после начала лечения или увеличения дозы. Вероятность развития нейролептического синдрома увеличивается при кокаинизме, алкоголизме, органической патологии ЦНС, гипокальциемии, нарушении функции щитовидных и паращитовидных желез. Чаще страдают молодые мужчины. Наблюдаются неврологические нарушения в виде медленных или быстрых непроизвольных движений. Вначале внезапно появляются мышечные спазмы в области головы и шеи. Возможно гримасничанье, высовывание языка, запрокидывание головы и т. п. Иногда развиваются ларингоспазм, фарингоспазм и обструкция дыхательных путей.
В последующем в насильственные движения вовлекаются мышцы туловища. Больной переразгибает спину в поясничном отделе, изгибается вправо или влево, иногда скручивается. Руки и ноги, как правило, не задействованы или мало задействованы. Спазмы часто причиняют боль и бывают настолько выраженными, что становятся причиной вывиха суставов. Выраженный ларингоспазм может представлять угрозу для жизни больного. Для устранения нейролептического синдрома уменьшают дозу или отменяют антипсихотик, вводят антихолинергические препараты.
Акатизия
Акатизия может начинаться как сразу после начала лечения (ранняя акатизия), так и на фоне длительной терапии (поздняя акатизия). Факторами риска являются женский пол, средний возраст, алкоголизм, лечение большими дозами препаратов, резкое увеличение дозы и использование типичных нейролептиков. Иногда эта форма нейролептического синдрома возникает после отмены или снижения дозы лекарственного средства и исчезает после возобновления терапии или увеличения дозы.
Данная патология проявляется непреодолимой потребностью в движении для устранения дискомфорта и внутреннего беспокойства. Больные ерзают, раскачиваются, переминаются, качают или стучат ногой, поглаживают голову, поправляют одежду и пр. Состояние тяжело переносится, может провоцировать депрессию и попытки суицида. Дифференциальный диагноз нейролептического синдрома проводят с другими неврологическими расстройствами, психозами и ажитированной депрессией. Лечение – отмена или снижение дозы антипсихотика. Иногда назначают антихолинолитики, бензодиазепины, бета-блокаторы и антигистаминные препараты. При неэффективности лекарственной терапии используют ЭСТ.
Поздняя дискинезия
Эта разновидность нейролептического синдрома возникает спустя несколько месяцев или лет после начала терапии. Факторами риска являются пожилой возраст, острый нейролептический синдром, женский пол, сахарный диабет, постклимактерический период, аффективные расстройства, болезнь Паркинсона у родственников, органические поражения головного мозга, курение, алкоголизм, использование типичных нейролептиков, большие дозы препаратов, прерывистое медикаментозное лечение и ЭСТ.
Вначале появляются непроизвольные движения лицевых мышц. Пациент высовывает язык, чмокает, облизывает губы, совершает сосательные или жевательные движения, гримасничает, надувает щеки. В тяжелых случаях возможны нарушения дыхания, ларингоспазм и фарингоспазм. В последующем в процесс вовлекаются туловище и конечности. Больной раскачивает и скручивает корпус, сгибает и разгибает кисти и пальцы стоп. Из-за мышечных спазмов ходьба искажается, приобретает причудливый характер.
Обычно нейролептический синдром не прогрессирует, неврологические нарушения выражены слабо или умеренно. Реже наблюдаются выраженные расстройства, становящиеся причиной инвалидизации пациентов. Поздняя дискинезия негативно влияет на самовосприятие, вызывает тревогу, гнев, стыд и чувство вины, затрудняет социализацию, может провоцировать депрессию, суицидальные намерения и действия. Лечение – отмена или уменьшение дозы нейролептика. Эффективность других способов лечения при данной форме нейролептического синдрома пока не удается точно оценить. Обычно психиатры используют холинолитики, антиоксиданты, бета-блокаторы, большие дозы витаминов и ботулинический токсин.
Злокачественный нейролептический синдром
По различным данным, злокачественный нейролептический синдром выявляется у 0,1-3,2% больных, получающих антипсихотики в условиях стационара. Может провоцироваться любыми нейролептиками и развиться на любом этапе лечения, однако чаще всего возникает в первую неделю терапии. Факторами риска являются истощение, нарушения водно-солевого обмена, аллергии, органическая патология ЦНС, деменция, ЧМТ, алкоголизм, инфекционные заболевания, высокая температура и влажность окружающей среды, ЭСТ, большие дозы или быстрое повышение дозы антипсихотиков.
Сопровождается выраженной гипертермией, вегетативными расстройствами (потливостью, гиперсаливацией, учащением пульса и дыхания, нестабильностью АД, недержанием мочи), повышением тонуса мышц и расстройствами сознания. Психические проявления могут варьировать от тревоги и возбуждения до спутанности сознания, кататонии, делирия, ступора и комы. Диагноз выставляется путем исключения других патологических состояний, способных вызвать подобные симптомы. Злокачественный нейролептический синдром дифференцируют с тяжелыми инфекциями, тепловым ударом, злокачественной гипертермией, опухолями мозга, синдромом длительного раздавливания и другими заболеваниями.
PsyAndNeuro.ru
Злокачественный нейролептический синдром или аутоиммунный анти-NMDA рецепторный энцефалит?
Этиология и патогенез ЗНС остаются до настоящего времени до конца не изученными. Большинство исследователей объясняют развитие ЗНС блокадой дофаминовых рецепторов в базальных ганглиях и гипоталамусе, а не прямым токсическим действием нейролептиков [13, 29]. У больных ЗНС отмечается подавление дофаминегрической и повышение адренегрической и серотонинергической активности [40]. Ряд исследователей рассматривает ЗНС как проявление острой нейролептической энцефалопатии [1]. При этом на ЭЭГ выявляются признаки метаболической энцефалопатии с генерализованным торможением электрической активности головного мозга [14, 43]. Результаты проведенных клинико-патогенетических исследований установили, что в патогенезе ЗНС и фебрильной шизофрении важную роль играют иммунологические нарушения и повышение проницаемости гематоэнцефалического барьера, с нейросенсибилизацией организма и последующим аутоиммунным поражением ЦНС, преимущественно гипоталамуса и висцеральных органов [9, 10]. Доказательством этого является высокая гуморальная сенсибилизация к различным аутоантигенам головного мозга с выявлением антител к лобной доли,зрительному бугру и максимальным количеством (до 66%) к гипоталамусу [9]. Причиной летального исхода являются нарастающие нарушения гомеостаза и, в первую очередь, водно-электролитного баланса и гемодинамики, явления отека мозга.
Анализ патоморфологических изменения у больных ЗНС с летальным исходом в мировой литературе не представлен. Обнаруженные патоморфологические изменения головного мозга при фебрильной (гипертоксической) шизофрении, а ряд исследователей рассматривают ЗНС как вызванную нейролептиками (drug-induced) форму летальной кататонии, не укладываются в какую-либо определенную нозологическую форму и могут быть отнесены к токсико-дистрофическому процессу в сочетании с генерализованными дисциркуляторными нарушениями. В таламо-гипофизарной области мозга у этих больных выявляются следующие изменения:
1) острое набухание, вакуализация, ишемия и гибель нервных клеток;
2) вздутие и набухание миелиновых оболочек ганглиоцитарных волокон;
3) гипертрофия и дистрофические изменения микроглиоцитов [7].
Факторами риска развития ЗНС является наличие у больных резидуальной церебральной органической недостаточности (перенесенные антенатальные и перинатальные вредности, черепномозговая травма, инфекции и интоксикации) [5, 9]. Предполагается, что физическое истощение и дегидратация, возникающие на фоне психомоторного возбуждения, могут приводить к повышению чувствительности к нейролептикам и способствовать развитию ЗНС [21, 43]. К факторам риска ЗНС относится также и наличие кататонических расстройств [43].
Диагностика ЗНС основывается на выявлении основных симптомов осложнения: центральной гипертермии, кататонической симптоматики с развитием ступора и мышечной ригидности, нарушения сознания, а также характерных изменений лабораторных показателей (умеренный лейкоцитоз без палочкоядерного сдвига, лейкопения и ускорение СОЭ, резкая активность КФК в плазме крови).
Наиболее ранним признаком развития ЗНС у больных шизофренией и шизоаффективным психозом, важным для диагностики осложнения, является появление экстрапирамидной симптоматики с одновременным обострением психоза и развитием кататонических расстройств в виде ступора с явлениями негативизма и каталепсии [5, 43] В связи с этим некоторые исследователи рассматривают ЗНС как нейролептический вариант злокачественной или фебрильной кататонии, относя их к заболеваниям одного спектра [3, 31, 30]. Это подтверждается как общностью клинических проявлений фебрильной шизофрении и ЗНС [7, 8, 41], так и сходностью биохимических и иммунологических нарушений [9], а также общими принципами терапии. Они включают отмену нейролептиков, назначение транквилизаторов, проведение инфузионной терапии и ЭСТ [5, 9, 14, 19, 36, 43, 45]. Эффективность агониста дофаминовых рецепторов бромокриптина и миорелаксанта дантролена при ЗНС не подтверждены доказательными исследованиями [6, 37, 38]. Имеются данные об эффективности плазмафереза и гемосорбции [3, 5]. Прогноз течения ЗНС зависит от того, насколько быстро отменяется нейролептическая терапия и назначается интенсивная инфузионная терапия, корригирующая гомеостаз. При своевременной отмене нейролептиков, адекватности проведения инфузионной терапии, дифференцированного применения методов ЭСТ удается в течение первых 3–7 дней добиться терапевтического эффекта у большинства больных [5], в соответствии с рекомендациями DSM-5 ЗНС необходимо дифференцировать с такими заболеваниями как вирусный энцефалит, объемные, сосудистые и аутоиммунные поражения ЦНС, а также с состояниями связанными с употреблением других лекарственных средств (амфетамины, фенциклидин, ингибиторы моноами-ноксидазы, серотонинергические антидепрессанты и рядом других препаратов).
В 2007 году были впервые описаны серии случаев, аутоиммунного NMDA рецепторного энцефалита, протекающего с психотическими симптомами и кататонией, вегетативными нарушениями и гипертермией, и риском развития летального исхода [16]. Симптоматика этого заболевания схожа с ЗНС и фебрильной кататонией и вызывает трудности дифференциальной диагностики [15, 23]. Заболевание вызывается антителами к NR1 и NR2-субединицами глутаматного NMDA-рецептора. Первоначально анти-NMDA рецепторный энцефалит был описан у молодых женщин с тератомами яичников [16]. В последующем вне связи с опухолевым процессом у лиц обоего пола и разных возрастов [26]. Диагностика анти-NMDA рецепторного энцефалита основывается на выявлении в плазме крови и спинномозговой жидкости аутоантител к NR1 и NR2-субъединицами глутаматного NMDA рецептора [17, 18, 20]. В последние годы случаи аутоимунного энцефалита были выявлены у больных психиатрических стационаров с первоначальными диагнозами шизофрения, шизоаффективное расстройство, нарколепсия и большое депрессивное расстройство [42, 46]. Лечение заболевания предусматривает проведение иммунотерапии с назначением иммуноглобулина и метилпреднизолона. Препаратами второй линии, которые используют при отсутствии эффекта, является ритуксимаб в сочетании с циклофосфамидом. Для купирования психомоторного возбуждения могут использоваться транквилизаторы, атипичные антипсихотики или хлопромазин [25, 44]. Имеется положительный опыт применения ЭСТ [12, 24, 27, 29, 32] и плазмафереза [11, 33].
Клинический случай
Больная Ш., 1988 года рождения, поступила на лечение в клиническую психиатрическую больницу №4 им. П.Б.Ганнушкина 18.06.2015 г. с диагнозом острое полиморфное психотическое расcтройство.
Анамнез. Наследственность психопатологией не отягощена. Беременность и роды у матери больной протекали без патологии. Родилась в срок. Старшая из 2-х детей. Имеет младшую сестру. Ранее развитие правильное. По характеру была спокойной, уравновешенной, общительной и активной. Переболела детскими инфекционными заболеваниями без осложнений. В школу пошла с 7 лет. Училась хорошо. Окончила 9 классов общеобразовательной средней школы, затем педагогический колледж и педагогический институт. В возрасте 22 лет вышла замуж. Проживала с мужем, от брака ребенок 3-х лет, отношения в семье хорошие. Работает в школе учителем младших классов. Вредных привычек не имеет. Со слов мужа, психическое состояние больной впервые изменилось с начала июня 2015 года. Стала рассеянной, забывчивой, тревожной. Постоянно переспрашивала близких: «покормила ли она ребенка?», «сходила ли в туалет», говорила, что у нее как будто «голова находиться отдельно от тела», временами неожиданно падала на пол, но сразу вставала. 16.06.2015 обратилась для обследования в ФГНБНУ Национального центра неврологии. На МРТ головного мозга выявлены признаки участка глиоза в правой теменной доле (8 мм–13 мм–18 мм), которые необходимо дифференцировать с ишемическим и демиелинизирующем или объемным процессом. Данных за наличие аневризм, артериовенозных мальформаций на изученных уровнях не получено. Вечером этого же дня стала тревожной,беспокойной, растерянной, спрашивала «что происходит вокруг?». Отмечался подъем систолического АД до 180 мм.рт.ст. Ночью была беспокойной. На следующий день стала высказывать нелепые идеи, считала, что ее «укусил клещ», что она беременна. Утверждала, что у нее в голове звучат песни. Периодически испытывала страх, тревогу, была обеспокоена тем, что не сможет работать, считала, что у нее «отберут ребенка», говорила «я умру», отмечала, что как будто ею кто-то управляет, движения происходят помимо ее воли. 18.06.2015 г. повторно обратилась в центр неврологии. На приеме была возбужденной, кричала «где моя мамочка?», разговаривала сама с собой, хаотично размахивала руками, рычала, плевалась. В связи с неадекватным поведением была осмотрена дежурным психиатром и госпитализирована в ПКБ №4 в недобровольном порядке.
Психическое состояние при поступлении. В отделение доставлена в сопровождении санитаров с мерами физического стеснения. Осмотрена в пределах постели. Продуктивному контакту мало доступна. Напряжена, тревожна, прислушивается к чему-то, озирается по сторонам. Отвечает только на шепотную речь. Ответы тихим голосом, краткие, чаще кивает или качает головой. Из беседы удается выявить, что не спала несколько ночей, испытывает наплывы мыслей в голове, «звучание мыслей». Не отрицает наличие «голосов», которые мешают спать и запрещают отвечать на вопросы. Отвечает преимущественно «не знаю». Временами громко кричит, извивается, плюётся.
Соматическое состояние: высокого роста, правильного телосложения, удовлетворительного питания. Кожные покровы и видимые слизистые обычной окраски. На правом локтевом сгибе следы от инъекций. На лице единичные красные высыпания. Температура тела в норме. Зев спокоен. В легких дыхание везикулярное, хрипов нет. ЧДД 16 в мин. Тоны сердца приглушены, ритмичны. ЧСС 82 уд/мин. АД 130/80 мм.рт.ст. Язык чистый, влажный. Живот при пальпации мягкий, безболезненный. Печень и селезенка не пальпируются. Симптом «поколачивания» отрицательный с обеих сторон. Отеков нет.
Неврологический статус: лицо симметричное, зрачки D=S, фотореакция сохранена. Отмечается повышение сухожильных рефлексов. Мышечный тонус не повышен. Менингеальных знаков нет, очаговая неврологическая симптоматика отсутствует.
Данные лабораторного обследования. Исследование общего клинического и биохимического анализов крови и мочи значимых патологических изменений не выявили, RW, ВИЧ, HBSAg, HCV –отрицательные, BD, BL – не выявлены. РПГА – столбняк – 0,77, дифтерия – 0,17. ЭКГ – синусовый ритм, ЧСС 55–62 в минуну. Нормальная ЭОС.
С целью профилактики пневмонии назначена антибактериальная терапия – цефтриаксон по 1,0 в/м 2 раз в день. С 13.07.2015 г. был отменен оланзапин и усилена инфузионная терапия до 1 200 мл/сут. Несмотря на проводимые терапевтические мероприятия, состояние оставалось тяжелым. Больная все время лежала в постели, отказывалась от еды, практически не реагировала на обращение, иногда отвечала только на шепотную речь, отмечались симптомы «восковой гибкости», сохранялись гипертермия и мышечная ригидность. 15.07.2015 г. была осмотрена дежурным неврологом скорой медицинской помощи.
Заключение: явления отека головного мозга на фоне интоксикационного синдрома. Рекомендовано проведение КТ головного мозга, МРТ с контрастом, перевод в стационар с реанимационным отделением. В 19:50 в сопровождении реанимационной бригады больная переведена в ПСО ГКБ им. С.П.Боткина для продолжения лечения и проведения обследования.
При поступлении состояние было расценено как тяжелое. Сохранялась заторможенность с элементами оглушения, не реагировала на обращенную речь, слабо реагировала на болевые раздражители. Отмечалось повышение тонуса в мышцах конечностей и шеи. Заторможенность, которая периодически сменялось возбуждением, ограниченным пределами постели, с повторением отдельных слов по типу речевых стереотипий. В соматическом статусе отмечались бледность кожных покровов, тахикардия до 110 уд. в мин., гипертермия. С целью дифференциальной диагностики демиелинизирующего заболевания и энцефалита проведена люмбальная пункция – цитоз 40 в 3мл, белок 0,33, лимфоциты 37, нейтрофилы 3. Антитела к вирусу Эпштейн-барра, вирус герпеса, микобактерии туберкулеза и к treponema pallidum в ликворе не обнаружены.
После осмотра инфекциониста диагноз вирусного энцефалита был снят. На МРТ головного мозга с контрастированием от 21.07.2015 г. выявлялась зона острого отека в семиовальных центрах справа, которое следует дифференцировать с острым нарушением мозгового кровообращения по ишемическому типу, опухолевым, димиелинизирующим и аутоиммунным заболеванием. Полученные результаты иммунотипирования лимфоцитов ликвора лимфопролиферативное заболевание не подтвердили. В отделении реанимации проводилась инфузионная терапия до 2 л. в сутки под контролем диуреза, дезинтоксикационная терапия, антибактериальная терапия (цефритиаксон, амоксициклин). С 24.07.2015 в схему лечения добавлен дексаметазон 12 мг/сут в/в капельно. Несмотря на проводимую терапию состояние больной оставалось тяжелым отмечалось повышение температуры тела до 40º С, падение артериального давления.
Заключение консилиума врачей от 29.07.2015. Состояние больной тяжелое, сохраняется фебрильная лихорадка и кататоническая симптоматика. Наиболее вероятным представляется наличие у больной фебрильной шизофрении. Выявленные на МРТ-исследовании изменения, учитывая их несоответствие клинической симптоматики, по всей видимости, является случайной находкой и могут быть последствием перенесенного ранее нарушения мозгового кровообращения.
Разбор
Тщательное соматическое, лабораторное и инструментальное обследование, в том числе исследование спинномозговой жидкости и МРТ головного мозга с контрастированием, установить причину, которая бы могла лежать в основе развития тяжелого психического и соматического состояния больной не смогло.
Смерь больной наступила на фоне гипертермии и нарастающих явлениях отека мозга, несмотря на отмену нейролептиков, проведение интенсивной терапии и назначения дексаметазона. Данные патологоанатомического исследования выявили у больной проявление аутоиммунного энцефалита с поражением подкорковых структур мозга, что явилось основанием для расхождения диагноза. В то же время у больной не проводились исследования крови и спинномозговой жидкости на выявление аутоантител к NMDA-рецепторам на основании которых диагностируется аутоиммунный энцефалит. Кроме того результаты патоморфологического исследования не противоречат диагнозу ЗНС, поскольку в проведенных клинико-патогенетических исследованиях была доказана важная роль аутоиммунной патологии с преимущественным поражением гипоталамуса в патогенезе развития фебрильных приступов шизофрении [9].
Известно, что нейролептики соединяясь с белками плазмы крови приобретают свойства гаптенов к которым начинают образовываться антитела, блокирующие их антипсихотическое действие [3]. Они же при определенных условиях, по всей видимости, способны спровоцировать развитие аутоиммунного процесса и вызвать развитие ЗНС. Следует отметить, что алгоритм диагностики ЗНС до последнего времени не предполагал исследование крови и спинномозговой жидкости на наличие аутоантител к NMDA-рецепторам. При этом в мировой литературе имеются описания случаев, когда первоначально выставленный диагноз ЗНС пересматривался после обнаружения в крови и ликворе аутоантител к NMDA-рецепторам [23]. Можно предположить, что ранняя диагностика ЗНС с отменой нейролептиков, назначения адекватной инфузионной терапии и проведение ЭСТ позволило бы предотвратить летальный исход. Однако особенностью данного случая явилось то, еще до момента манифестации психоза у больной выявлялись изменения на МРТ мозга в виде участка глиоза, что непозволяло полностью исключить наличие текущего органического заболевания ЦНС и поставить диагноз эндогенного заболевания – шизофрении или шизоаффективного психоза опираясь на структуру психопатологических расстройств.
Литературные сслыки можно просмотреть в оригинале