Лечение аденокарциномы
Аденокарцинома – это онкологический процесс, приводящий к развитию злокачественного образования в железистых и эпителиальных клетках. Из этих клеток состоят практически все органы тела человека, поэтому аденокарцинома может появиться в любом внутреннем органе человеческого организма.
Причины возникновения аденокарциномы:
Если определять причину возникновения аденокарциномы связанные с каким-то конкретным органом, то стоит отметить¸ аденокарцинома поджелудочной железы начинает развиваться из-за курения и хронического панкреатита. Аденокарцинома желудка возникает в связи с хроническими язвами желудка, полипами. Аденокарцинома толстой кишки – причинами могут быть колит, полипы, длительные запоры, свищи. Аденокарцинома простаты может возникнуть в связи с генетической предрасположенностью, возрастными гормональными изменениями.
Виды аденокарциномы
С учетом уровня дифференцировки клеток различают три вида аденокарциномы:
Лечение аденокарциномы
Лечение аденокарциномы проводится с помощью хирургического вмешательства, химиотерапии, лучевой терапии, иммунотерапии и некоторые другие.
В клинике «Семейная» лечение аденокарцином осуществляются с применением самых современных методик – лапароскопии и эндоскопии. После таких малоинвазивных операций пациенты гораздо быстрее восстанавливаются и возвращаются к привычной жизни. Лечение проводится комплексно, с участием врачей разных специальностей.
Запись на прием к врачу онкологу
Обязательно пройдите консультацию квалифицированного специалиста в области онкологических заболеваний в клинике «Семейная».
Стадии рака
Все опухоли (или, на языке врачей — новообразования) делят на две большие группы: доброкачественные и злокачественные. Первые обычно не опасны для жизни, а вторые, если человек не получает лечения, приводят к гибели. В 2015 году от рака во всем мире умерло почти 9 миллионов человек.
Фатальность злокачественных опухолей связана с двумя их главными свойствами, которые, собственно, и отличают их от доброкачественных новообразований:
Для врача важно понимать, насколько сильно рак успел распространиться в организме пациента. Ведь от этого зависит лечение и прогноз. Для того чтобы упростить эту задачу и внести четкость, в течении каждого онкологического заболевания принято выделять определенные стадии.
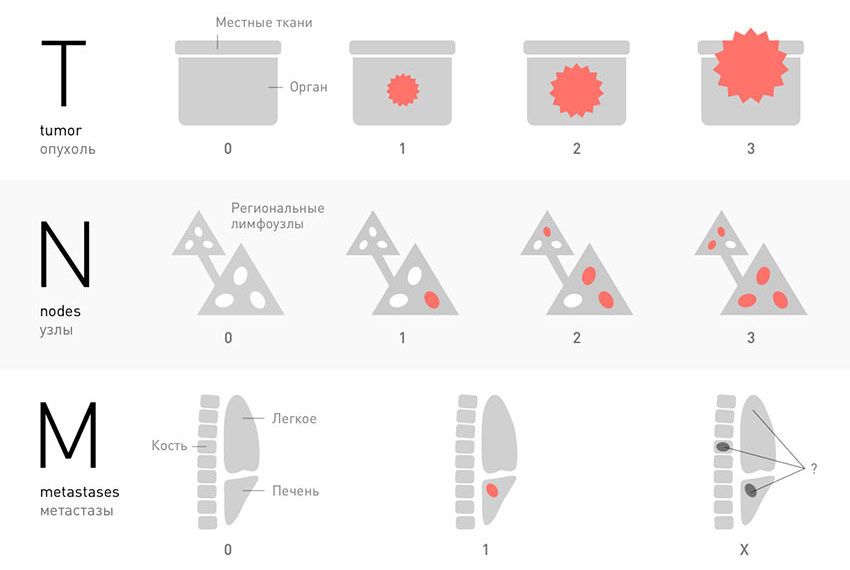
Классификация TNM
В большинстве случаев, для того чтобы установить стадию рака, ориентируются на три характеристики злокачественной опухоли, которые соответствуют трем буквам аббревиатуры TNM. К каждой букве приписывают индекс в виде цифры или специального обозначения.
T — tumor. Эта буква обозначает первичную опухоль, ее размеры, прорастание в стенку органа, соседние ткани:
N — nodus. Когда раковые клетки отрываются от первичной опухоли и мигрируют с током лимфы, в первую очередь они попадают в близлежащие (регионарные) лимфатические узлы. Можно сказать, что это первые баррикады на пути распространения рака в организме. В зависимости от того, обнаружены ли опухолевые клетки в регионарных лимфатических узлах, N может принимать значения:
M — metastasis. Эта буква показывает, обнаружены ли в теле больного отдаленные метастазы — вторичные очаги в различных органах:
Классификация TNM применима для большинства видов рака. Она позволяет очень подробно описывать злокачественные опухоли. В пределах основных групп выделяют подгруппы, их обозначают с помощью букв, например: T1a, T1b, T1c.
Однако, зачастую система TNM оказывается слишком громоздкой и не совсем удобной. Существует ее упрощенный вариант, когда возможные сочетания значений T, N и M сводят к пяти стадиям.
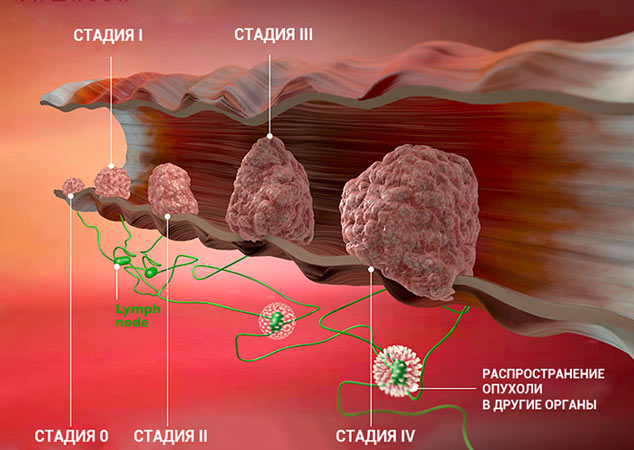
Стадии злокачественной опухоли
Часто онкологи обозначают стадию рака римской цифрой от I до IV. Эта классификация основана на TNM, но она проще и зачастую удобнее:
Это очень приблизительное описание стадий. Деление зависит от типа рака, от того, в каком органе он находится. Для того чтобы обозначить подстадию, к букве приписывают цифру. Например, стадия I может делиться на подстадии IA и IB.
Сторожевой лимфатический узел
Когда хирург оперирует онкологического пациента, зачастую ему приходится решать сложную задачу: стоит ли удалять регионарные лимфатические узлы? Если в них есть раковые клетки, и они будут оставлены в организме больного, произойдет рецидив. Если же удалить «чистые» лимфоузлы, это чревато осложнением в виде лимфедемы — отека на руке или ноге из-за нарушения оттока лимфы.
Раньше врачи нередко предпочитали меньшее из зол и удаляли лимфатические узлы «на всякий случай». Современные хирурги уже не действуют вслепую и могут более точно определить показания к лимфодиссекции. Это стало возможно благодаря появлению сентинель-биопсии или биопсии сторожевого лимфатического узла.
Сторожевым называется лимфатический узел (или группа лимфатических узлов), который первым принимает лимфу, оттекающую от злокачественной опухоли. Его можно обнаружить во время операции: для этого нужно ввести в опухоль флуоресцентный краситель или препарат с радиоактивной меткой. Препарат проникает в лимфатические сосуды, затем в сигнальный лимфоузел и «прокрашивает» его. Лимфатический узел удаляют и проверяют, нет ли в нем раковых клеток.
Для обозначения состояния сигнального лимфоузла используют специальную классификацию:
Если в сигнальном лимфоузле обнаружена опухолевая ткань — это показание к удалению регионарных лимфоузлов.
Степень злокачественности
Злокачественность и степень дифференцировки — два показателя, которые тесно взаимосвязаны. Они описывают внешний вид раковых клеток под микроскопом. Степень дифференцировки показывает, насколько раковая клетка отличается от здоровой. Если она высокая — опухолевая ткань похожа на здоровую. Низкодифференцированные раковые клетки полностью теряют сходство с нормальными.
Чем ниже степень дифференцировки и выше злокачественность, тем агрессивнее ведет себя рак и быстрее распространяется в организме. Для оценки используют гистологическую классификацию:
Шкала Глисона при раке простаты
Для того чтобы оценить степень злокачественности и агрессивности рака предстательной железы, используют шкалу Глисона, разработанную в 1960-х годах. В зависимости от того, как опухолевая ткань выглядит под микроскопом, ей присваивают оценку от 1 до 5. Чем ниже оценка, тем более высокодифференцированными и менее злокачественными являются клетки. Патологоанатом должен выявить два преобладающих типа ткани и выставить две оценки. Итоговая сумма баллов может колебаться от 2 до 10. Чем она больше, тем агрессивнее ведет себя опухоль, и выше риски.
Классификации рака печени
Классификация TNM не очень хорошо отражает течение злокачественных опухолей печени, поэтому в разных странах были созданы специальные классификации печеночно-клеточного рака. Например, многие врачи используют Барселонскую клиническую классификацию. В ее рамках выделяют следующие стадии рака печени:
В некоторых странах практикуется классификация итальянской программы по изучению рака печени (CLIP). В ней учитывается четыре фактора: состояние функции печени, распространение опухолевых очагов (больше или меньше половины печени), уровень альфа-фетопротеина (опухолевый маркер) и наличие тромбоза портальной вены. По каждому показателю врач выставляет оценку 0, 1 или 2 балла. Выживаемость пациентов зависит от суммы баллов:
В соответствии с системой CLIP, всех больных печеночно-клеточным раком можно поделить на две группы: 0–2 балла — значительно более благоприятный прогноз; более 2 баллов — значительно менее благоприятный прогноз.
В 1985 году была предложена классификация Okuda, в которой учитываются: степень поражения печени, наличие асцита (скопления жидкости в брюшной полости), изменение уровня альбумина и билирубина в крови. В соответствии с классификацией Okuda, выделяют три стадии рака печени:
Почему важно установить стадию злокачественной опухоли?
Знание стадии рака по TNM и другим системам помогает онкологу решать важные задачи:
Единые классификации помогают врачам из разных клиник и стран «разговаривать на одном языке». Видя стадию опухоли, диагностированную в другой клинике, онколог четко понимает, что это значит, и как дальше работать с пациентом.
Рак яичников-современный взгляд на проблему (по данным обзора литературы)
Среди множества патологических процессов наибольший интерес у теоретиков и клиницистов во все времена вызывали те из них, которые чаще всего приводили к гибели или инвалидизации больных. Без преувеличения можно сказать, что самым тяжелым и коварным заболеванием злокачественного генеза у женщин является рак яичников (РЯ). Проблема этой патологии была и остается одной из самых актуальных и трудных разделов онкологии, и поэтому широко обсуждается в различных областях медицины.
Рак яичников (РЯ) наряду со злокачественными опухолями шейки и тела матки является одним из наиболее распространенных заболеваний онкологической природы и в мировой статистике занимает третье место. По данным литературы, карцинома яичников составляет 6-8% из числа всех онкологических заболеваний и 20-25% среди злокачественных опухолей женских половых органов, причем рак яичников составляет около 80% всех опухолей придатков.
Анализ тенденций заболеваемости и смертности и их географических особенностей позволяет приблизиться к пониманию некоторых аспектов этиологии и патогенеза данного заболевания (Макаров О.В., 1996).
В настоящее время накоплено значительное количество экспериментальных, эпидемиологических и клинических фактов, позволяющих обозначить многие стороны этиопатогенеза РЯ, несмотря на это причины возникновения большинства опухолей яичников остаются неизвестными. Обзоры многочисленных исследований указывают на высокую частоту рака яичника в индустриальных странах, за исключением Японии. Возможно, это обусловлено диетическими факторами, а именно, высоким потреблением животных жиров, хотя последние исследования не подтверждают связи развития РЯ ни с высококалорийной пищей, ни с употреблением алкоголя, кофеина и никотина. Нет и убедительных доказательств возможного канцерогенного эффекта радиации, применяемой в диагностических и терапевтических целях, в развитии РЯ, хотя в эксперименте моделей опухоли яичника создавали путем облучения грызунов рентгеновскими лучами или при помощи пересадки ткани яичника в селезенку или другие органы портальной системы. В нескольких исследованиях развитие карцином яичников связывают с использованием талька в гигиенических целях.
Л.В. Акуленко с соавт. (1998) предложили критерии идентификации наслед-ственных форм РЯ. Таковыми являются:
Ранняя диагностика РЯ остается главной нерешенной проблемой в онкогинекологии. Клиническое ректо-вагинальное обследование малого таза нередко позволяет идентифицировать новообразование яичников. С 1970-х годов благодаря внедрению ультразвуковых технологий наступила новая эра в диагностике опухолей яичника. Ультразвуковое исследование малого таза стало рутинным методом в обследовании пациентки при подозрение на опухоль яичника. При небольших новообразованиях в малом тазу наибольшей информативностью обладает трансвлагалищная эхография, при образованиях более 6-7 см возрастает роль трансабдоминальной эхографии. Рак яичника на ранних стадиях эхографически представляет собой кистозное образование с единичными сосочковыми образованиями с нечеткими контурами, тогда как при 1С и ІІ стадиях уже визуадизируются обширные папиллярные разрастания с нарушением целостности капсулы кисты и в позадиматочном пространстве определяется небольшое количество жидкости. Для генерализованных стадий РЯ эхографически характерно наличие неправильной формы опухолевого конгломерата кистозно-солидного строения с размытыми границами разрастаниями по наружному контуру. Асцит выявляется в 70-80% набдюдений. При выявлении эхографических признаков злокачественности опухолевого процесса в яичниках и за их пределами необходимо дифференцировать первичность и вторичность поражения яичников.
Эхографические критерии дифференциальной диагностики первичного и метастатического рака яичников
Критерии: первичный рак, метастатический рак
Сторона поражения: чаще двустороннее всегда двустороннее
Структура кистозно-солидная: преимущественно кистозная Солидная,реже-с некрозом в центре
Размеры опухоли: свыше 10 см До 10 см
Контуры опухоли: нечеткие,неровные Четкие, бугристые
Связь с маткой: в конгломерате с маткой связь с маткой отсутствует
Современные стандарты лечения рака яичников были сформированы Интернацио¬нальной группой по изучению рака яичников на 7-ой международной конферен¬ции по онкогинекологии, проходившей в Риме в 1999.
При раке яичников различают пять типов хирургических вмешательств:
При ранних стадиях РЯ, к которым относят la, Ib и Па, в качестве хирургиче¬ского этапа лечения необходимо выполнять пангистерэкгомию с экстирпацией боль¬шого сальника на уровне поперечно-ободочной кишки. Для обоснования ранней ста¬дии, обязательно производится цитологическое исследование перитонеальной жидко¬сти, при её наличии, смывов с брюшины малого таза, боковых карманов брюшной полости, печени и диафрагмы. При низкодифференцированных опухолях необходима биопсия тазовых и парааортальных лимфоузлов. У молодых женщин с высокодиффе-ренцированным раком яичников или опухолями пограничной злокачественности, при желании пациентки сохранить детородную функцию, возможен органосохраняющий объем операции: односторонняя аднексэктомия с обязательной резекцией второго яичника, оментэктомией и цитологическим контролем. В подобных наблюдениях, которые чрезвычайно редки, после родов выполняют экстирпацию матки с оставшимися придатками. Следует помнить, что органосохраняющие операции при раке яичников — это исключение, а не правило.
Лапароскопия при подозрении на РЯ выполняется только в диагностиче-ских целях. Рядом авторов этот метод рекомендован для биопсии тазовых и парааортальных лимфатических узлов, как стандартный. Необходимо избегать неадек¬ватных лапароскопических вмешательств для хирургического лечения рака яич¬ников.
При подтверждении ранней стадии РЯ, адьювантная химиотерапия может не выполняться в случаях пограничной злокачественности и при высокодифференциро-ванном раке. В остальных случаях рекомендована комбинированная химиотерапия в количестве 4-6 циклов препаратами платины с алкилирующими агентами. Примене¬ние таксанов и антрациклинов при индукционной химиотерапии при ранних стадиях РЯ остается дискуссионным. Эффективность таких методов, как лучевая терапия и гормональное лечение при ранних стадиях РЯ не доказана.
При местно-распространенном и диссеминированном процессе, к которому ряд авторов причисляет и 1с стадию, в связи с наличием опухолевых клеток по брюшине, хирургическое вмешательство всегда должно быть этапом комплексно¬го лечения и носить циторедуктивный характер. Оптимальной циторедуктивной операцией считается субтотальная гистераднексэктомия или пангистерэктомия с экстирпацией большого сальника, с уменьшением остаточных опухолевых масс, по мнению разных авторов, от 0,5 до 2 см3. Только оптимальная циторедукция может быть основанием для постановки ШЬ стадии, при которой отдаленные ре¬зультаты заметно лучше, по сравнению с Шс стадией, в которой к сожалению, на¬ходится более половины больных, получивших комплексное лечение. В повседневной клинической практике встречают ситуации, когда полное удаление опухоли невозможно. Массивный канцероматоз, тотально замещенный опухолью “панцирный” большой сальник, прорастание опухоли в диафрагму, ворота печени и ее паренхиму, малый сальник, брыжейку тонкой кишки, забрюшинные пространства часто вынуждают хирурга минимизировать объем хирургического вмешательства. Вместе с тем, всегда следует стремиться к удалению первичной опухоли, большей части сальника и крупных опухолевых узлов на париетальной брюшине.
При Шс стадии объем вмешательства может быть уменьшен только из-за невозможности удаления масс опухоли без повреждения жизненноважных органов. Удаление лимфатических узлов забрюшинного пространства при РЯ, по мнению многих хирургов, носит диагностический характер. Дополнение операции аппендэктомией, спленэктомией, удалением пораженных отделов кишки, может проводиться только с целью достижения условной радикальности операции. Паллиативные вмешательства при нарастании кишечной непроходимости производятся с целью улучшения качества жизни больных. При массивных отдаленных метастазах в пе¬чень и легкие циторедуктивное вмешательство не показано. В свою очередь, около 10% больных раком яичников при первичном обращении оперировать не представляется возможным. Основными причинами подобных клинических ситуаций являются прорастание первичной опухоли в смежные органы и мягкие ткани малого таза, тотальный канцероматоз и множественные метастазы в органы брюшной полости, асцит, плевриты, отягощенное соматическое состояние, пожилой и старческий возраст, резко ослабленное состояние больных. Лечение этой категории больных начинается с системной полихимиотерапии. В результате короткого курса индукционной химиотерапии (2-4 цикла) примерно 30% больных представляется возможным выполнить промежуточную циторедуктивную операцию. Операция предпринимается с целью уменьшения массы первичной опухоли и ее метастазов и, таким образом, повысить эффективность последующей химиотерапии, а также улучшить качество жизни больных. Доказано, что промежуточная циторедуктивная операция повышает выживаемость больных раком яичников.
Прогноз больных раком яичников зависит, прежде всего, стадии заболевания (распространенности процесса), гистологического строения опухоли и плоидности опухолевых клеток. Далее следуют: степень дифференцировки клеток опухоли, экспрессия онкогена HER-2/neu, скорость размножения опухоли, размеры остаточной опухоли после хирургического вмешательства, выраженность асцита и возраст больной. Наиболее неблагоприятным прогнозом отмечаются больные с массивными диссеминированными формами злокачественных эпителиальных опухолей яичников. Полисерозиты и отдаленные метастазы у больных пожилого и старческого возраста, у которых верифицирован светлоклеточный или низкодифференцированный серозный рак с анэуплоидией клеток опухоли сводят шансы на излечение больной практически к нулю. В то время, как высокодифференцированные злокачественные опухоли яичников любого гистологического строения IА и IВ стадий излечиваются в 95-100% наблюдений. Приведенные факторы прогноза у больных запущенными формами рака яичников в связи с массивным распространением и большим суммарным объемом опухоли существенного прогностического значения не имеют, а любые методы лечения носят лишь паллиативный характер.
Статья добавлена 27 марта 2013 г.
Недифференцированный рак носоглотки
Общая информация
Краткое описание
Для практической работы наибольшее признание в онкологических учреждениях получила Международная гистологическая классификация опухолей носоглотки.
Название: Недифференцированный рак носоглотки
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Всем больным необходимо проведение тщательного инструментального отоларингологического осмотра, пальцевое обследование рото- и носоглотки.
1. Рентгенологические методы диагностики: стандартные рентгенологические укладки (боковой снимок носоглотки, прямой снимок придаточных пазух носа), а также обзорная краниография в аксиальной и полуаксиальной проекциях, позволяют в большинстве случаев получить достаточный объем информации.
2. В более сложных случаях необходимо применение рентгеновской томографии и компьютерной томографии, которая имеет большее диагностическое значение. По показаниям – КТ или МРТ головного мозга с контрастированием.
Лабораторная диагностика
Лечение
Профилактические мероприятия: профилактика цитотоксических, постлучевых осложнении, симптомов ВЧД – сопроводительная терапия (антибактериальная, антиэметогенная, колоностимулирующая, дезинтоксикационная, дегидратационная, гармонотерапия, и т.д.).
Дальнейшее ведение: после окончания лечения необходимо регулярное обследование с целью выявления рецидивов или прогрессирования заболевания – КТ или МРТ с контрастированием.
Что такое первичный рак неизвестного происхождения?
Раковая опухоль возникает в случаях, когда клетки начинают бесконтрольно расти. Такую особенность могут приобрести клетки практически любого органа. Кроме того, по мере роста опухоли они с током крови или лимфы могут переноситься в другие области тела, оседать там и давать начало росту новых очагов. Такие очаги называют вторичным раком, или метастазами, а начальную опухоль, соответственно, первичным раком.
Метастазы в любых органах классифицируют в зависимости от того, из какого органа изначально происходит опухоль. Например, вторичный очаг рака легких в печени все равно будет называться раком легких, только получит приставку «вторичный». Иногда не получается определить, в каком именно органе сначала возникла опухоль. Однако при исследовании выявляются ее метастазы в других частях тела. Если их первичный очаг определить не удается, то врачи говорят про первичный рак неизвестного происхождения, или скрытый первичный рак.
Пример выявления
Скрытый первичный рак встречается нечасто. Более того, в ходе дальнейших обследований первичный очаг может обнаружиться. Если так происходит, то опухоль более не считается первичным раком неизвестного происхождения. Ей присваивают название в соответствии с органом происхождения и, опираясь на новые данные, модифицируют схему лечения онкологического заболевания.
На практике это происходит следующим образом:
Однако в ряде случаев даже самое тщательное обследование не позволяет обнаружить первичный очаг. Более того, его не всегда получается найти даже при патологоанатомическом исследовании.
Типы раковых опухолей
Обычно опухоли классифицируют по их первичной локализации. Однако их также можно сгруппировать по типам клеток, по тому, как раковые клетки выглядят под микроскопом. Знание типа клетки может дать врачам ключ к пониманию того, из каких тканей или органов происходит данная опухоль.
Карциномы
Карцинома — это рак, который происходит из клеток, выстилающих внутреннюю или внешнюю поверхности различных органов нашего тела. Такие клетки называются эпителиальными. Наиболее распространенные типы карцином:
1) Плоскоклеточный рак
Самым ярким примером плоских клеток являются клетки, встречающиеся на поверхности кожи. Кроме того, они составляют часть слизистых оболочек многих полых органов. Плоскоклеточный рак может возникать в ротовой полости, в горле, пищеводе, легких, прямой кишке, на шейке матки, во влагалище и некоторых других органах.
2) Аденокарциномы
Эти злокачественные новообразования развиваются из железистых клеток, то есть из тех, которые способны производить какие-либо вещества. Железистые клетки входят в состав очень многих органов нашего тела, в том числе и тех, которые формально не считаются железами. Например, большинство видов раковых опухолей желудка, кишечника и толстой кишки представляют собой именно аденокарциномы и примерно 4 из 10 случаев рака легких также являются аденокарциномами.
Другие виды злокачественных опухолей
Из других типов клеток раковые новообразования возникают реже. К таким опухолям относятся:
Итак, при первичном раке неизвестного происхождения не всегда получается установить орган, где изначально возникла опухоль. Однако, исследуя под микроскопом клетки вторичного очага, чаще всего удается отнести их к одной из пяти категорий:
В дальнейшем эта информация поможет более точно идентифицировать опухоль и в конечном итоге обнаружить ее первичный очаг.
Зачем нужно искать первичный очаг?
Основная причина для поисков начальной опухоли — выбор правильной тактики лечения. Вторичные метастатические очаги состоят из тех же клеток, что и начальная опухоль, даже если развиваются в совершенно других органах. Значит, для их лечения будут эффективны те же препараты, что и для терапии первичного рака, а не те, которые используются при лечении онкопатологий органа, где развился метастаз.
Это имеет особенно важное значение при некоторых формах рака, которые хорошо поддаются лечению определенными химиотерапевтическими или гормональными препаратами. Например, такими особенностями характеризуются многие опухоли молочной железы. Их можно эффективно лечить гормональными средствами. А значит, такие же препараты подойдут и для терапии их метастазов в костях, головном мозге, печени.
К сожалению, предугадать развитие злокачественного заболевания пока практически невозможно. А потому наиболее эффективным способом борьбы с опухолями является выявление рака на 1 стадии развития. В этом случае успешному лечению поддаются более 90% всех злокачественных новообразований. Обнаружить опухоль на начальных этапах возникновения можно только при помощи периодических скринигов. Такие скрининговые программы действуют и в медицинском центре «Анадолу». На первичной консультации специалист-онколог оценит риск развития у вас онкологического заболевания и составит индивидуальный план прохождения профилактических обследований для ранней диагностики рака.
Материал подготовлен по согласованию с врачом «Анадолу», терапевтом и медицинским онкологом Шерефом Комурджу.