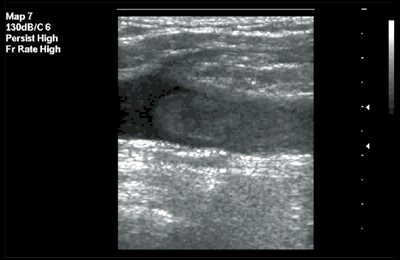
4.4. Дуплексное сканирование при тромбозе вен нижних конечностей.
Основные задачи ультразвуковой диагностики при подозрении на острый тромбоз глубоких вен включают:
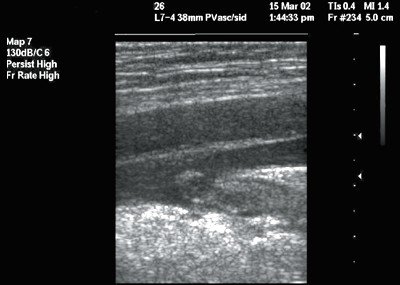
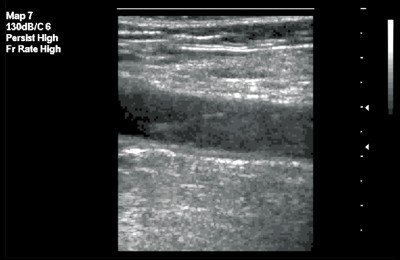
Поскольку свежий тромб по эхоплотности не отличается от крови, ультразвуковыми признаками заболевания являются эктазия вены, отсутствие «дыхания» ее стенок, неполное их смыкание или отсутствие реакции вены на компрессию датчиком (Рис.19). Режим цветового кодирования потоков позволяет дифференцировать дефект заполнения сосуда при неокклюзивном тромбе или отсутствие заполнения при окклюзии просвета сосуда. Неокклюзивный тромб проявляется также наличием на поперечных эхограммах симптома сомкнутого или разомкнутого кольца вследствие «смывания» тромба кровью. Допплеровские спектрограммы демонстрируют снижение кровотока в свободной зоне и его отсутствие в области расположения тромба. Уже в раннем периоде выражен ускоренный коллатеральный кровоток по подкожным венам.

Рис. 19. Острый окклюзивный тромбоз общей бедренной вены.
Флотирующий тромб в условиях специализированной клиники наблюдается редко, что обусловлено поздним обращением больных в результате неоправданной «этапности» оказания медицинской помощи и низкого уровня диагностики в районных поликлиниках. Для флотирующего тромба характерно перемещение головки тромба в просвете вены (Рис.20), его «омывание» кодированным по цвету потоком, низкая скорость кровотока в зоне тромба и дистальнее его, отсутствие дыхательных волн.
В возрасте 5-7 дней в структуре тромба появляются изменения, свидетельствующие о начальных процессах организации: в результате выпадения фибрина эхогенность образования неравномерно повышается, более плотные участки располагаются в виде разводов на гипоэхогенном фоне. Характерные признаки окклюзивного тромба – «зияние» вены, наличие тромботических масс в ее просвете, отсутствие колебательных движений стенок, неспадаемость просвета при компрессии, отсутствие кровотока (Рис. 21).
Важным диагностическим тестом окклюзионного поражения является потеря компрессивности при надавливании датчиком. Компрессивность вены оценивается в продольном и поперечном сечении, сила сдавления датчиком контролируется по деформации просвета корреспондирующей артерии. Однако при оценке этого критерия необходимо учитывать клиническую картину и срок заболевания, так как при «свежих» тромбозах тест нужно использовать с осторожностью в связи с опасностью фрагментации тромба. Кроме того, «свежие» тромбы за счет своей незрелости и мягкой структуры могут давать почти полную сжимаемость просвета.

|  Рис. 20. Верхушка флотирующего тромба в просвете ствола БПВ (а – в приустьевом сегменте; б – в нижней трети бедра).
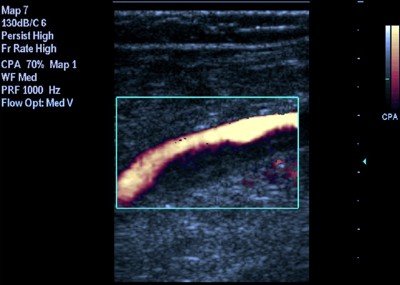
Рис. 21. Окклюзивный тромбоз: а – общей бедренной вены; б – поверхностной бедренной вены; в – мышечно-венозного синуса камбаловидной мышцы. В случае неокклюзивного тромба вена расширена, при компрессии датчиком спадается не полностью, визуализируются неровные контуры неоднородных тромботических масс, кровоток в просвете сосуда снижен, без дыхательных волн. Коллатеральные пути оттока расширены, скорость кровотока по ним возрастает. После двух недель от момента заболевания тромботические массы уплотняются, появляются первые признаки реканализации просвета вены. При допплеровском исследовании возможна регистрация резко ослабленного кровотока. Коллатеральный кровоток ускорен. В дальнейшем формируется симптомокомплекс посттромботической болезни. Следует отметить важность ультразвукового исследования не только на этапе диагностики и принятия решения (вопрос особенно актуален при принятии решения о постановке кава-фильтра, пликации нижней полой вены, перевязке магистральной вены), но и в процессе дальнейшего госпитального лечения для оценки динамики изменений, определения фиксированности головки тромба. Исключительная роль отводится ультразвуковому исследованию и в период дальнейшего наблюдения и оценки степени изменений венозной системы нижних конечностей. Систематическое и полноценное клиническое и инструментальное наблюдение позволяет предотвратить тяжелые осложнения посттромботической болезни, своевременно предпринять необходимые шаги для коррекции венозной гемодинамики. Удаление тромбов из артерийКратко о методе леченияУдаление тромбов (тромбэктомия) может быть отдельным видом лечения, но чаще его компонентом. Тромбоз сосуда может образоваться вследствие его сужения или расширения, фрагмент тромба может быть принесен из других артерий или сердца. Тромботические массы в просвете сосудов блокируют кровоток и вызывают недостаточность кровообращения, которая может привести к гангрене органа или конечности. Современная сосудистая хирургия имеет ряд технологий, позволяющих удалять тромботические массы из сосудов. Преимущества лечения в ИСЦВ нашей клинике для удаления тромбов применяются как традиционные технологии, так и малоинвазивные современные методы. Показания и противопоказания к методу леченияПодготовка к лечениюВ случае острых тромбозов операция по удалению тромбов должна проводиться по срочным показаниям с целью спасения конечности. Срочность операции зависит от степени недостаточности кровообращения и срока заболевания. Подготовка к такому вмешательству минимальная. Обезболивание при леченииВыбор метода анестезии зависит от предполагаемого объема вмешательства и общего состояния больного. При операциях на артериях ног мы чаще всего используем эпидуральную анестезию, иногда для тромбэктомии применяется местная анестезия. Если необходимо удалять тромб из аорты или подвздошных артерий, либо предполагается увеличение объема операции, то мы можем использовать общий наркоз. Как проходит метод леченияУдаление тромбов зондом ФогартиОткрытая тромбэктомия с помощью зонда Фогарти проводится через разрез. Разрез обычно проводится ниже места тромботической закупорки артерии, так как удаление тромбов облегчается по току крови. Если у пациента тромбоз аорты или подвздошных артерий в животе, то разрез выполняется в паховой области, если тромбоз в подколенной артерии, то доступ проводится на голени или на стопе. После выделения и оценки состояния артерии на ней проводится надрез 3-5 мм в который проводится баллонный зонд Фогарти в сжатом состоянии. Для лучшей упругости в зонд устанавливаетмя металлический проводник, который после прохождения зонда выше тромба извлекается. К зонду присоединяется шприц, через который проводится раздувание баллона. После этого хирург извлекает раздутый баллон, который подталкивает тромботические массы к разрезу артерии. Давление крови выше тромба помогает процессу удаления тромба. После извлечения тромба процедура повторяется, для того, чтобы быть уверенным в полном удалении. На артерии устанавливаются сосудистые зажимы и отверстие в ней ушивается сосудистым швом. После этого рана послойно ушивается Такая несложная операция хорошо помогает при острой закупорки неизмененных артерий тромбоэмболом (тромбом принесенным из сердца или из более крупных артерий), однако если наступает тромбоз артерий, пораженных атеросклерозом, то тромбэктомия зондом Фогарти становится невозможной или даже опасной, так как зонд легко разрывается об острые края атеросклеротических бляшек или может зацепиться за бляшку и надорвать ее. Поэтому для таких случаев мы используем другие методы удаления тромбов. Удаление тромбов зондом Rotarex StraubeВозможные осложнения при леченииПри использовании зонда Фогарти возможны следующие осложнения:Такие осложнения встречаются довольно редко. Частота их уменьшается по мере накопления опыта тромбэктомий в клинике. В нашей клинике мы не наблюдаем таких осложнений на протяжении последних пяти лет. Осложнения при тромбэктомии Rotarex:Подобные осложнения обычно выявляются по ходу операции и обычно сразу устраняются. Прогноз после метода леченияПрограмма наблюдения после метода леченияПосле удаления тромбов и устранения причин их появления пациент нуждается в наблюдении сосудистого хирурга. Во время нахождения в стационаре хирург оценивает компенсацию кровообращения и скорость кровотока с помощью допплерографии. При выписке пациенту назначается антитромботическая терапия, в зависимости от причин тромбоза. Это могут быть препараты типа плавикса, варфарина, аспирина. Через месяц после выписки необходимо провести контрольное ультразвуковое дуплексное сканирование артерий, чтобы оценить состояние восстановленных сегментов и компенсацию кровообращения. Необходимо так же оценивать возможные источники тромбоэмболии (полости сердца, аорту) с использованием эхокардиографии. ЗаболеванияУдаление тромбов (тромбэктомия) из артерий проводится в случаях острой закупорки. Чаще всего тромбэктомия является вмешательством, которое устраняет только закупорку артерий, но не ее причины и поэтому рассматривается как элемент лечения. Только в случаях закупорки артерии тромбом, принесенным из сердца (тромбоэмболии) удаление тромбов становится самостоятельным методом лечения. Для операции на артериях пораженных атеросклерозом предпочтительно использовать методы зондовой тромбэктомии Rotarex, при тромбоэмболиях оптимальным методом является удаление тромбов с помощью баллонного зонда Фогарти. Основные показания для тромбэктомии1. Острые артериальные эмболии. Метод имеет преимущество перед классической тромбэктомией катетером Фогарти. Не требуется открытый доступ к артерии, вмешательство осуществляется через прокол. В случае раннего обращения ликвидируются все последствия артериальной непроходимости и больной может быть выпущен из стационара на следующий день. Возможность удаления эмболов и тромбов в аорте и подвздошных артериях. 2. Артериальный тромбоз на фоне атеросклеротических бляшек (атеротромбоз). Rotarex позволяет удалять тромботические массы из артерии пораженной атеросклерозом без повреждения сосудистой стенки. Кроме того срезаются мягкие атеросклеротические бляшки. После удаления тромба возможна ангиопластика и стентирование пораженных артерий. При поражении подвздошных артерий (синдром Лериша) удаление тромба из подвздошной артерии позволяет выполнить операции небольшого объема вместо аорто-бедренного шунтирования. Такая возможность особенна важна у пожилых и ослабленных пациентов, имеющий высокий риск открытой операции. 3. Удаление тромбов из сосудистых протезов. Повторные операции на артериях при закрытии протезов очень тяжелая техническая задача. Риск нагноения и кровотечения повышается в несколько раз. Использование технологии Rotarex позволяет восстаналивать проходимость сосудистых протезов без сложного хирургического доступа. Специальный зонд удаляет не только тромб, но и вновь образовавшуюся избыточную внутреннюю оболочку, которая суживает анастомоз и приводит к тромбозу. Ультразвуковая диагностика венозного тромбоза в амбулаторных условияхУЗИ аппарат RS85Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования. ВведениеОсновными механизмами внутрисосудистого образования тромбов, известными со времен R.Virchow, являются замедление тока крови (стаз), гиперкоагуляция, травма стенки сосуда (повреждение эндотелия). Острый венозный тромбоз достаточно часто развивается на фоне различных онкологических заболеваний (злокачественные опухоли желудочнокишечного тракта, женской половой сферы и др.) в силу того, что раковая интоксикация вызывает развитие гиперкоагуляционных изменений и угнетение фибринолиза, а также из-за механического сдавления вен опухолью и прорастания ее в сосудистую стенку. Предрасполагающими факторами ТГВ считаются также ожирение, беременность, прием оральных гормональных контрацептивов, наследственные тромбофилии (дефицит антитромбина III, протеина C и S, лейденовская мутация и др.), системные заболевания соединительной ткани, хронические гнойные инфекции, аллергические реакции [3, 4]. Наибольшему риску развития ТГВ подвержены больные пожилого и старческого возраста и лица, страдающие хронической венозной недостаточностью нижних конечностей, а также пациенты с инфарктом миокарда, декомпенсированной сердечной недостаточностью, инсультом, пролежнями, гангреной нижних конечностей. Особую тревогу вызывают травматологические больные, так как переломы бедренной кости в основном встречаются у лиц пожилого и старческого возраста, наиболее отягощенных соматическими заболеваниями [5]. Тромбозы у травматологических больных могут возникнуть при любой травме нижних конечностей, так как при этом имеют место все этиологические факторы тромбоза (повреждение сосуда, венозный застой и изменения свертывающих свойств крови) [6]. Надежная диагностика флеботромбоза является одной из актуальных клинических задач. Физикальные методы обследования позволяют поставить правильный диагноз лишь в типичных случаях заболевания, при этом частота диагностических ошибок достигает 50% [7]. Так, например, тромбоз вен икроножных мышц при сохраненной проходимости остальных вен нередко протекает бессимптомно. Из-за опасности пропустить острый ТГВ голеней клиницисты зачастую ставят этот диагноз в каждом случае появления болей в икроножных мышцах [8]. Особое внимание заслуживают «травматологические» больные, у которых наличие боли, отека и изменения окраски конечности могут быть следствием самой травмы, а не ТГВ. Иногда первым и единственным проявлением подобного тромбоза служит массивная ТЭЛА. В задачи инструментального обследования входят не только подтверждение или опровержение наличия тромба, но также определение его протяженности и степени эмбологенности. Выделение эмболоопасных тромбов в отдельную группу и изучение их морфологической структуры имеют большое практическое значение, так как без этого невозможны разработка эффективной профилактики легочной эмболии и выбор оптимальной тактики лечения. Тромбоэмболические осложнения чаще наблюдаются при наличии флотирующего тромба с гетерогенной структурой, неровным гипо- или изоэхогенным контуром в отличие от тромбов, имеющих гиперэхогенный контур и гомогенную структуру. Важным критерием эмбологенности тромба является степень его подвижности в просвете сосуда. Эмболические осложнения чаще отмечаются при выраженной и умеренной подвижности тромбомасс [9, 10]. Из всех неинвазивных методов, применяемых для диагностики тромбоза, в последнее время все чаще используется ультразвуковое сканирование венозной системы. Метод триплексного ангиосканирования, предложенный Barber в 1974 г., включает исследование сосудов в В-режиме, анализ допплеровского сдвига частот в виде классического спектрального анализа и цветового картирования потока (в скоростном и энергетическом режимах). Использование спектральной допплерографии позволило точно измерять кровоток внутри просвета вен. Применение метода цветового допплеровского картирования (ЦДК) обеспечило возможность быстро отличать окклюзирующий тромбоз от неокклюзирующего, выявлять начальные стадии реканализации тромбов, а также определять местоположение и размер венозных коллатералей. При исследованиях в динамике ультразвуковой метод позволяет обеспечить достаточно точный контроль за эффективностью тромболитической терапии. Кроме того, с помощью ультразвукового исследования можно установить причины появления клинической симптоматики, сходной с таковой при патологии вен, например выявить кисту Бейкера, межмышечную гематому или опухоль. Внедрение в практику ультразвуковых приборов экспертного класса с датчиками частотой от 2,5 до 14 МГц позволило достичь практически 99% точности диагностики. Материал и методыВсем обследуемым проводилось триплексное сканирование венозной системы на современных ультразвуковых аппаратах линейным датчиком с частотой 7 МГц. При этом оценивалось состояние вен бедра, подколенной вены, вен голени, а также большой и малой подкожных вен. Для визуализации подвздошных вен и НПВ использовался конвексный датчик с частотой 3,5 МГц. При сканировании НПВ, подвздошных, большой подкожной вены, бедренных вен и вен голени в дистальном отделе нижних конечностей пациент находился в положении лежа на спине. Исследование подколенных вен, вен верхней трети голени и малой подкожной вены проводилось в положении пациента лежа на животе с валиком, подложенным под область голеностопных суставов. Затруднения в диагностике возникали при визуализации дистального отдела поверхностной бедренной вены у тучных пациентов, визуализации вен голени при выраженных трофических и индуральных изменениях тканей. В этих случаях также использовался конвексный датчик. Глубину сканирования, усиление эхо-сигнала и другие параметры исследования подбирали индивидуально для каждого пациента и сохраняли неизменными во время всего обследования, включая наблюдения в динамике. Сканирование начинали в поперечном сечении для исключения наличия флотирующей верхушки тромба, о чем свидетельствовало полное соприкосновение венозных стенок во время легкой компрессии датчиком. Убедившись в отсутствии свободно флотирующей верхушки тромба, компрессионную пробу датчиком проводили от сегмента к сегменту, от проксимальных отделов к дистальным. Предлагаемая методика является наиболее точной не только для выявления тромбоза, но и для определения его протяженности (исключая подвздошные вены и НПВ, где проходимость вен определялась в режиме ЦДК). Продольное сканирование вен подтверждало наличие и характеристики венозного тромбоза. Кроме того, продольное сечение использовалось для локации анатомического слияния вен. Во время обследования оценивались состояние стенок, просвет вен, локализация тромба, его протяженность, степень фиксации к сосудистой стенке. Ультразвуковая характеристика венозных тромбов проводилась по отношению к просвету сосуда: они различались как пристеночные, окклюзирующие и флотирующие тромбы. Признаками пристеночного тромбоза считались визуализация тромба с наличием свободного кровотока в просвете вены, отсутствие полного спадения стенок при компрессии вены датчиком, наличие дефекта заполнения при ЦДК, наличие спонтанного кровотока при спектральной допплерографии (рис.1). Рис. 1. Неокклюзирующий тромбоз подколенной вены. Продольное сканирование вены. Огибающий кровоток в режиме энергетического кодирования потока. Результаты исследованияС 2003 по 2006 г. были обследованы 236 пациентов в возрасте от 20 до 78 лет, из них 214 с клиникой острого тромбоза и 22 с клиникой ТЭЛА. В первой группе в 82 (38,3%) случаях проходимость глубоких и поверхностных вен не была нарушена и клиническая симптоматика обусловлена иными причинами (табл. 1).
Вероятные причины (факторы риска) развития венозного тромбоза представлены в табл. 2.
В наших наблюдениях наиболее часто выявлялись распространенная форма тромбоза, а также поражение вен на уровне подколенно-берцового и бедренно-подколенного сегментов (табл. 3).
Рис. 2. Флотирующий тромб в общей бедренной вене. В-режим, продольное сканирование вены. Тромб гетероэхогенной структуры с четким гиперэхогенным контуром. Рис. 3. Флотирующий тромб в поверхностной бедренной вене. В-режим, продольное сканирование вены. Тромб изоэхогенной структуры с гиперэхогенным контуром. Рис. 4. Флотирующий тромб в поверхностной бедренной вене. В-режим, продольное сканирование вены. Тромб гомогенной эхоструктуры с четким контуром. В группе пациентов с клиникой ТЭЛА у 5 (22,7%) больных имел место ТГВ различных стадий развития (преимущественно бедренно-подколенный сегмент). В динамике для оценки течения тромботического процесса были обследованы 82 пациента, из них у 63 (76,8%) отмечалась частичная реканализация тромботических масс. В этой группе у 28 (44,4%) больных наблюдался центральный тип реканализации (при продольном и поперечном сканировании в режиме ЦДК реканализационный канал визуализировался в центре сосуда); у 23 (35%) пациентов диагностирована пристеночная реканализация тромботических масс (чаще кровоток определялся вдоль стенки вены, непосредственно прилежащей к одноименной артерии); у 13 (20,6%) больных выявлялась неполная реканализация с фрагментарным асимметричным окрашиванием в режиме ЦДК. Тромботическая окклюзия просвета вены наблюдалась у 5 (6,1%) больных, в 6 (7,3%) случаях отмечалось восстановление просвета вены. Признаки ретромбоза сохранялись у 8 (9,8%) обследованных. ВыводыКомплексное ультразвуковое исследование, включающее ангиосканирование с использованием спектрального, цветового и энергетического допплеровских режимов и эхографию мягких тканей, является высокоинформативным и безопасным методом, позволяющим наиболее достоверно и быстро решать вопросы дифференциальной диагностики и лечебной тактики в амбулаторной флебологической практике. Это исследование целесообразно проводить на амбулаторном этапе для более раннего выявления пациентов, которым не показана (а иногда и противопоказана) тромболитическая терапия, и направления их в профильные отделения; при подтверждении наличия венозного тромбоза необходимо выявлять лиц с высоким риском развития тромбоэмболических осложнений; наблюдать в динамике за течением тромботического процесса и тем самым корректировать лечебную тактику. ЛитератураУЗИ аппарат RS85Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 в
в