Способы противоишемической защиты почки при органосохраняющем хирургическом лечении больных почечно-клеточным раком
Полный текст
Аннотация
Преимущества органосохраняющих операций на почках заключаются в улучшении функциональных результатов, уменьшении числа пациентов с терминальной хронической почечной недостаточностью в отдаленном послеоперационном периоде и связанных с ней сердечно-сосудистых осложнений и, как следствие, в повышении качества жизни больных. С одной стороны, сухое операционное поле необходимо для визуализации края резекции, а с другой — его создание запускает процесс острого ишемического повреждения ткани оперируемой почки. Каждая минута ишемии пропорционально повышает риск развития почечной недостаточности в отдаленном послеоперационном периоде. Особенно важно учитывать продолжительность ишемии при операциях на единственной почке, при двустороннем опухолевом поражении почек, а также при наличии хронической почечной недостаточности. После резекции почки ее остаточная функция зависит от предоперационного уровня клубочковой фильтрации, количества сохраненной в ходе операции паренхимы и длительности ишемии почки. Прогнозируемая функциональная недостаточность «здоровой» контралатеральной почки в послеоперационном периоде составляет 18 %. Возможность развития или усугубления уже имеющейся хронической почечной недостаточности вследствие прогрессирования нефросклероза достигает почти 80 %. Риск развития хронической почечной недостаточности III стадии и выше в отдаленные сроки после резекции почки составляет более 30 %. Таким образом, развитие прецизионной хирургии, а также поиск средств противоишемической защиты почки представляют важную задачу, направленную на сохранение максимального объема функционирующей почечной паренхимы.
Ключевые слова
Полный текст
Любое органосохраняющее оперативное пособие по поводу заболевания почки сопровождается ее ишемическим повреждением и может приводить к острому или хроническому нарушению функции органа. Даже среди пациентов с элективными показаниями к резекции почки, по данным литературы, частота развития послеоперационных урологических осложнений (острой почечной недостаточности, мочевых свищей, гнойно-воспалительных процессов, инфаркта почки) в зависимости от нозологии и объема оперативного вмешательства достигает 9 % [1, 2]. Прогнозируемая функциональная недостаточность «здоровой» контралатеральной почки в послеоперационном периоде составляет 18 % [3], а вероятность развития хронической почечной недостаточности вследствие прогрессирования нефросклероза — почти 80 % [4]. Развитие хронической почечной недостаточности III стадии и выше в отдаленные сроки после резекции почки составляет более 30 % [5]. Потеря почечной функции снижает продолжительность жизни, повышая риск развития сердечно-сосудистых заболеваний и их летальных осложнений [6–9].
После резекции остаточная функция почек зависит от предоперационного уровня клубочковой фильтрации, количества сохраненной в ходе операции паренхимы, длительности ишемии почки во время резекции [10].
Так называемая тепловая ишемия почки (временное пережатие почечных сосудов) является основным фактором, запускающим процесс острого ишемического повреждения почки во время органосохраняющей операции [11]. Особенно актуальна продолжительность гемостаза при операциях на единственной почке, при двустороннем опухолевом поражении почек, а также при наличии хронической почечной недостаточности [10]. В 2007 г. R.H. Thompson et al. [12], проанализировав результаты масштабного многоцентрового исследования, посвященного влиянию тепловой ишемии на функцию единственной почки после открытой органосохраняющей операции по поводу опухоли, сделали вывод, что к более частому развитию нарушений функции почки приводит тепловая ишемия, продолжающаяся более 20 мин. Исследования М.С. Мосояна и др. (2014) показали, что даже при среднем времени тепловой ишемии, равном 14,4 мин, снижение почечной функции наблюдается уже через 24 ч и продолжается не менее 1 года [13]. F. Porpiglia et al. (2012) выявили стойкое снижение скорости клубочковой фильтрации через 3 мес. после тепловой ишемии почки без тенденции к дальнейшему ухудшению [14]. R.H. Thompson et al. (2010) отметили значительное повышение вероятности развития острой почечной недостаточности при проведении резекции почки в условиях тепловой ишемии, чем без нее [15]. Установлено, что на отдаленные функциональные результаты резекции почки влияет каждая минута ишемии [16, 17]. Исследования J.D. Choi et al. (2012) показали, что тепловая ишемия более 28 мин через 3 мес. после операции снижает скорость клубочковой фильтрации на 22,4 %, а через 12 мес. — на 30,6 %, в то время как при продолжительности тепловой ишемии менее 28 мин скорость клубочковой фильтрации значимо не меняется [17]. В исследовании С.Б. Петрова и др. (2009) время тепловой ишемии более 15 мин приводило к ультраструктурному повреждению нефронов и снижению клубочковой фильтрации на 20–30 % [18].
Обратимость возникающих во время тепловой ишемии изменений зависит от выраженности нарушения кровообращения в органе (гипоксия, неполная или тотальная ишемия). Снижение функции оперированной почки после длительного ишемического воздействия нивелируется при наличии функции контралатеральной почки [19].
Факторы, влияющие на продолжительность тепловой ишемии и вероятность развития осложнений, оценивали в исследованиях с использованием шкал R.E.N.A.L. и PADUA, которые включали такие характеристики опухоли почки, как диаметр, близость к полостной системе, локализация (передняя/задняя, медиальная/латеральная) и вовлечение чашечно-лоханочной системы. Используя при подготовке к органосохраняющей операции эти шкалы, можно спрогнозировать время тепловой ишемии, интраоперационное нарушение целостности чашечно-лоханочной системы почки, объем кровопотери и спланировать ход резекции. Независимыми предикторами времени тепловой ишемии более 20 мин и осложнений в целом являются не только анатомические характеристики опухоли, но и опыт хирурга [20, 21].
ПРИМЕНЕНИЕ МЕТОДА ХОЛОДОВОЙ ИШЕМИИ
Холодовая ишемия почки на сегодняшний день наиболее известный и широко применяемый метод длительной защиты почки и сохранения ее функции. Защитное действие метода заключается в снижении интенсивности энергетических процессов путем охлаждения резецируемой почки. Противоишемическую защиту осуществляют либо перфузией стерильными охлажденными растворами через почечную артерию, либо при помощи замороженных компонентов (льда), которые располагают вокруг органа. Холодовая ишемия — достаточно трудоемкий процесс, приводящий к общей гипотермии организма, вследствие этого она не получила достаточного признания при интракорпоральной резекции почки. Ее используют при экстракорпоральной резекции почки с последующей ее аутотрансплантацией у пациентов с большими, центрально расположенными новообразованиями, когда органосохраняющая операция in situ предполагает длительную ишемию и в связи с этим зачастую становится технически невыполнимой. Методика экстракорпоральной операции является сложной, трудоемкой и травматичной с высоким риском развития сосудистых осложнений, кровотечения и некроза мочеточника [22–25]. Б.К. Комяков и др. (2012) представили способ интракорпоральной консервации — холодовой ишемии при резекции почки in situ в условиях ее полного интракорпорального отключения от кровотока и постоянной селективной перфузии охлажденным раствором Кустодиола [26]. В клинической практике метод позволяет продлить время ишемии до 95 мин с хорошими послеоперационными результатами. Интракорпоральная консервация способствует радикальности резекции любой сложности с минимальным риском волемических, метаболических и гипотермических осложнений (потеря почечной функции); устраняет необходимость в аутотрансплантации органа, снижая травматизм и длительность оперативного вмешательства [26].
СОКРАЩЕНИЕ ВРЕМЕНИ ТЕПЛОВОЙ ИШЕМИИ
По данным ряда исследований, среднее время тепловой ишемии в ходе открытой резекции почки составляет 14–21 мин, а при опухолях единственной почки или опухолях большого размера — 38 мин. При лапароскопической резекции почки время ишемии колеблется от 27 до 35 мин, а при робот-ассистированной — от 19,7 до 32,1 мин. Таким образом, продолжительность тепловой ишемии почки по различным причинам не всегда остается в рамках «безопасной» [27]. Поиск путей сокращения времени ишемизации органа ведут многие авторы.
Сократить общее время тепловой ишемии можно путем применения методик, сокращающих время, необходимое для ушивания дефекта почки. Например, техника «скользящей клипсы» может сократить тепловую ишемию до 7 мин за счет отсутствия дополнительных швов. На операционный дефект накладывают клипсы Hem-o-lok, размещенные на обоих концах нити, которые сдвигают манипуляторами, повышая натяжение при ушивании паренхимы почки, для достижения надежного гемостаза и позиционирования паренхимы [28].
С.Н. Димитриади и др. (2014) предложили метод сокращения времени тепловой ишемии при лапароскопической резекции почки, суть которого состоит в исключении отдельного ушивания вскрытой полостной системы: наложение гемостатических швов происходит с использованием техники «скользящих клипс» без применения дополнительных гемостатических материалов. Авторы отмечают, что данная методика не повышает риска образования мочевых свищей [29].
С целью сокращения времени тепловой ишемии почки можно прибегать к раннему удалению зажима: кровоток по почечной артерии восстанавливается после наложения первого ряда швов на паренхиму почки с поврежденными сосудами и элементами собирательной системы почки. Этот метод вдвое сокращает время тепловой ишемии и может использоваться при любых малоинвазивных оперативных вмешательствах [30].
Уменьшение времени тепловой ишемии может быть достигнуто также при помощи специальных шовных материалов, например нити V-Loc — монофиламентного рассасывающегося шовного материала с насечками для самофиксации с целью профилактики прорезывания ткани паренхимы почки при осуществлении окончательного гемостаза [31].
СОКРАЩЕНИЕ ПЛОЩАДИ ИШЕМИИ
Ишемизация почечной паренхимы в зависимости от распространенности может носить глобальный (включать весь орган — при пережатии сосудистой ножки) или регионарный (парциальный) характер. Таким образом, осуществляя временный гемостаз при органосохраняющей операции на почке, можно корректировать объем ишемического повреждения органа путем:
Пережатие всей почечной ножки служит причиной бóльших патологических изменений, нежели пережатие только почечной артерии [32]. Возможно, из-за несоответствия реального и безопасного времени в последние годы разрабатывается концепция так называемой нулевой ишемии. Этим термином обозначают способы выполнения вмешательства, не приводящие к ишемическому повреждению даже части органа.
Беззажимная техника подразумевает резекцию опухоли без пережатия почечной ножки и при нормальном уровне артериального давления. Данная операция может сопровождаться значительным, зачастую неконтролируемым, объемом кровопотери из ложа удаленной опухоли, но позволяет максимально сохранить количество функционирующих нефронов. Из-за опасности развития кровотечения технику no-clamping применяют ограниченно — только при резекции опухолей небольшого размера с преимущественно экстраренальным ростом [13, 33].
Селективная диссекция и клипирование питающих опухоль артерий третьего или четвертого порядка является наиболее технически сложным способом защиты почки от ишемического повреждения органа при резекции. Анатомической предпосылкой служит радиальный тип кровоснабжения почки и, соответственно, сегментарная структура. В почке принято выделять пять сегментов, каждый из которых кровоснабжается отдельной веткой почечной артерии: верхний, нижний, передневерхний, передненижний и задний. Это позволяет удалить патологически измененную часть почки без нарушения функции органа в целом с сохранением оставшейся функционирующей паренхимы. I.S. Gill et al. (2012) описали 15 случаев роботической и 43 случая лапароскопической резекции почки в условиях нулевой ишемии без пережатия почечной ножки путем микродиссекции почечных артерий, питающих опухоль, 3-го и более порядка и наложения на них зажимов типа «бульдог» с положительными послеоперационными результатами [34].
Суперселективная эмболизация почечных артерий, питающих опухоль, выполняемая до резекции почки, позволяет отказаться от интраоперационного пережатия почечных сосудов и повысить безопасность лапароскопического вмешательства. G. Simone et al. (2011) описали 7-летний опыт выполнения лапароскопической резекции почки в условиях нулевой ишемии путем трансартериальной эмболизации опухоли с положительными результатами. Авторы предложили использовать данную методику при опухолях со средними значениями нефрометрии [31]. По мнению Ю.Г. Аляева и др. (2016), данная методика имеет ряд преимуществ: предотвращает тепловую ишемию нормальной паренхимы почки, которая в последующем могла бы негативно сказаться на ее функции; делает возможным проведение резекции в случаях сложной сосудистой анатомии, когда мобилизация почечной артерии, а тем более сегментарных сосудов технически сложна или невозможна; ведет к снижению интраоперационной кровопотери, что положительно сказывается на общем течении послеоперационного периода; способствует расширению показаний к использованию суперселективной эмболизации при лапароскопических операциях. В качестве недостатка метода авторы отмечают ухудшение визуальной дифференцировки между опухолевой и здоровой тканью в ходе резекции по линии демаркации [32].
Метод контролируемой гипотензии, при котором системное артериальное давление снижается до 65 мм рт. ст., позволяет выполнить резекцию почки без пережатия почечных сосудов с минимально возможной геморрагией. I.S. Gill et al. (2012) описали хорошие результаты 12 случаев лапароскопической и 3 случая робот-ассистированной резекции почки по поводу маленьких опухолей (1–4 см в диаметре) без наложения зажима на сосудистую ножку с фармакологической гипотонией до 60 мм рт. ст. в течение 1–5 мин. Однако при таких низких цифрах артериального давления, особенно в условиях пневмоперитонеума, резко нарушается фильтрация в почечных клубочках и могут страдать жизненно важные кислород-зависимые органы (сердце, головной мозг). С учетом этого многие авторы не считают этот метод достаточно безопасным.
G.L. Martin et al. (2012) сравнивали тотальную, селективную и неартериальную техники наложения зажима в ходе лапароскопической и робот-ассистированной резекции почки и получили сопоставимые среднесрочные результаты применения техники селективного пережатия артерий почки и выполнения процедуры без ишемии [35].
Еще одну возможность для создания «сухого» операционного поля при органосохраняющем оперативном вмешательстве на почке без пережатия почечных сосудов предоставляет метод локального сдавления паренхимы почки в месте резекции. При открытых операциях это может быть пальцевое сдавление или же наложение зажима на паренхиму почки. В литературе описаны различные модификации зажимов, применяемых для селективного пережатия почечной паренхимы как при открытых (Reniclamp, DeBakey), так и при лапароскопических (Simon, Aesculap) и роботических (Семенова – Мосояна, Аль-Шукри – Мосояна и Короста – Мосояна) операциях [13, 36–39]. Показаниями для компрессии паренхимы во время резекции почки являются небольшие (до 3 см) опухоли верхнего или нижнего полюса в стадии Т 1 или бóльшие опухоли, но расположенные экстраренально, а также высокий риск развития послеоперационной острой почечной недостаточности. Исследования показали, что резекция почки в условиях селективной ишемии с наложением зажима на паренхиму составляет альтернативу пережатию почечной ножки и позволяет избежать интраоперационного кровотечения. Недостаток метода заключается в возможности его полноценного использования только при резекциях полюсов почки.
К механическим инструментам интраоперационной компрессии паренхимы почки относятся также и гибкие конструкции. В 1995 г. I.S. Gill et al. предложили использовать специальный турникет, представляющий собой двойную петлю, которую надевают на паренхиму почки, обеспечивая компрессию и обескровливание полюса органа. О.Б. Лоран и др. (2013) предложили накладывать вокруг опухоли по всему ее диаметру, отступя около 1 см от ее края, превентивные швы, которые затем завязываются над паренхимой [40]. После наложения швов выполняют резекцию почки с опухолью в пределах намеченной окружности. После достижения гемостаза ложе опухоли ушивают, чаще всего с применением какой-либо прокладки. Наложенные ранее провизорные швы используют при ушивании паренхимы почки в области ложа опухоли. Эти швы захватывают в шов, предотвращая прорезывание нитей. Методика позволяет уменьшить интенсивность кровотечения во время выполнения резекции; снизить риск прорезывания тканей при ушивании ложа опухоли; уменьшить длительность операции во время гемостаза; снизить вероятность пережатия почечной артерии [40]. При полярном расположении опухолей для компрессии паренхимы почки также может быть использована эндопетля Endoloop [41].
Для улучшения отдаленных функциональных результатов в ходе резекции почки можно сочетать различные методики. Например, некоторые авторы предлагают выполнять селективную микродиссекцию и пережатие артерии, питающей опухоль, в сочетании с фармакологической гипотонией [42]. А.К. Носов и др. (2016) произвели лапароскопическую резекцию почки в условиях нулевой ишемии и без наложения гемостатического шва 70 пациентам с положительными послеоперационными результатами: объем функционирующей паренхимы резецированной почки уменьшился лишь на объем удаленной опухоли [43]. По мнению авторов, для профилактики кровотечения и герметизации чашечно-лоханочного комплекса достаточно только электрогемостаза с дополнением местными клеевыми композициями [43].
КОНТРОЛЬ ЗА КРАЕМ РЕЗЕКЦИИ
Радикальность удаления опухоли почки при органосохраняющей операции определяется отсутствием положительного края в зоне резекции. Контроль за краем зоны резекции, с одной стороны, обеспечивает длительное безрецидивное течение болезни, а с другой — позволяет максимально сохранить неповрежденную онкологическим процессом паренхиму и, соответственно, почечную функцию. Для онкологического контроля применяют экспресс-биопсию из резецируемого участка ложа удаленной опухоли. Однако данный критерий оценки нельзя назвать точным, так как иногда нет возможности четко визуализировать опухолевую ткань в крае резекции, то есть материал для биопсии из различных участков области резекции берут не прицельно, а случайным методом. Как следствие, существует вероятность ложноотрицательного результата. Кроме того, морфологическое исследование занимает много времени, что увеличивает период ишемии и может привести к серьезному нарушению почечной функции [44]. Применение УЗИ интраоперационно, в том числе с маркировкой края резекции соноконтрастными иглами, позволяет более точно определить границы опухоли. Это дает возможность максимально сохранить здоровую паренхиму почки, не влияя на количество ранних осложнений и на специфическую и безрецидивную выживаемость. Благодаря данному варианту контроля края резекции были расширены показания к органосохраняющему лечению больных почечно-клеточным раком с опухолями размером более 7 см, а также с опухолями «неудобных» локализаций [45].
К современным методам контроля за краем резекции относится также флуоресцентная диагностика (первичная и вторичная) злокачественных новообразований. Метод основан на применении фотосенсибилизаторов (разнообразных производных порфирина и родственных макроциклов), которые при воздействии на них светом определенной длины волны переходят в возбужденное состояние и инициируют физико-химические процессы, сопровождающиеся люминесценцией и деструкцией опухоли. Аутофлуоресцентная диагностика (первичная) подразумевает определение различий в интенсивности и спектральном составе собственной флуоресценции здоровой и опухолевой ткани без применения фотосенсибилизаторов, так как ткани с повышенной пролиферативной способностью (неопластическая, эмбриональная и регенеративная) больше накапливают порфирины, соответственно, интенсивность их свечения будет больше. Вторичная флуоресцентная диагностика состоит в применении фотосенсибилизаторов, тропных к раковым клеткам, с возможностью их обнаружения по характерной флуоресценции экзогенных или эндогенных флуорохромов. Яркая флуоресценция флуорохромов, избирательно накапливающихся в ткани злокачественного новообразования, позволяет отличать объекты, достигающие размеров долей миллиметра. Флуоресцентная диагностика является неинвазивной и не воздействует на динамику различных биологических процессов в тканях. Вследствие моментальной обработки данных оптического анализа можно быстро скорректировать объем резекции в соответствии с полученной информацией, оценить хирургическое ложе после операции, а в случае выявления остаточной опухоли — выполнить срочную биопсию из конкретного участка. Метод позволяет выявить биохимические изменения тканей при трансформации нормальных клеток в диспластические и злокачественные (которые происходят раньше структурных перестроек), микроочаги новообразований и микрометастазы (в том числе множественные), невидимые при обычном освещении. Исследования показывают, что флуоресцентная диагностика представляет высокоэффективный метод оценки радикальности оперативного вмешательства, использование которого снижает риск местного рецидива заболевания и повышает продолжительность безрецидивного течения [46, 47].
Важным этапом подготовки к органосохраняющему оперативному вмешательству является предоперационное виртуальное планирование, которое дает возможность прогнозировать особенности операции, ее трудные и опасные этапы, предвидеть возможные осложнения. Технология дополненной реальности для интраоперационной навигации на основе предоперационного 3D-моделирования зоны хирургического интереса путем совмещения компьютерной модели и изображения реального органа во время видеоэндоскопической операции позволяет получить важную информацию о пространственной структуре органа, локализации патологического процесса, выбрать сегментарный сосуд для осуществления тепловой ишемии [48].
ВЫВОД
В результате выполнения органосохраняющей операции на почке удается улучшить функциональные результаты, сократить число пациентов с терминальной стадией хронической болезни почек и связанных с ней сердечно-сосудистых осложнений. Это особенно важно для пациентов с анатомически или функционально единственной почкой, так как в значительной мере может повысить качество их жизни. В настоящее время существует необходимость развития прецизионной хирургии, а также дальнейшего совершенствования средств противоишемической защиты почки, направленной на сохранение максимального объема функционирующей почечной паренхимы.
Ишемическая нефропатия ( Ишемическая болезнь почек )
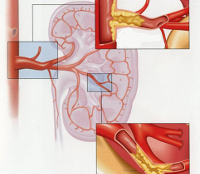
Ишемическая нефропатия – это патологическое снижение активности выделительной системы по причине нарушения кровоснабжения почек. Симптомы патологии зависят от ее формы и варьируются от вялотекущего нарастания признаков ХПН до острой и быстропрогрессирующей почечной недостаточности. Диагностика основывается на данных лабораторных анализов мочи и крови, ультразвуковых и рентгеноконтрастных исследований почек и их сосудистого русла, функциональных почечных проб. Лечение зависит от причин, провоцирующих патологию, и включает в себя использование гиполипидемических средств, антиагрегантов, гемодиализа и хирургическую реваскуляризацию почек.
Общие сведения
Ишемическая нефропатия или ишемическая болезнь почек является достаточно распространенным состоянием, особенно среди лиц пожилого и старческого возраста. Особой формой патологии выступает нефропатия ишемического типа у новорожденных, которую большинство специалистов выделяет в отдельную нозологическую единицу.
В большинстве случаев нефропатия возникает у лиц, страдающих ожирением, сахарным диабетом, атеросклерозом и другими разновидностями метаболических нарушений. Имеются указания на наличие генетической предрасположенности к развитию заболевания – оно чаще диагностируется у пациентов с определенными вариантами гена ангиотензин-превращающего фермента (АПФ). Также нефропатия выступает главной причиной терминальной хронической почечной недостаточности и вносит заметный вклад в общую картину смертности пожилых людей в развитых странах.
Причины
Характерной чертой ишемической нефропатии является ее тесная ассоциация со многими другими заболеваниями, затрагивающими сердечно-сосудистую систему, процессы метаболизма, железы внутренней секреции. В то же время, некоторые урологи считают истинной ишемической нефропатией только те формы, которые обусловлены первичным поражением почечных сосудов, тогда как другие причины окклюзии артерий приводят хоть и к похожим, но несколько иным патологическим процессам. Научная дискуссия относительно причин заболевания продолжается, на сегодняшний день большинством врачей-нефрологов признается наличие следующих этиологических факторов:
У новорожденных ишемическое поражение почек возникает по причине обезвоживания, перегрева, гиповолемии. Это вызывает нейрогенный спазм почечных артерий с резким ограничением поступления крови через них. При некоторых экстремальных ситуациях подобный процесс может наблюдаться и у взрослых людей, приводя к молниеносным формам ишемической нефропатии.
Патогенез
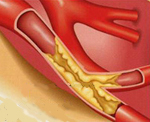
Часто причиной ишемической нефропатии выступают атеросклеротические изменения в почечных сосудах, обусловленные отложением холестерина и липидов на стенках артерий и артериол. У определенной доли больных поражение почек обусловлено воспалительной реакцией, носящей иногда аутоиммунный характер. Все это приводит к уменьшению ширины просвета сосудов и тем самым затрудняет поступление крови к тканям почки.
Недостаточное количество кислорода и питательных веществ приводит к постепенной дистрофии клеток нефронов, особенно эпителия канальцев, которые затем подвергаются аутолизу и некрозу. Гибель нефрона сопровождается разрастанием соединительной ткани, менее требовательной к объему поступаемого с кровью кислорода.Снижение объема кровотока через почки приводит к замедлению фильтрации и очистки крови от продуктов обмена веществ. Это явление еще больше усугубляется гибелью и снижением количества активных нефронов и отражается на функционировании всего организма.
Гипоперфузия юкстагломерулярного аппарата ведет к повышенному образованию ангиотензина 2 и развитию вазоренальной гипертензии, что ускоряет процессы образования атеросклеротических бляшек. Сочетание этих патогенетических процессов и приводит к сложной и разнообразной картине ишемической болезни почек. На терминальных стадиях заболевания из-за резкого снижения количества нефронов и прогрессирования сосудистых нарушений возникает ХПН, часто носящая терминальный характер.
Классификация
В современной урологии выделяют несколько основных клинических форм ишемической нефропатии. Они различаются характером и скоростью нарастания патологических проявлений и имеют разную этиологию. Это оказывает влияние как на подходы к лечению нефропатических состояний, так и на дальнейший прогноз жизни больного. Также они могут рассматриваться как различные этапы прогрессирования одного патологического процесса. Основными вариантами ишемического поражения почек являются:
Некоторые специалисты выделяют в качестве истинной формы патологии только одну разновидность (торпидную), полагая, что остальные следует дифференцировать от нее или признать ее осложнениями. Возражение такой точке зрения обусловлено тем, что различные клинические типы ишемической болезни отличаются не только проявлениями, но и своей этиологией.
Симптомы ишемической нефропатии
Особенностью заболевания является длительный период бессимптомного течения и крайне медленное развитие. Первые жалобы и характерная симптоматика торпидного варианта патологии возникают уже при выраженном снижении функциональной активности почек. Больные жалуются на уменьшение объема диуреза (олигурия), частые ночные позывы (никтурия), отеки конечностей и тканей лица. Возможны ухудшения общего состояния – слабость, снижение работоспособности, быстрая утомляемость.
Со временем перечисленные проявления нарастают и переходят в ХПН – помимо отеков и нарушения образования мочи, возникает неприятный (аммиачный) запах изо рта, раздражение кожи. Терминальная ХПН также характеризуется изменениями в психо-эмоциональном состоянии больного – он становится раздражительным, возникают перепады настроения, возможны суицидальные наклонности. Нарушения затрагивают и другие системы организма: со стороны желудочно-кишечного тракта отмечаются частые диареи, тошнота, нарушения аппетита.
Смещение водно-ионного равновесия приводит к гиперкалиемии, проявляющейся нарушениями мышечной системы и аномалиями сердечного ритма. На финальных этапах развития ишемической нефропатии почки практически утрачивают свою функцию – развивается анурия с образованием менее 50 миллилитров мочи в сутки. Без использования гемодиализа больной на этом этапе торпидной формы патологии может умереть от уремии.
Другие формы заболевания характеризуют значительно более стремительным течением. Так, быстропрогрессирующая ишемическая нефропатия проявляется болями в пояснице, резким уменьшением диуреза и развитием анурии с отеками и электролитными нарушениями, характерными для ОПН. Нередко ей предшествуют многочисленные эпизоды инфарктов почек, обусловленных эмболизацией их сосудов холестериновыми фрагментами. Острая форма характеризуется еще более быстрым возникновением ОПН, а также тяжелым состоянием больного вплоть до комы или шока. И в том, и в другом случае необходимы срочные реанимационные мероприятия.
Осложнения
Закономерным итогом ишемической нефропатии при отсутствии лечения выступает хроническая почечная недостаточность, которая и является наиболее частым осложнением. Острую недостаточность почек, характерную для быстропрогрессирующих форм заболевания, чаще рассматривают как часть симптомокомплекса патологии. Среди иных осложнений выделяют инфаркт почки, представляющий собой крайний вариант ишемии тканей органа – его возникновению во многом способствует атеросклеротическое поражение сосудов. Косвенными последствиями состояния считают нарушения, обусловленные высоким уровнем артериального давления – вазоренальная гипертензия может провоцировать патологии сердца, сосудов, инсульты и инфаркты миокарда.
Диагностика
Медленно прогрессирующие варианты ишемической нефропатии на первоначальных этапах развития диагностировать достаточно сложно. Они не проявляются субъективными симптомами и очень слабо отражаются на результатах инструментальных и лабораторных исследований. По этой причине их определяют случайно при выполнении медицинских исследований по иному поводу. Клинические проявления обнаруживаются на этапе выраженного снижения функциональности выделительной системы.
Острые формы патологии характеризуются более явной симптоматикой, однако и в этом случае их не всегда просто дифференцировать от других типов поражения почек (например, некоторых форм гломерулонефрита). Диагностические мероприятия при нефропатии включают в себя следующие процедуры и методы:
Дифференциальную диагностику следует производить с другими формами нефропатии – например, гипертензивной, в результате гломеруло- или пиелонефрита и ряда других патологий. Ключевым признаком, отличающим ишемию почек от прочих заболеваний, является нарушение кровоснабжения, не соответствующее («опережающее») степени снижения их функциональной активности.
Лечение ишемической нефропатии
Терапевтические назначения сводятся к поддерживающему лечению и устранению патологий, способствующих гипоперфузии почек. В случае острых и быстропрогрессирующих форм может потребоваться интенсивная терапия для сохранения жизни больного. В отдельных ситуациях прибегают к хирургическим методам лечения, направленным на устранение основного звена поражения почек – пониженной перфузии. К ним относят стентирование почечных артерий с целью устранения стеноза и эндартерэктомию для удаления атеросклеротических бляшек. Консервативное же лечение производится с применением следующих групп препаратов:
Важную роль в замедлении ишемических процессов в почках играет правильное соблюдение водного режима, отказ от вредных привычек (в особенности от употребления алкоголя), приема определенных лекарственных средств (нефротоксических антибиотиков, некоторых НПВС). Следует также ограничивать потребление соли, придерживаться диеты с пониженным содержанием липидов в рационе. Длительность консервативной терапии и вспомогательных мероприятий довольно велика, часто они назначаются пожизненно. При резком снижении функции почек применяют гемодиализ.
Прогноз и профилактика
Прогноз ишемической нефропатии зависит от того, на каком этапе развития было выявлено это патологическое состояние. В случае раннего обнаружения заболевания, соблюдения назначенных врачом рекомендаций прогноз относительно благоприятный. Прогрессирование патологии замедляется, и качество жизни больного практически не изменяется. Ухудшает прогноз наличие ХПН, что указывает на декомпенсацию работы выделительной системы и требует регулярного применения гемодиализа.
Профилактика нефропатии тесно связана с предотвращением развития атеросклероза, включает правильное и сбалансированное питание, уменьшение количества животных жиров в рационе (особенно пожилых больных). При наличии гиперлипидемии следует начинать превентивное назначение гиполипидемических средств для предотвращения атеросклероза и связанных с ним патологий.