Паранеопластический синдром — прогностическая значимость

В статье представлены возможные особенности клинического течения паранеопластического синдрома, а также его сходства с другими заболеваниями, что при современной диагностической доступности позволит выявить опухоль задолго до ее клинического проявления.
The article presents the possible features of the clinical course of paraneoplastic syndrome and its similarity to other diseases, which, considering modern diagnostic accessibility, will reveal the tumor long before its clinical manifestation.
Повышенный интерес к сфере онкологии обусловлен быстрым ростом уровня заболеваемости и поздней диагностикой, которая, к сожалению, приводит к высоким показателям летальности.
В 2017 г. в России впервые диагностировано 617 177 злокачественных новообразований. В сравнении с 2016 г. прирост составил 3,0%. В общей структуре смертности от злокачественных новообразований летальность в 2017 г. составила 15,9% (290,7 тысячи больных) [4].
Под паранеопластическим синдромом следует понимать клинические проявления отдаленного эффекта опухолевого процесса, что в свою очередь является результатом химических, биологических, иммунологических и гормональных повреждений опухолью [5].
Паранеопластический синдром входит в группу определенных синдромов, детерминированных особенностью воздействия опухолевых клеток на различные органы и системы организма, включая иммунитет и метаболические процессы. Развивающиеся патологические процессы проявляются разнообразными симптомами, не связанными с самой злокачественной опухолью, в месте ее локализации и очагах метастазирования [2]. По этим причинам на протяжении длительного времени больные со злокачественными опухолями проходят обследование и лечение у врачей различных специальностей, не подозревая о коварности и драматичности течения паранеопластического синдрома [3].
По современным опубликованным литературным данным, паранеопластический синдром чаще развивается в среднем и пожилом возрасте. Паранеопластические синдромы, по разным данным авторов, диагностируются у 60% больных злокачественными опухолями [1].
Данный синдром регистрируется в 10–18,5% случаев при раке толстой кишки, мелкоклеточном раке легкого, раке молочной железы и яичников, злокачественных лимфомах [5].
Важным в диагностическом поиске является тот факт, что паранеопластический синдром может формироваться вместе с развитием опухоли и, что более значимо, задолго до ее клинического дебюта. После проведения необходимого объема лечения злокачественной опухоли паранеопластический синдром может купироваться и вновь появиться при возможных рецидивах опухоли [1].
Исходя из патогенеза, паранеопластический синдром может быть представлен разнообразными механизмами:
Возникновение паранеопластического синдрома зачастую является перерождением стероидов опухолевыми клетками в биологически активные формы [2].
Распространение опухоли или исход метастатического поражения могут быть диагностированы как паранеопластический синдром. Например, если рассматривать лихорадку или анорексию, паранеопластический синдром, по мнению большого круга специалистов, возникает приблизительно у 50% всех онкологических больных [2].
Довольно часто возникновение и симптоматика паранеопластического синдрома при различных видах опухолевых заболеваний указывают на их нозологическую специфичность [2]. Например, редко встречающаяся разновидность паранеопластического синдрома — неспецифический аортоартериит, развивается при раке ободочной кишки [5].
По мнению многих авторов, основная роль в патогенезе паранеопластического синдрома отводится процессам в иммунной системе. Основу иммунного механизма представляет ответная реакция на выработку опухолью биологически активных веществ с развитием иммунных и аутоиммунных комплексов. Особую роль занимает формирование патологических активных эктопических рецепторов в ткани опухоли, при этом действие физиологических гормонов блокируется [5].
В большинстве случаев при B-клеточных лимфопролиферативных заболеваниях (болезни Кастлемена, макроглобулинемии Вальденстрема, тимоме, веретеноклеточном раке) развивается тяжелый патологический процесс — паранеопластическая пузырчатка. У пациентов наблюдается лихенизация кожных покровов, стоматит. При этом выявляются антитела к лектину, антигену буллезной пузырчатки I, десмосомальным элементам [2].
Синдром Шегрена также может быть отнесен к паранеопластическому синдрому, в случае выявления моноклональных антител 17–109. Наличие синдрома Шегрена может провоцировать развитие лимфом различной локализации. Синдром Шегрена может развиться на фоне овсяноклеточного рака легких, рака шейки матки, бронхолегочной карциномы [5].
Лимфогранулематоз (лимфома Ходжкина) — злокачественная опухоль лимфоидной ткани, отличительной чертой которой является наличие в ее субстрате гигантских многоядерных клеток Рида–Штернберга. По данным исследований S. Shams’ili et al., лимфома Ходжкина была диагностирована у 16% больных с паранеопластической мозжечковой дегенерацией [9, 10].
Одним из классических проявлений паранеопластического синдрома является гипертрофическая остеоартропатия, характерная при опухолях легочной ткани [5].
В 1995 г. Д. Познер первым описал паранеопластический неврологический синдром, возникающий у больных со злокачественными опухолями и являющийся составной частью поражения центральной и периферической нервной системы, поражения скелетных мышц [6, 10]. В большинстве случаев у пациентов до развития клинических проявлений опухолевого процесса при обращении к неврологу могут быть выявлены неврологические расстройства [8]. Паранеопластический неврологический синдром наиболее часто проявляется: лимбическим энцефалитом, паранеопластическим энцефаломиелитом, подострой мозжечковой дегенерацией, миастеническим синдромом Ламберта–Итона, синдромом опсоклонус-миоклонус, паранеопластической ретинопатией [8].
Колоссальным достижением нейрорадиологии является открытие и применение в клинической практике антионконевральных антител. Хорошо стала известна тесная связь паранеопластического лимбического энцефалита с аутоантителами против антигенов нейронов [8].
При лимбическом энцефалите, энцефаломиелите, мозжечковой дегенерации, синдроме опсоклонус-миоклонус идет поражение на уровне мозга, черепно-мозговых нервов, сетчатки. Уровнем поражения при миастеническом синдроме Ламберта–Итона будут нервно-мышечные синапсы [7].
Паранеопластический лимбический энцефалит ассоциирован с анти-Ма2-антителами (или анти-Та-антителами) при тестикулярном раке и с анти-Нu-антителами при мелкоклеточном раке легкого [8].
При выявлении в сыворотке крови или ликворе у больных со злокачественными опухолями анти-Hu-антител клиническая симптоматика может сопровождаться эпилептическими припадками, нарушением краткосрочной памяти, расстройством психики по типу синдрома Вернике–Корсакова. Обнаружение анти-Ма2-антител в сыворотке крови или ликворе представляет клинику панических атак, обсессивно-компульсивных расстройств, нарушения краткосрочной памяти, стволовой симптоматики, диэнцефального синдрома, повышения дневной сонливости [8].
При первичном выявлении в сыворотке крови или ликворе у больных со злокачественными опухолями анти-Ма2- (или анти-Та-) и анти-Hu-антител следует провести магнитно-резонансную томографию (МРТ) головного мозга с тонкими Т2-взвешенными изображениями, так как на МРТ головного мозга в более чем 57% случаев определяется паранеопластический лимбический энцефалит, даже при отсутствии клинических проявлений, таких как полифагия, повышенная сонливость в дневное время, катаплексия, нарколепсия, гипокинезия, надъядерный паралич взора (в большинстве случаев вовлечены вертикальные движения глаз) [8].
Тимома является одним из часто встречающихся опухолевых образований средостения. Факторы, которые влияют на развитие тимом, изучены недостаточно. Существует теория воздействия вируса Эпштейна–Барр на развитие данного заболевания. У больных с тимомой, по данным исследований, которые проводились в США и Швеции, возрастал риск развития саркомы мягких тканей, неходжкинской лимфомы, рака простаты [10].
Синдром эктопической продукции адренокортикотропного гормона был впервые описан Д. Брауном в 1928 г. Следствием синдрома является организация адренокортикотропного гормона опухолевой тканью, что в свою очередь способствует развитию гиперкортицизма. В клиническую симптоматику гиперкортицизма входят лунообразное лицо, ожирение туловища, стрии на груди и животе, внутренней поверхности бедер, гиперсутизм, аменорея, депрессия, слабость. Дифференциальную диагностику гиперкортицизма (с обязательным включением в диагностический ряд злокачественной опухоли) следует проводить между болезнью Кушинга, повышенной секрецией кортиколиберина и заболеванием надпочечников [2].
Синдром Пархона (синдром неадекватной продукции антидиуретического гормона) у большого круга пациентов сопровождает мелкоклеточный рак легкого и в наименьшем количестве опухоли головы, шеи. Значительное понижение осмолярности плазмы при синдроме Пархона является результатом гипонатриемии при продолжающейся секреции антидиуретического гормона. Клиническими проявлениями при синдроме Пархона являются гипонатриемия и водная интоксикация. По мере развития клинической симптоматики у больных развивается поражение центральной нервной системы токсического характера, возникает спутанное сознание, развивается бред, появляются судороги, кома; возможен летальный исход. Приведенные клинические проявления необходимо учитывать у всех онкологических больных [2].
Опухоли неостровковых клеток являются частой причиной паранеопластического синдрома с гипогликемией. Причиной могут быть мезенхимные опухоли (мезотелиомы, саркомы) любой локализации. Патогенезом паранеопластического синдрома с гипогликемией может быть повышенная пролиферация рецепторов к инсулину, образование ингибиторов синтеза глюкозы печенью, повышенный метаболизм глюкозы [2].
Паранеопластический синдром при поражении клубочковой системы почек в большинстве случаев проявляется нефритическим синдромом (протеинурия, отеки, макрогематурия, артериальная гипертензия) или нефротическим синдромом (гипопротеинемия, отеки). Возможно бессимптомное течение, изменения возникают только в анализах мочи (латентный гломерулонефрит). К сожалению, паранеопластический синдром при поражении почек довольно часто диагностируется вместе с опухолевой патологией. При своевременном и правильно подобранном лечении опухоли нефротический синдром может быть полностью купирован. При критическом уровне потери белка обязательным является контроль за возможным развитием тромбоэмболии легочной артерии (ТЭЛА), тромбозов почечных вен [2].
При опухолевом процессе почки довольно часто поражаются метастатически или инфильтрируются. Инфильтративный характер поражения почек возникает зачастую при гемобластозах, особенно острых. Для лимфогранулематоза характерной особенностью является билатеральное поражение ткани почек [2].
Паранеопластический синдром, который сочетает в себе анорексию и кахексию, на сегодняшний день часто сопровождает большую часть опухолевых заболеваний любой локализации. Патогенетически кахексия развивается вследствие повышенной секреции фактора некроза опухоли α, интерферона-γ, ИЛ-6, ИЛ-1, трансформирующего фактора роста β. Клинические проявления паранеопластического синдрома обусловлены преобладанием вышеописанных факторов над противокахектическими факторами — ИЛ-4, ИЛ-10, ИЛ-13. Секреция в ткани опухоли веществ, которые приводят к изменению восприятия вкуса пищи и запаха, является причиной понижения чувства насыщения и удовольствия от принятой пищи. На сегодняшний день нет эффективных методов лечения, чтобы полностью купировать данные проявления [2].
Паранеопластические дерматозы составляют комплекс симптомов и заболеваний поражения кожи, развивающихся под воздействием злокачественных образований внутренних органов. Наибольшее клиническое значение среди паранеопластического кожного синдрома имеют акрокератоз Базекса, черный акантоз, паранеопластический пемфигус [1].
Акрокератоз Базекса чаще на несколько лет предшествует опухолевому процессу или возникает совместно с клинической симптоматикой злокачественного процесса [1].
Паранеопластический черный акантоз возникает уже в периоде метастазирования, что является неблагоприятными прогностическими данными. По данным различных исследований, после появления первых кожных изменений около 50% больных погибают в течение 9 месяцев, 75% больных — в течение 1,5 лет, 90% больных — в период до 2 лет [1]. Дифференциальную диагностику паранеопластического черного акантоза проводят с псевдоакантозом, который появляется при избыточной массе тела, и с доброкачественным черным акантозом, возникающим после рождения, в детстве или в период полового созревания [1].
Паранеопластический пемфигус появляется в любом периоде возникновения опухоли. После удаления опухоли дерматоз регрессирует и заново возникает при метастазировании [1].
Довольно часто паранеопластический синдром проявляется тромботическими осложнениями, такими как мигрирующий тромбофлебит, тромботической микроангиопатией, тромбоэмболией легочной артерии, небактериальным тромбоэндокардитом, парадоксальными кровотечениями [3]. Возможно паранеопластическое поражение сосудов по типу васкулита. Патогенез паранеопластического васкулита изучен недостаточно. Многие авторы являются сторонниками аутоиммунного механизма с образованием иммунных комплексов в сосудистой стенке разного калибра и дальнейшим формированием воспаления, некроза. Неиммунный механизм, по мнению других авторов, трактуется воспалением в сосудистой стенке и воздействием на эндотелий субстанций и медиаторов, продуцируемых опухолью [9, 10]. Время возникновения первой клинической симптоматики коагулопатии и верификации опухоли составляет в среднем от 2 до 5 лет [3].
Диагностика определенных видов паранеопластического синдрома дает возможность онкологу сориентироваться в наиболее правильном диагностическом поиске опухолевого процесса. На современном этапе с привлечением высоких технологий диагностики основательно доказано, что опухоль будет выявлена в 80% случаев [9].
В большинстве случаев паранеопластический синдром и клинически сходные заболевания имеют множество особенностей. Все это может способствовать определению и характеристике группы пациентов для тщательного и прицельного поиска онкологической патологии [4].
Сегодня злокачественные опухоли поражают различные органы. Многообразие онкологических патологий и обусловленная ими высокая летальность представляют серьезную задачу для проведения ранней диагностики. Современная диагностика паранеопластического синдрома позволит выявить опухоль на стадии доклинических проявлений.
Литература
ФГБОУ ВО КемГМУ Минздрава России, Кемерово
Чем отличается доброкачественная опухоль от злокачественной
В медицине понятие доброкачественности означает лёгкое течение болезни, хорошие результаты лечения и неопасность для жизни. Под злокачественным процессом подразумевают разрушительное течение, сложность терапии, высокий риск смертности.
Для опухолей такое разделение условно. Тем не менее пациентам и врачам крайне важно определить вид опухоли. От этого зависят тактика лечения и прогноз.
Характеристика доброкачественных и злокачественных опухолей
Существуют чёткие критерии:
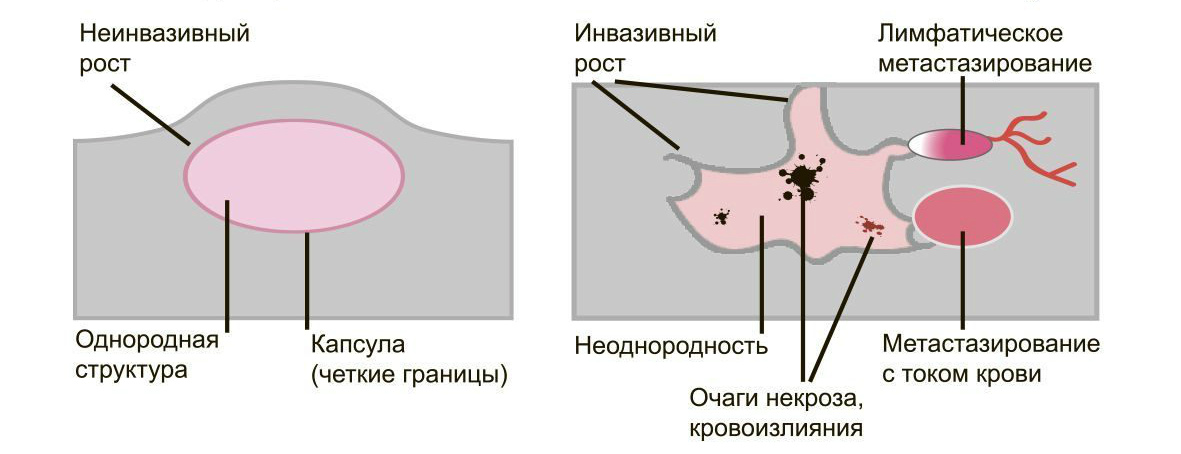
Доброкачественные опухоли чётко отграничены от здоровых тканей, часто имеют капсулу. Рак прорастает окружающие ткани, внедряется в сосуды, его контуры более аморфны.
Большинство доброкачественных опухолей могут расти годами, не проявляя симптомов. Карциномы растут быстро, нарушая функции органов и отравляя организм. Рост сопровождается утомляемостью, слабостью, потерей веса, болью.
Доброкачественные образования “сидят” на одном месте, постепенно растут и раздвигают здоровые ткани, подвижны при прощупывании. Раковые клетки слабо скреплены друг с другом, легко отделяются и разносятся лимфой и кровью по организму. Они оседают в лимфоузлах, костях, внутренних органах, образуя новые опухолевые очаги — метастазы. При пальпации узел спаян с тканями и не сдвигается.
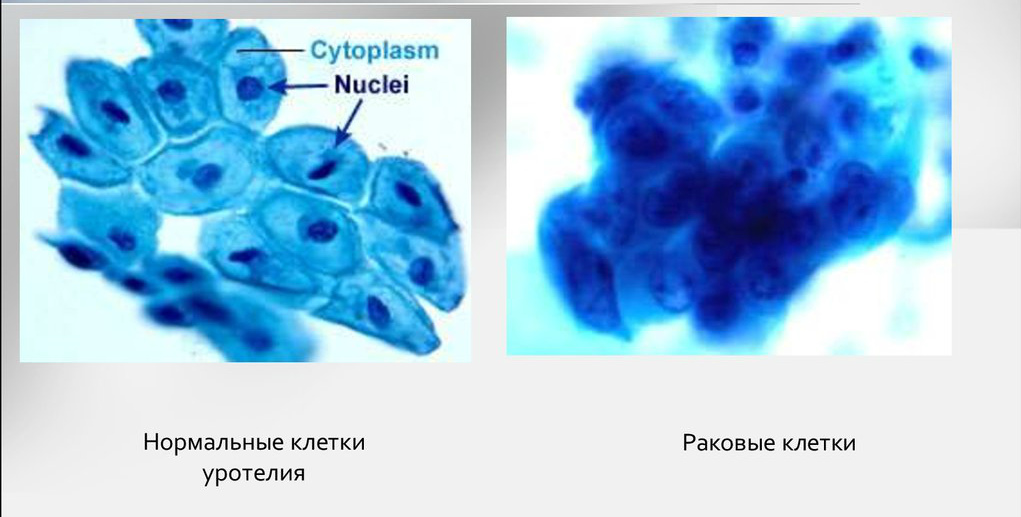
Много информации даёт биопсия. Исследование показывает, что доброкачественные клетки похожи на здоровые, их структура более чёткая. Структура злокачественных клеток сильно изменена из-за выраженных мутаций. Чем меньше клетки напоминают ткань, из которой выросли, тем хуже прогноз для лечения и жизни.
Доброкачественную опухоль, такую как аденома простаты, можно удалить и добиться полного излечения. Если возникнет рецидив, он будет на том же месте, где нашли первичный очаг. Злокачественные образования трудно удалить полностью. Даже одна оставшаяся клетка даст новую опухоль либо на старом месте, либо там, куда она попала по сосудам. Выживаемость больных существенно ниже.
Общие свойства доброкачественных и злокачественных опухолей
Есть моменты, объединяющие оба вида новообразований:
Тяжесть симптомов зависит не только от степени сдавления тканей опухолью, но и от неспособности новообразования выполнять функцию здоровых клеток.
Виды опухолей
Различия не всегда очевидны. Нужна тщательная диагностика для поиска атипичных клеток.
Может ли доброкачественная опухоль стать злокачественной
Любая опухоль способна к малигнизации. Миомы, липомы, фибромы редко переходят в рак. Кисты — крайне редко. Невусы, аденомы, полипы в желудке или кишечнике — очень часто. Многое зависит от условий, в которых находится опухоль, питания, экологии, уровня стресса, гормональных сбоев, наличия предраковых болезней.
В Клинике урологии имени Р. М. Фронштейна доступна современная диагностика опухолей, разработаны эффективные методики лечения. Обращайтесь на консультацию и наши специалисты вам помогут.
Злокачественное новообразование: причины появления, виды и стадии развития
Существует более двухсот разновидностей онкологических заболеваний, которые могут развиваться в любой области человеческого организма. Болезнь провоцируется неконтролируемым появлением атипичных мутировавших клеток, что со временем вызывает нарушение работы отдельных органов и систем организма, а также ухудшает общее самочувствие человека.
Проявление симптомов зависит от того, где расположено злокачественное новообразование и какова стадия его развития. Основными симптомами становятся: общая слабость, ухудшение аппетита, резкая потеря веса, субфебрильная температура, чрезмерная потливость, озноб.
Лечение и шансы на полное выздоровление зависят от стадии злокачественных новообразований, их вида и реакции на различные препараты. Чтобы предотвратить появление онкологии или быстро ее обнаружить, важно знать причины болезни и первые симптомы. Если есть подозрения на злокачественное новообразование, рекомендуется обратиться за консультацией опытного врача-онколога. Наилучшую помощь оказывают в иностранных клиниках.
В Турции пациентам обеспечивается максимально эффективное лечение, быструю и точную диагностику, демократичные цены на услуги.
Причины злокачественных новообразований
Ученые определили ряд причин злокачественных новообразований, способных спровоцировать развитие рака. Для удобства их принято разделять на две большие группы: эндогенные и экзогенные.
Рассмотрим подробнее каждую из них.
Эндогенные причины злокачественных новообразований:
Экзогенные причины злокачественных новообразований:
Виды злокачественных новообразований
Злокачественное образование по строению в первую очередь зависит от тканей, в которых оно сформировалось. По этому признаку различают следующие виды злокачественных новообразований:
По принципу деления злокачественных клеток выделяют гистологические, клинические и морфологические виды опухолей.
По сложности строения бывают простые (образование из одного типа ткани) или сложные виды злокачественных новообразований. Также рак различают по органу или системе, в которых он сформировался: костей, кишечника, яичников, кожи, желудка, молочных желез, предстательной железы, шейки матки, легких и т.п.
Виды злокачественных новообразований по строению клеток, на основе которых они развиваются:
Стадии злокачественных новообразований
По степени агрессивности болезни и ее распространению по организму, различают 4 стадии злокачественных новообразований.
Рассмотрим признаки каждой из них:
Стадии злокачественных новообразований определяются после тщательного обследования и консультации врача-онколога.
Саркомы мягких тканей – редкое заболевание, которое составляет 1% от всех случаев рака в мире. Они характеризуются высоким риском рецидива – по разным данным от 25 до 60%. Чаще всего причиной гибели пациентов с этим диагнозом становится генерализация опухолевого процесса, то есть его распространение и метастазирование.
Главным методом лечения сарком мягких тканей остается хирургическое вмешательство. В то же время по данным международных рандомизированных исследований лучевая терапия снижает частоту возникновения рецидивов.
На данный момент в клинической практике применяются два варианта лучевой терапии для таких пациентов – до операции и после. Для врачей по всему миру остается открытым вопрос планирования облучения – в каком случае терапию лучше провести до хирургического вмешательства, а в каком – после? Оба метода имеют свои преимущества и недостатки.
Так, предоперационная терапия снижает биологическую агрессивность опухоли и ее размеры. Предоперационное облучение также характеризуется высокой точностью доставки дозы и может способствовать запуску естественного иммунного ответа организма человека. Главный недостаток такого метода – значительное увеличение послеоперационных осложнений, которые связаны с облучением здоровых тканей вокруг опухоли. Послеоперационная лучевая терапия, которая направлена на опухолевое ложе и окружающие ткани, снижает риски рецидива и метастазирования.
Сочетание этих двух видов облучения позволило бы использовать преимущества обоих методов. Однако, если выполнять такое лечение в стандартных объемах, указанных в клинических рекомендациях, пациент получит непереносимо высокую лучевую нагрузку.
— Мы встаём перед выбором – либо проводить предоперационную лучевую терапию, рассчитывая на её иммунологические феномены, и на то, что она уменьшит размеры опухоли; либо проводить послеоперационную лучевую терапию, которая защитит от рецидивов.
Наш научный коллектив решил изучить возможность комбинированного подхода, чтобы пациент получал одновременно плюсы и предоперационного облучения и послеоперационной лучевой терапии, — разъяснил Сергей Николаевич Новиков, д.м.н., заведующий отделением радиотерапии, заведующий научным отделением радиационной онкологии и ядерной медицины НМИЦ онкологии им. Н.Н. Петрова, руководитель исследования.
В 2017 году группа ученых отделения радиотерапии и хирургического отделения опухолей костей, мягких тканей и кожи Центра онкологии им. Н.Н. Петрова начала работать над научным исследованием, целью которого было проанализировать целесообразность и безопасность комбинации пред- и послеоперационной лучевой терапии у пациентов с саркомами мягких тканей конечностей.
Чтобы реализовать научный эксперимент, ученые разработали протокол лечения, рассчитали допустимые дозы облучения и выбрали методы облучения пациентов. Опираясь на опыт коллег, в качестве предоперационного лечения врачи выбрали стереотаксическую абляционную лучевую терапию, которая должна проводиться исключительно в пределах опухолевых тканей и места операции. Этот метод позволяет снизить риск послеоперационных осложнений на здоровых тканях, сделать более четкими границы опухоли, что важно во время проведения операции, запустить иммунный ответ организма и снизить риск метастазирования.
Лечение по разработанному протоколу в рамках исследования прошли 14 пациентов с диагнозом саркома мягких тканей. Они получили предоперационную стереотаксическую лучевую терапию, хирургическую операцию, а также стандартное послеоперационное облучение. Каждый больной наблюдался в послеоперационном периоде от 13 до 30 месяцев. В это время лишь в двух случаях (14%) были зафиксированы тяжелые осложнения, при этом ни у кого из пациентов не было зафиксировано рецидива заболевания. В 2020 году ученые провели промежуточный анализ результатов научной работы.
— Мы достигли главной цели исследования – убедились в технической возможности проведения предоперационной и послеоперационной лучевой терапии, а также доказали, что данный подход не приведёт к увеличению осложнений и он безопасен для больных, — разъяснил Сергей Николаевич Новиков. – В какой-то степени это новый подход, который позволяет существенно расширить список задач, которые мы сможем решать с помощью лучевой терапии. Мы рассматриваем его как модель, которую можно будет внедрить и при лечении других онкологических заболеваний, например, рака легкого.
Промежуточные результаты первой в мире научной работы о возможности и безопасности сочетания пред- и послеоперационной лучевой терапии опубликованы в мае 2021 года в журнале Radiotherapy and Oncology.
Ознакомиться с текстом научной статьи можно зде сь
Работа над новым протоколом продолжается.