Интратекальное пространство что это
Введение лекарственных веществ непосредственно в ликворную систему (интратекально, эндолюмбально) является очень ответственной процедурой. Такой путь введения лекарственных препаратов (преимущественно этиотропных) в субарахноидальное пространство наиболее часто показан при инфекционных поражениях мозговых оболочек и вещества головного мозга (менингит, менингоэнцефалит).
При крайне тяжелых вариантах течения бактериальных нейроинфекций интратекальное введение антибактериальных препаратов применяется в сочетании с основными методами их введения — внутримышечным, внутривенным и внутриартериальным.
Показаниями для интратекального введения антибиотиков являются:
— ациклично протекающие (затяжные, вяло- и волнообразно текущие) тяжелые и крайне тяжелые формы гнойных менингитов и менингоэнцефалитов;
— угроза развития или наличие вентрикулита;
— угроза формирования абсцесса головного мозга на фоне основного заболевания и(или) организации гноя на поверхности головного мозга;
— тромбоэмболические поражения сосудов и синусов головного мозга на фоне сепсиса;
— развитие гнойного менингита и(или) менингоэнцефалита как осложнения нейрохирургического заболевания, в том числе в послеоперационном периоде.
При выборе этиотропного препарата, предполагаемого к интратекальному введению, определении его разовых, курсовых доз и длительности курса необходимо помнить о том, что интратекальное введение антибиотика является дополнением к основной этиотропнои терапии, а также учитывать следующие факторы:
— предрасположенность больного к аллергии;
— степень выраженности отека головного мозга (при выраженном отеке введение препаратов в концевую цистерну малоэффективно);
— спектр выделенных штаммов патогенных микроорганизмов, их чувствительность к антибиотикам;
— фармакокинетические и фармакодинамические особенности конкретных препаратов и их сочетаемость (синергизм) с препаратами, в том числе антибактериальными, получаемыми больным в виде базисной терапии;
— возможность появления токсических эффектов при интратекальном введении препаратов, особенно при наличии у больного тяжелого сопутствующего патологического процесса (поражение почек, печени и т. д.);
— проведение больному ликворосорбционной терапии и ряда других экстракорпоральных методов лечения.
Прямых противопоказаний к интратекальному введению антибиотиков нет, однако именно факторы непосредственного миелотоксического и других прямых токсических воздействий на ткани ЦНС большинства антибиотиков и противобактериальных химиопрепаратов значительно сузили спектр используемых для эндолюмбального введения антибиотиков.
Второй, не менее существенной, проблемой является тенденция к изменению резистентности основных нейротропных этиопатогенов к все еще широко используемым препаратам пенициллинового ряда и аминогликозидов первых поколений. Общепризнанным является факт, что не чувствительны in vitro и клинически к этим препаратам выделенные от больных практически 90% штаммов стафилококков, до 40% штаммов пневмококков, до 15% штаммов менингококков (в странах Азии, США, Канаде).
Кроме того, наблюдается повсеместная тенденция к росту удельного веса в этиологии бактериальных нейроинфекций листерий, гемофильной палочки, энтеробактерий, традиционно резистентных к названным препаратам.
Интратекальное пространство что это
ФГБОУ ВО «Тюменский государственный медицинский университет», Тюмень, Россия
ГБОУ ВПО «Тюменская государственная медицинская академия», Тюмень
Государственный медицинский университет, Семей, Казахстан
ГБОУ ВПО «Тюменский государственный медицинский университет», Тюмень, Россия, Государственный медицинский университет, Семей, Казахстан
ГБОУ ВПО «Тюменский государственный медицинский университет», Тюмень, Россия
Интратекальное введение лекарственных препаратов
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(10): 89-92
Лебедев И. А., Левитина Е. В., Акимжанова А. К., Рахманина О. А., Шторк Т. Э. Интратекальное введение лекарственных препаратов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(10):89-92.
Lebedev I A, Levitina E V, Akimzhanova A K, Rakhmanina O A, Shtork T E. Intrathecal administration of drugs. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2016;116(10):89-92.
https://doi.org/10.17116/jnevro201611610189-92
ФГБОУ ВО «Тюменский государственный медицинский университет», Тюмень, Россия
Обобщены сведения о введении лекарственных средств в цереброспинальную жидкость. Освещены показания и противопоказания к введению фармацевтических препаратов в ликворное пространство. Приведены основные группы фармакологических препаратов, применяемых для эндолюмбального введения и показания для их назначения, отмечены преимущества и недостатки такого метода лечения. Описана методика введения антибиотиков при бактериальном и грибковом поражении ЦНС. Подчеркивается необходимость оценки интракраниального давления перед выполнением процедуры пункции концевой цистерны и исключения блокады ликворопроводящих путей. Отражены основные сведения об интратекальном введении противоопухолевых и цитостатических препаратов при первичных и метастатических поражениях головного мозга, а также эффективности введения кислородно-озоновой смеси в лечении пациентов с черепно-мозговой травмой. Отмечены результаты исследования, показавшие статистически значимое уменьшение выраженности неврологического дефицита при введении церебролизина в эндолюмбальное пространство в 1-е сутки после развития инфаркта мозга. Приведена информация о возможных осложнениях описываемого способа доставки лекарственных средств, методы борьбы с ними и способы их предотвращения.
ФГБОУ ВО «Тюменский государственный медицинский университет», Тюмень, Россия
ГБОУ ВПО «Тюменская государственная медицинская академия», Тюмень
Государственный медицинский университет, Семей, Казахстан
ГБОУ ВПО «Тюменский государственный медицинский университет», Тюмень, Россия, Государственный медицинский университет, Семей, Казахстан
ГБОУ ВПО «Тюменский государственный медицинский университет», Тюмень, Россия
Исторические сведения о первом интратекальном введении фармакологических препаратов с лечебной целью отсутствуют. Имеются данные о том, что люмбальную пункцию (ЛП) впервые выполнил и описал Г. Квинке в 1890 г. Он же первым исследовал цереброспинальную жидкость (ЦСЖ), определил состав, удельный вес, изучил и описал ее характеристики при гнойном менингите. Известный нейрохирург У. Денди, обучавшийся данной специальности у Х. Кушинга, разработал и использовал на практике такие диагностические методы, как пневмовентрикулография (1918 г.) и пневмоэнцефалография с эндолюмбальным введением воздуха (1919 г.). Спинальная анестезия была впервые выполнена 16 августа 1898 г. А. Биром при резекции пораженного туберкулезом голеностопного сустава. А. Бир и его ученик А. Гильдебрандт лично на себе испытали действие нового метода анестезии [1—6].
Термин «интратекальное введение» («эндолюмбальное введение») обозначает доставку вещества в подоболочечное пространство (от лат. teka — оболочка), т. е. субарахноидально после прокола твердой мозговой оболочки. В нейрохирургической практике при выполнении лекарственных блокад анестетик и кортикостероидные препараты могут вводиться в эпидуральное пространство, т. е. между твердой оболочкой спинного мозга и желтой связкой.
Основными преимуществами интратекального введения являются возможность создания максимальных концентраций лекарственного вещества в мозговой ткани и ЦСЖ, а также введение препаратов, не проникающих через гематоэнцефалический барьер. В ряде случаев введение лекарственного средства в концевую цистерну позволяет уменьшить его дозу и снизить системное токсическое воздействие. К недостаткам метода можно отнести относительно сложную методику введения фармакологических средств, риск перепадов интракраниального давления и невозможность введения эмульсий и суспензий. При соблюдении техники выполнения ЛП вероятность повреждения мозговой ткани минимальна.
Не касаясь в данной статье введения в эндолюмбальное пространство препаратов для анестезии и контрастных веществ, выделим показания к интратекальному введению лекарственных средств. Одним из основных показаний для введения антибактериальных препаратов в ЦСЖ методом пунктирования люмбального пространства является бактериальный менингит. Такая процедура показана при отсутствии клинического и лабораторного улучшения состояния больного в течение 72 ч после начала парентерального введения антибиотиков. Существует точка зрения, что данный временной промежуток должен быть меньше, и отсутствие санации ЦСЖ на фоне проводимого лечения в течение 24—48 ч — достаточное основание для интратекальной противомикробной терапии [2]. Показаниями для этого вида лечения являются вентрикулит, поздно начатое лечение и рецидив менингита или менингоэнцефалита, особенно у больных с иммунодефицитом. Под вентрикулитом понимают воспаление эпендимы желудочков мозга, обычно развивающееся в результате ее инфекционного поражения с резким ухудшением состояния больного, рвотой, угнетением сознания и гипертермией. Причиной его развития могут быть гематогенное распространение бактериальных агентов, распространение менингита из подпаутинного пространства, а также прорыв абсцесса мозга, в результате чего его содержимое попадает в полость желудочков.
Клинический опыт позволил определить основные группы антибиотиков, используемых для введения в ЦСЖ с учетом наиболее вероятной природы возбудителей и их резистентности к препаратам данной группы. В настоящее время при бактериальном поражении ЦНС в концевую цистерну вводятся аминогликозиды (амикацин по 5—20 мг 1 раз в сутки, гентамицин по 4—8 мг 1 раз в сутки, тобрамицин по 4—8 мг 1 раз в сутки), ванкомицин по 4—10 мг 1 раз в сутки, полимиксин В по 50 000 ЕД 1 раз в сутки (детям до 2 лет — по 20 000 ЕД в сутки), диоксидин по 5—10 мг в концентрации 0,1—1% 1 раз в сутки. Необходимо помнить о недопустимости введения в ликворное пространство калиевой соли пенициллина и колистина (полимиксин Е) — это может привести к летальному исходу прямо во время процедуры.
Коррекция этиотропного лечения, как правило, проводится после получения результатов бактериологического исследования. Такие ранее применяемые препараты, как стрептомицин, олеандомицин, морфоциклин, неомицин, мономицин, левомицетина гемисукцинат, полимиксин М в настоящее время для интратекального введения используются все реже из-за выраженной токсичности.
Перед выполнением ЛП врач должен понимать степень выраженности у больного отека головного мозга, о котором можно судить по данным нейровизуализации и офтальмоскопии. При выраженном отеке введение препаратов в концевую цистерну малоэффективно, а выведение ЦСЖ может привести к повреждению головного мозга в результате его вклинения в большое затылочное отверстие. После прокола твердой мозговой оболочки необходимо оценить проходимость субдурального пространства путем проведения ликвородинамических проб. Это особенно важно в случае наличия у пациента опухолевого или метастатического поражения спинного мозга или его оболочек. При наличии блока ликворопроводящих путей вводимый препарат не поступит интракраниально, а его миелотоксическое действие может повыситься из-за невозможности распределения в ЦСЖ.
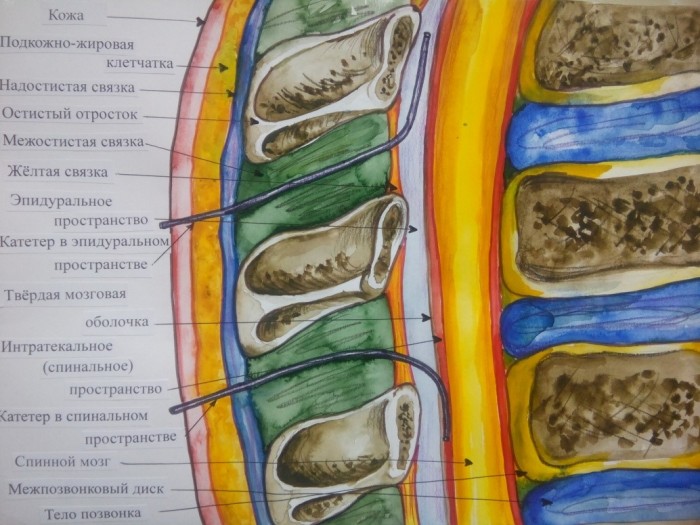
Методика введения лекарственных средств в субарахноидальное пространство состоит в следующем: разовую дозу вводимого препарата разводят в 2—3 мл изотонического (0,9%) раствора натрия хлорида. После выполнения ЛП на уровне L3—S1 (игла прокалывает кожу, гиподерму, межостистые и желтые связки отростков позвонков и твердую оболочку мозга) канюлю шприца вставляют в павильон пункционной иглы, набирают в шприц до 5—6 мл ЦСЖ и медленно вводят 2—3 мл содержимого шприца. Затем вновь наполняют шприц ЦСЖ до 5 мл и медленно вводят все содержимое шприца. После манипуляции пункционную иглу извлекают. Если состояние больного позволяет, то ему показано нахождение в постели с приподнятым ножным концом в течение 30 мин. В случае курсового введения антибиотиков показанием для отмены данной манипуляции являются появление признаков токсического воздействия препарата (снижение содержания белка в ЦСЖ ниже 1 г/л) и наступление лимфоцитарной санации ЦСЖ (кроме туберкулезного поражения ЦНС) [7].
При выборе антимикробного препарата, предполагаемого для интратекального введения, определении его разовых и курсовых доз, а также длительности курса необходимо помнить, что введение антибиотика в эндолюмбальное пространство не заменяет этиотропной терапии, получаемой больным парентерально. Кроме того, необходимо учитывать такие факторы, как аллергологический анамнез, спектр выделенных штаммов патогенных микроорганизмов и их чувствительность к антибиотикам, фармакокинетические и фармакодинамические особенности конкретных препаратов, их сочетаемость и синергизм с препаратами, в том числе антибактериальными, получаемыми больным в виде базисной терапии. Необходимо помнить о возможности появления токсических эффектов при эндолюмбальном введении препаратов, особенно при наличии у больного тяжелого сопутствующего заболевания (поражение почек, печени и т. д.), проведения больному ликворосорбционной терапии и других экстракорпоральных методов лечения.
Обращает на себя внимание, что в инструкциях по применению противобактериальных препаратов этот метод введения практически не представлен, а антибиотики, рекомендуемые для лечения менингитов, не охарактеризованы с точки зрения переносимости при введении в ликворопроводящее пространство.
Прямых противопоказаний к интратекальному введению антибиотиков нет, однако именно факторы непосредственного токсического воздействия на ЦНС большинства препаратов этой группы и противобактериальных химиопрепаратов значительно сузили спектр используемых лекарственных средств. Второй проблемой является тенденция к изменению резистентности основных нейротропных патогенов ко все еще используемым препаратам пенициллинового ряда и аминогликозидов первых поколений. Общепризнанно, что нечувствительны in vitro и клинически к этим препаратам выделенные от больных практически 90% штаммов стафилококков, до 40% — пневмококков, до 15% — менингококков (особенно в странах Азии, США, Канаде). Кроме того, наблюдается повсеместная тенденция к росту удельного веса в этиологии бактериальных нейроинфекций листерий, гемофильной палочки, энтеробактерий, традиционно резистентных к названным препаратам [8].
Другим показанием для эндолюмбального применения лекарственных средств является грибковый менингит (криптококковый, кандидозный, гистоплазмоидный, кокцидиоидомикозный), в этом случае вводится амфотерицин В. Учитывая его относительно высокое нефротоксическое действие, встречающееся у 80% больных, целесообразно применение липосомального варианта (амбизом), обладающего меньшей токсичностью. В дозе 0,25—1,0 мг он вводится 2—4 раза в сутки, через катетер, установленный в концевой цистерне [9—14].
При туберкулезном поражении ЦНС возможно интратекальное введение изониазида (до 2,5 мг/кг), хотя в реальной клинической практике это встречается редко [15].
При наличии у пациента таких нейроонкологических заболеваний, как менингеальный карциноматоз, нейролейкоз, лептоменингеальная лимфома и некоторые злокачественные опухоли ЦНС, в том числе метастазы рака, интратекально вводятся цитостатики. Метотрексат применяется в дозе 0,25 мг/кг массы тела больного, на курс 120—180 мг с началом на 7—10-е сутки после оперативного вмешательства. Недостатком данного препарата являются выраженное токсическое действие, нарастание отека в послеоперационной зоне и реактивная гиперпродукция ЦСЖ, что сопровождается внутричерепной гипертензией [16].
Необходимо отметить, что только в инструкции к применению метотрексата и противоопухолевого препарата цитозар сказано об их возможном введении в ликворное пространство. Близким по составу и действию к цитозару препаратом, который может вводиться в концевую цистерну для лечения онкологических процессов в ЦНС, является вепезид. В инструкции к применению противоопухолевого препарата велкейд (бортезомиб) отмечено о недопустимости его эндолюмбального введения и то, что во время такой процедуры были отмечены летальные случаи.
В ряде исследований была показана эффективность и безопасность интратекального введения церебролизина в остром периоде инфаркта мозга. Установлено достоверно более быстрое и значительное развитие регресса неврологического дефицита у больных, получавших такой вид лечения, по сравнению с пациентами, перенесшими ишемический инсульт, которым данный препарат в подоболочечное пространство не вводился. При однократном эндолюмбальном введении 5 мл церебролизина в первые 12 ч после развития острого инсульта и последующем лечении внутривенными капельными введениями по 10 мл через 12 ч отмечено статистически значимое повышение эффективности терапии по сравнению только с внутривенным введением препарата в той же дозе [17].
Кроме того, имеется опыт введения в ликворное пространство озоно-кислородной смеси и биологического регулятора гипофиза эпиталамина при лечении черепно-мозговой травмы (ЧМТ). Эффективность такой методики доказана в исследованиях, основанных на данных лабораторного анализа ЦСЖ, нейроофтальмологических методов, нейрокартирования и вызванных потенциалов. Динамика клинических изменений при комплексном лечении среднетяжелой ЧМТ и ее осложнений у больных, получавших такую смесь в концевую цистерну, достоверно свидетельствует о более быстром регрессе общемозговой и очаговой неврологической симптоматики, менингеального синдрома и нормализации ЦСЖ, чем у пострадавших, не получавших такого лечения [18].
В нейрохирургической практике при лечении люмбосакральных радикулопатий со стойким выраженным болевым синдромом применяется эпидуральное введение кортикостероидов, в частности дипроспана (бетаметазон) 1—2 мл (7—14 мг), триамциналона диацетата (50 мг) или метилпреднизолона ацетата (80 мг). Эти препараты, как правило, разводятся на каком-либо анестетике, чаще на лидокаине.
Для уменьшения спастичности, сопровождающей некоторые заболевания ЦСЖ, интратекально, через установленный в концевой цистерне катетер с помощью специальной помпы вводят баклофен, выпускаемый для такого применения в специальной инъекционной форме по 1 и 5 мл под торговым названием лиорезал интратекальный. Инфузия препарата непосредственно под твердую оболочку обеспечивает воздействие этого лекарственного средства на рецепторные зоны задних рогов спинного мозга.
Необходимо помнить, что попадание в субарахноидальное пространство инородных субстанций (воздух, контрастные вещества, анестетики, химиотерапевтические препараты, антибактериальные средства) может вызвать средней степени или выраженную менингеальную реакцию. Она проявляется плеоцитозом до 1000 клеток в 1 мкл, повышением содержания белка при нормальном содержании глюкозы и стерильном посеве ЦСЖ. В большинстве случаев это состояние быстро регрессирует, но иногда может привести к арахноидиту, радикулиту или миелиту. Частота таких осложнений неизвестна.
Имеющиеся сведения позволяют рассматривать введение лекарственных препаратов в ЦСЖ как один из способов повышения эффективности проводимой терапии у пациентов с различными заболеваниями нервной системы.
Конфликт интересов отсутствует.
1 В РФ в качестве лекарственного препарата не зарегистирован.
Имплантация спинальных (эпидуральных) порт-систем.
Имплантация спинальных (эпидуральных) порт-систем.
Методические рекомендации
Хроническая боль – проблема, с которой, по данным ВОЗ, встречается треть населения Земли. Хронической называют длительно существующую (более 3 месяцев) боль, связанную с заболевания различной природы и локализации. По предложению Международной ассоциации по изучению боли [IASP, 1994] боль формулируется, как «неприятное сенсорное и эмоциональное ощущение (переживание), связанное с состоявшимся или потенциальным повреждением или описываемое в терминах такового».
По данным ВОЗ треть населения планеты страдает от хронической боли. Чаще всего людей беспокоит боль в спине, основной причиной которой являются дегенеративно-дистрофические изменения позвоночника – межпозвонковых дисков и дугоотростчатых суставов, с последующим вовлечением в процесс связок, мышц, сухожилий и фасций [1]. Факторами риска развития неспецифических болей в спине являются: трудоспособный возраст (период интенсивной рабочей нагрузки на позвоночник), избыточный вес, профессиональная деятельность (тяжелая физическая работа, неподвижная статическая нагрузка на позвоночник, вибрация, монотонный физический труд), аномалии развития скелета (асимметрия тела, спондилолиз, люмбализация) [2].
К не менее актуальной проблематике относится и онкологическая боль. По самой скромной оценке более 3,5 миллионов человек в мире ежедневно мучаются от раковой боли, а у 50% из них болевое ощущение оценивается, как сильное или очень сильное [3]. Основными причинами болевых ощущений при онкологических заболеваниях являются: сама опухоль, которая вызывает вовлечение болевых афферентов различных органов и тканей (поражение костей, мягких тканей, кожи, внутренних органов, окклюзию сосудов и органов пищеварительного тракта и др.). Во-вторых, осложнения опухолевого процесса (патологический перелом, некроз, изъязвление, воспаление, инфицирование тканей и органов, тромбозы). В третьих: последствия астенизации (пролежни, трофические язвы, запоры), и наконец, в четвертых: противоопухолевое лечение само становится источником сильнейших болевых реакций [4]
Современный подход к лечению болевых синдромов построен на так называемой «лестнице ВОЗ». Суть метода заключается в пошаговой стратегии назначении препаратов различных фармакологических групп и интервенционных методов лечения в зависимости от степени выраженности болевого синдрома [6]
Так на первой ступени, при лечении боли слабой интенсивности, назначают ненаркотические анальгетики. Прежде всего, это НПВП различных групп[5].
Использование всех вышеперечисленных фармакологических групп имеет ряд побочных эффектов, которые существенно ограничивают их применение. Так при использовании НПВС возникает высокий риск желудочно-кишечных кровотечений, агранулоцитоза, развития острой почечной и печёночной недостаточности, обострения бронхиальной астмы [8].
Таблетированные опиоиды, в частности, трамал, требуют частого приема (каждые 3,5-4 часа) и обладают неблагоприятным профилем безопасности (тошнота, рвота, запоры) [11]. Инъекционные опиоиды требуют такого же частого применения (причем инъекции сопровождаются болью). Использование трансдермальных форм характеризуется быстрым развитием толерантности, нарушениями сна, дневной активности пациента [10]
Кроме того, сложность назначения, хранения, учёта наркотических анальгетиков и приравненных к ним препаратов, заставляет искать альтернативные методы и средства лечения болевых синдромов. К подобным средствам справедливо можно отнести нейроаксиальные блокады: спинальные и эпидуральные [9].
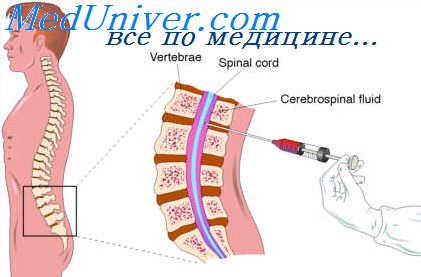
Регионарные методы обезболивания нашли широкое применение в хирургической практике как компоненты анестезии, а в дальнейшем, как эффективные методики послеоперационной аналгезии пациентов. Использование катетеров для введения местных анестетиков позволяет длительно блокировать болевую им пульсацию, идущую от периферии к центральным нервным структурам (Рис.1)
Рис.1 Анатомические структуры спины в разрезе, с эпидуральным и спинальным катетерами.
Однако, есть один недостаток этих методов: невозможность использования их вне стационара, так как выведенный наружу катетер является входными воротами инфекции даже при самом тщательном уходе за ним. Имплантируемые порт-системы, являются прекрасной альтернативой для частого и длительного введения лекарственных средств пациентам вне стационара. Использование порт-систем особенно целесообразно у пациентов с инкурабельными онкологическими заболеваниями, сопровождающимися тяжёлым болевым синдромом, который плохо купируется традиционными лекарствами.
Показания и противопоказания
Показания для постановки эпидуральных порт-систем:
Показания для постановки спинальных порт-систем:
Противопоказания к применению спинальных (эпидуральных) порт-систем:
Материально-техническое обеспечение новой медицинской технологии
Описание медицинской технологии
Процедура проводится в условиях операционной.
Накануне пациенту выполняется очистительная клизма. В день операции устанавливается периферический внутривенный катетер и проводится инфузия кристаллоидных растворов в объёме 500-1000 мл.
Имплантация порт-системы
Больной находится в положении на боку, с приведёнными к груди коленями, максимально согнутой спиной. Кожа спины обрабатывается антисептическими растворами по общепринятым хирургическим правилам. Операционное поле изолируется стерильным материалом.
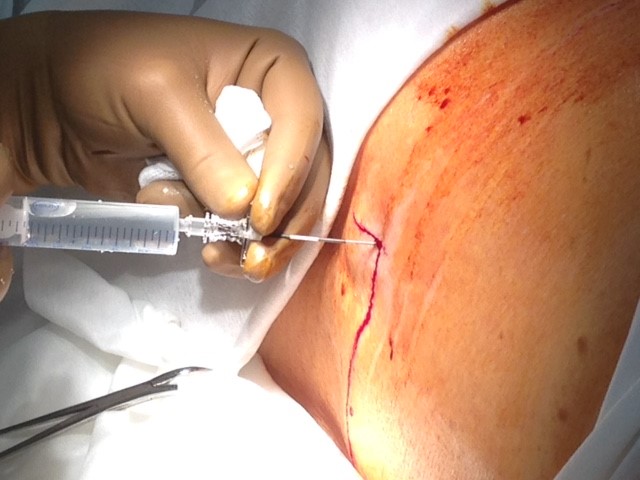
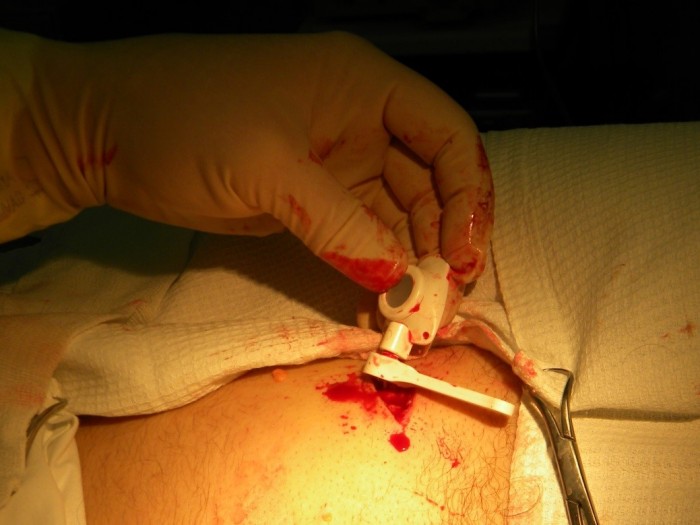
Рис. 2. Пункция эпидурального пространства
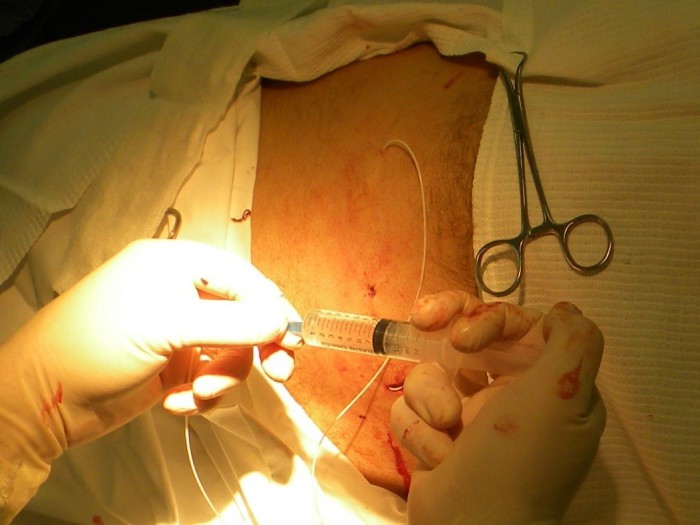
Через иглу Tuohy устанавливается полиуретановый катетер с металлическим мандреном. Катетер продвигается до тех пор, пока он не достигнет конца иглы. Производится заведение катетера с мандреном на глубину до 5 см в спинальное пространство ниже места пункции. Срез иглы Tuohy, при этом, должен быть направлен дистально. Для определения длины на катетере имеются метки, через каждые 5 см. При пункции эпидурального пространства направление введения катетера может быть разным (в зависимости от локализации источника болевого синдрома). Далее, металлический мандрен извлекается. Правильность положения конца катетера в спинальном пространстве определяется ликвореей из проксимального конца катетера. Игла Tuohy извлекается, придерживая катетер в фиксированном положении.
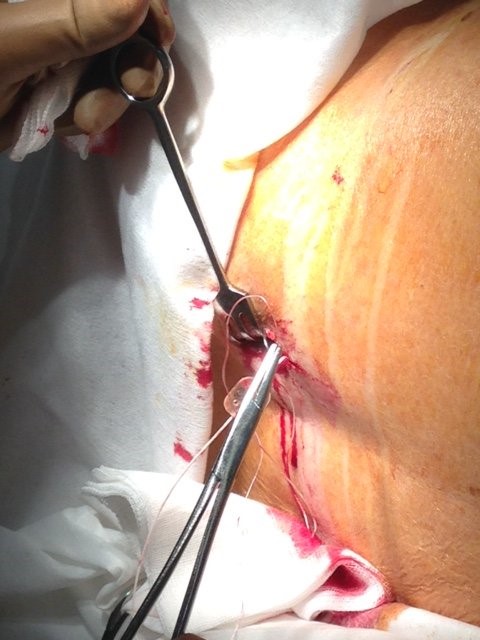
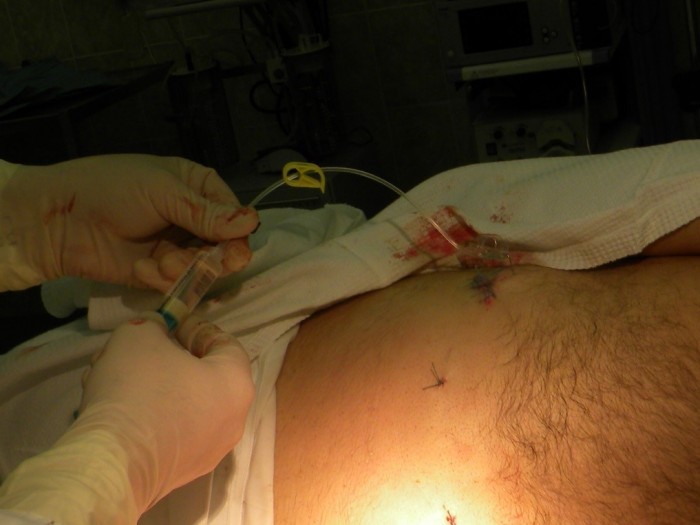
К месту выхода наружу одевается фиксатор (держатель) катетера, устройство, предотвращающее перегиб катетера. «Держатель» погружают в сформированный «карман» и пришивают за «ушко» к фасции при помощи швов (Рис. 3)
Рис. 3. Подшивание «держателя» катетера
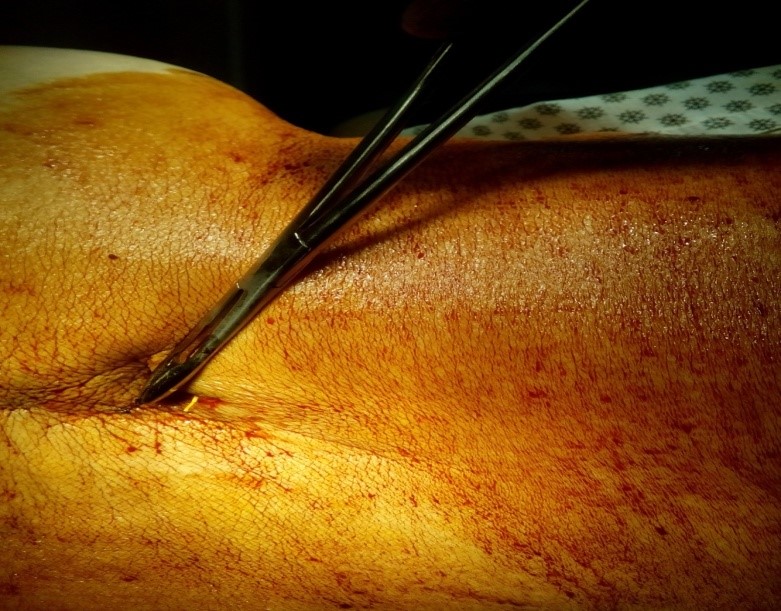
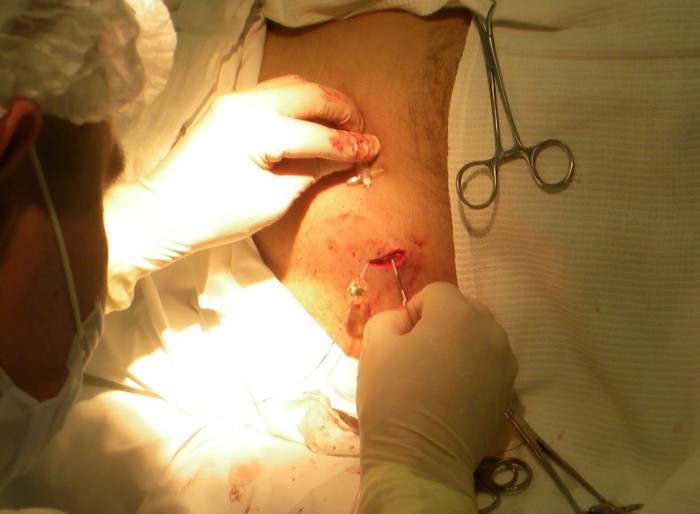
Далее, в месте пересечения задне-аксилярной линии и 11-12 ребра, в зоне имплантации камеры порт-системы осуществляется инфильтрация кожи и подлежащих тканей раствором местного анестетика для обезболивания. После этого производится разрез кожи и подкожно-жировой клетчатки длиной в 4-5 см. Тупым способом в подкожно-жировой клетчатке формируют «карман» для камеры, так чтобы она нижней поверхностью опиралась на основание ребра.
Проводится местная анестезия кожи от места выхода катетера на поверхность до места стояния камеры порт-системы. Катетер насаживается на металлический проводник – туннелизатор, которым в несколько приёмов, осуществляют проведение катетера через кожу к камере порт-системы (Рис. 4). Катетер обрезается ножницами под прямым углом на необходимую длину. При этом оставляют небольшой «люфт», рассчитанный на движение пациента (обычно 1-2 см).
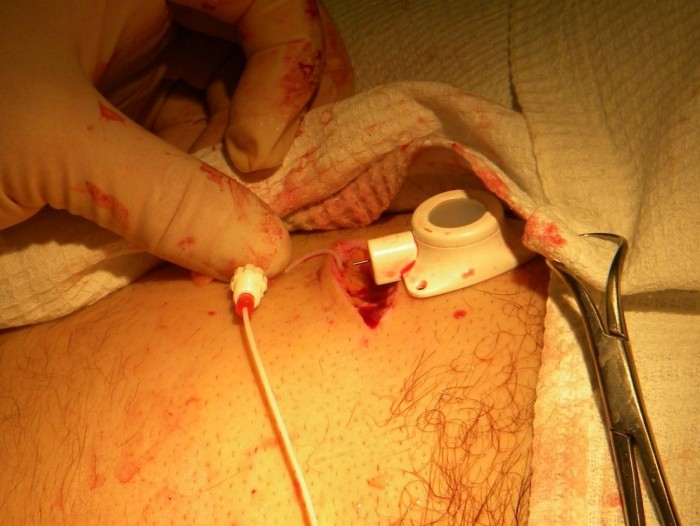
Соединительная муфта отодвигается проксимально по катетеру, его кончик вставляется в выходную канюлю камеры порта (Рис.5)
 |  |