Опухоль мочевого пузыря
Что такое опухоль мочевого пузыря?
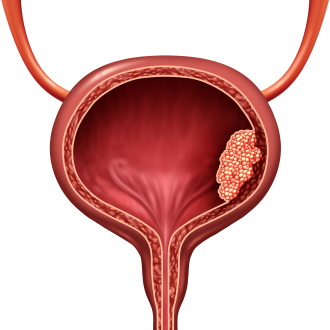
Опухолью мочевого пузыря называется новообразование, возникающее внутри или на стенке органа. По частоте встречаемости данный вид опухоли составляет порядка 4-5% и уступает лишь опухоли пищевода, желудка, гортани и легких. Наиболее часто заболевание диагностируется у мужчин старше 50 лет, однако может встречаться и у женщин (соотношение по половому признаку 4:1).
Опухоль мочевого пузыря может носить доброкачественный или злокачественный характер. В первом случае болезнь обычно устраняется малотравматичными методами – электрокоагуляцией или электрорезекцией во время цистоскопии; реже – с помощью открытой операцией. При злокачественной опухоли (раке мочевого пузыря) требуется сложное многокомпонентное лечение, включающее операцию, лучевую терапию и иммунотерапию.
Виды опухолей мочевого пузыря и стадии их развития
Новообразования мочевого пузыря по природе происхождения делятся на добро- и злокачественные. Это учитывают урологи при выборе наиболее рациональной программы лечения.
К доброкачественным относятся следующие образования:
Значительно реже в мочевом пузыре могут возникать неэпиталиальные новообразования: фибромы, миомы, фибромиксомы, гемангиомы, невриномы.
Злокачественные опухоли мочевого пузыря подразделяются на 3 вида:
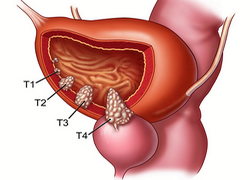
В зависимости от распространенности злокачественного процесса, выделяют четыре стадии рака мочевого пузыря:
Симптомы опухолей мочевого пузыря
Признаки опухолей мочевого пузыря во многом зависят от их размера, стадии и типа. Так, доброкачественные новообразования на ранних этапах развития могут никак себя не проявлять. Лишь со временем больной начинает испытывать трудности с выведением урины. Появляются примеси крови в моче, при акте мочеиспускания возникают болезненные ощущения в области промежности и над лобком.
Злокачественные опухоли, как правило, проявляют себя уже на начальных стадиях своего развития. В моче больного обнаруживаются примеси крови. При этом кровь может быть хорошо заметной невооруженным глазом или скрытой (диагностируется при анализе мочи на скрытую гематурию). При обильных и продолжительных кровотечениях может развиться острая задержка урины из-за заполнения мочевого пузыря кровяными сгустками. Болевой синдром локализуется в области паха или крестца. На запущенных стадиях рака боль становится непроходящей и нестерпимой.
Если мужчина или женщина игнорирует симптомы опухолей мочевого пузыря и не обращается к врачу за лечением, последствия могут быть самыми неприятными от нарушений тока мочи до общей интоксикации организма и летального исхода в последней стадии рака.
Причины опухолей мочевого пузыря
Возникновение любых опухолевых новообразований связано с патологически активным делением клеток. Подобные процессы запускаются под влиянием ряда факторов, провоцирующих мутации в генетическом клеточном материале:
Ультразвуковое трехмерное изображение при диагностике рака мочевого пузыря в процессе его комплексного химиолучевого лечения
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
Известно, что приблизительно 30-50% больных поступают в стационары с распространенным опухолевым процессом.
После местного хирургического лечения рак мочевого пузыря имеет тенденцию к рецидивированию [6].
Трудность диагностики заключается в том, что многие папиллярные формы рака мочевого пузыря представлены множественными полиморфными эндофитными, узловатыми новообразованиями с отдельными сосочковыми фокусами, ворсинчатыми структурами, иногда имеющими сливной характер, или участками изъязвлений. При этом окончательный диагноз опухоли может быть установлен при биопсии [7,8].
Ведущее место в выявлении новообразований мочевого пузыря на современном этапе принадлежит ультразвуковым методам исследования. Большая клиническая значимость ультразвуковых методов обусловлена их высокой информативностью, безопасностью для пациента и относительной дешевизной исследования. Метод двухмерно-серошкальной эхографии позволяет визуализировать объемные образования, оценивать локализацию, размеры, состояние контуров, эхоструктуру и характер их взаимодействия с окружающими органами и сосудистыми структурами, а также изучать области регионарного метастазирования и одновременно оценивать состояние других органов брюшной полости и, что особенно важно, почек [9].
По данным некоторых авторов [5,10], УЗИ дает возможность установить диагноз опухоли мочевого пузыря у 70-82% больных. При этом, согласно данным Ли-Шен-Ли и соавт. [10], проведение КТ не дает существенной дополнительной информации о распространенности процесса.
Использование традиционного трансабдоминального многоплоскостного ультразвукового сканирования не всегда оказывается достаточно информативным для точного определения объема опухоли, степени инфильтрации стенки мочевого пузыря и определения стадии бластоматозного процесса. Наличие сгустков крови, детрита и солей в полости мочевого пузыря затрудняет ультразвуковую диагностику. Наибольшие трудности возникают при инфильтративных опухолях мочевого пузыря, располагающихся в области его шейки или в мочепузырном треугольнике. Лучшими диагностическими возможностями при поражениях этих отделов обладает трансректальное ультразвуковое сканирование [10].
Материалы и методы
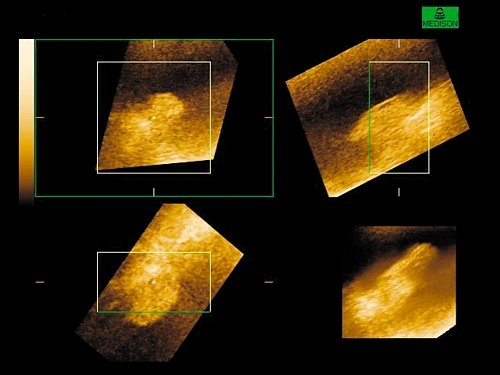
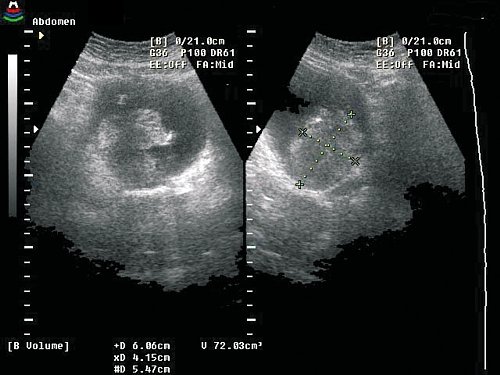
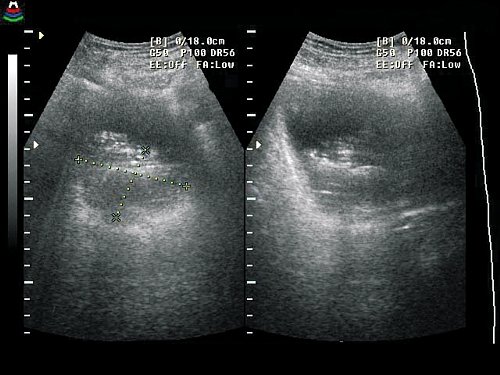
Объемную визуализацию в виде трехмерного изображения мочевого пузыря получали включением автоматической обработки, которая осуществлялась с учетом полутоновых градаций для каждого элемента трехмерного изображения вдоль соответствующей проекции выбранного направления движения сканирующего луча. В дальнейшем для улучшения качества трехмерного изображения использовались различные алгоритмы обработки и подбирались соответствующие режимы прозрачной, поверхностной, световой визуализации или их смешивание; для наилучшего выявления опухоли изменяли размер просматриваемого участка и пространственное его расположение. Использовалось цветное изображение в коричневых тонах, позволяющее получать больше информации об отдельных деталях бластоматозного процесса, в особенности о состоянии основания опухоли и степени поражения стенки мочевого пузыря (рис. 1). Использование опции позволяло сохранить трехмерное изображение в форме файла, а применение режима кинопамяти давало возможность просматривать трехмерное изображение под различными углами зрения в виде подвижного.
Рис. 1. Получение 3D изображения на основании реконструкции серии эхотомографических срезов новообразования мочевого пузыря в различных проекциях.
Результаты и обсуждение
На основании клинического, лучевого и лабораторного обследования с учетом анамнестических данных радикальное хирургическое лечение всем этим больным было противопоказано, поэтому проводилось комплексное химиолучевое лечение [11,12]. На первом этапе всем пациентам проводили дистанционное облучение области первичной опухоли. Суммарная очаговая доза составляла в среднем 60-66 Гр. Через 1 мес после окончания лучевой терапии проводилась регионарная внутриартериальная химиотерапия в сочетании с СВЧ гипертермией и селективной гипергликемией, которая по показаниям повторялась через 1-2 мес.
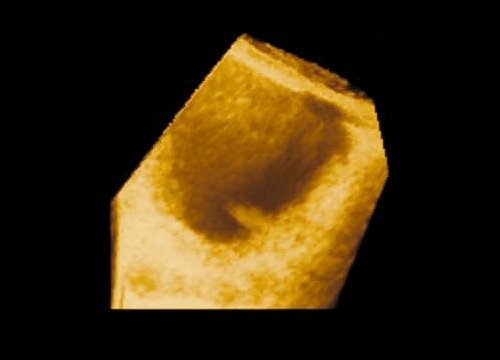
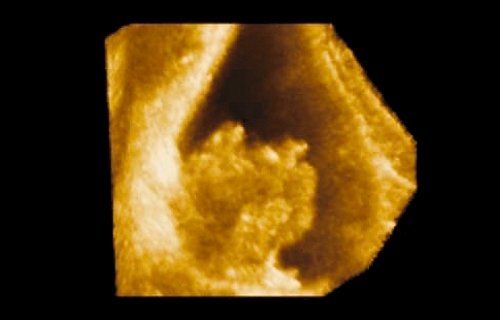
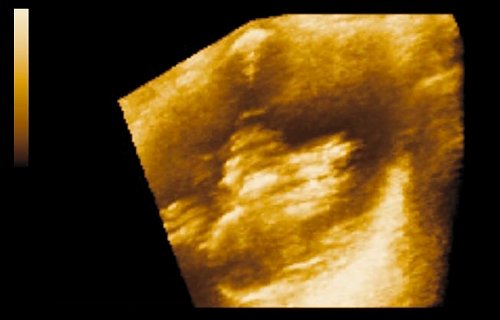
Рис. 2. Полип мочевого пузыря размером 4 мм (режим 3D).
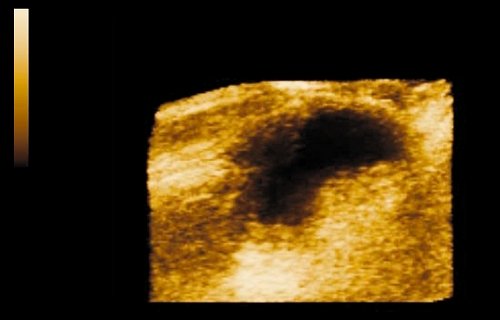
Полный регресс рака мочевого пузыря с восстановлением структуры слизистой оболочки получен у 5 пациентов. В остальных случаях положительная динамика выражалась в уменьшении размеров опухоли (рис. 3 а-г).
б) Трехмерное изображение опухоли после реконструкции.
в) Значительное уменьшение объема опухоли после комплексного химиолучевого лечения.
г) Уменьшение объема опухоли наглядно визуализируется на трехмерном изображении.
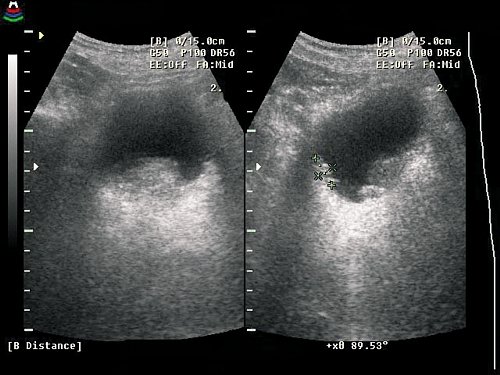
а) По задней стенке мочевого пузыря отчетливо определяется новообразование.
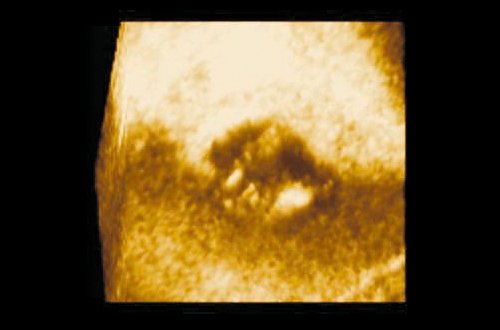
б) То же новообразование в трехмерном изображении.
в) Через 4 мес после трансуретральной резекции мочевого пузыря и химиолучевого лечения. Признаки фиброза стенки мочевого пузыря и паравезикальной клетчатки.
Выводы
Таким образом, используемый ультразвуковой метод трехмерной реконструкции позволяет выявить опухоли мочевого пузыря на ранних стадиях заболевания и их возможные рецидивы, что является новым направлением в лучевой диагностике, обеспечивающим получение объективной информации о пространственном расположении, форме, виде и объеме патологического образования. Возможность оценить степень прорастания опухолью стенки мочевого пузыря и степень вовлечения в процесс околопузырной клетчатки, соседних органов и тканей позволяет судить о стадии заболевания. В результате использования программ последующей обработки изображений можно с большой точностью судить о степени злокачественности новообразований.
Метод трехмерной реконструкции изображения обеспечивает объективный и качественный контроль за результатами проводимых лечебных мероприятий, в том числе химиолучевой терапии.
Литература
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Рак мочевого пузыря – стадии, симптомы, диагностика
Рак мочевого пузыря — это злокачественное образование на стенке мочевого пузыря или его слизистой оболочке. Болезнь занимает третью позицию после онкоурологической патологии простаты и почек. У мужчин это заболевание диагностируется втрое чаще, чем у представительниц женского пола. Ориентировочно 79% заболевших — это люди возрастом 50-80 лет. Смертность от осложнений этой болезни невысокая — от трёх до восьми процентов (статистические данные развитых стран). Каждый год в нашей стране онкология мочевого пузыря диагностируется свыше чем у 16000 человек. Число заболевших ежегодно нарастает.
Анатомия мочевыделительной системы
Мочевой пузырь (МП) — это полый орган мочевыводящей системы, располагающийся в малом тазу. Является резервуаром накопления урины, который опорожняется через уретру. Вместительность органа мужчины — 0,35-0,55 л; женщины — 0,25-0,45 л. При заполненности органа 0,15-0,25 л, происходит позыв к мочеиспусканию. Чем быстрее наполняется орган, тем сильнее происходит раздражающее воздействие на мышечные рецепторы и учащается работа мочевыводящей системы.
Рак МП: классификация и стадии
Мочевой пузырь (МП) — это полый орган мочевыводящей системы, располагающийся в малом тазу. Является резервуаром накопления урины, который опорожняется через уретру. Вместительность органа мужчины — 0,35-0,55 л; женщины — 0,25-0,45 л. При заполненности органа 0,15-0,25 л, происходит позыв к мочеиспусканию. Чем быстрее наполняется орган, тем сильнее происходит раздражающее воздействие на мышечные рецепторы и учащается работа мочевыводящей системы.
Рак МП: классификация и стадии
Злокачественная опухоль данного органа выявляется гистологическим исследованием, по степени дифференцировки клеток, образованию вторичных очагов (метастазов), характеру роста. Эти параметры крайне важны для планирования стратегии терапии.
Степень анаплазии делится на низко-, умеренно- и высокодифференцированные новообразования. Одну из главных ролей играет включение в опухелогенное действие разных слоёв стенки мочевого пузыря. По этой причине заболевание инвазивно в высокой или низкой стадии, или протекает поверхностно.
Рак мочевого пузыря классифицируется по международной системе ТNМ.
Рак МП: признаки
Возникновение рака на начальной стадии может никак себя не проявлять, проходить даже без слабых признаков. То есть, опухоль находится на первичной стадии развития, но пациент это никак не ощущает.
Слишком частое мочеиспускание также может быть вызвано опухолеобразованием. Когда неоплазия достаточно развита и достигает в размерах нескольких сантиметров, она уменьшает ёмкость мочевого пузыря. Поэтому в нём накапливается меньшее количество мочи, что является причиной слишком частого мочеиспускания.
На фоне развития новообразования нарастают болевые ощущения в области малого таза как во время мочеиспускания, так и в состоянии покоя. Боли зачастую тянущие и редко носят острый характер. На поздних стадиях боли могут быть интенсивными и продолжительными. Состояние усугубляется прогрессирующей анемией и вызванной ей общей слабостью.
Иногда опухоль расположена так, что она не даёт моче проходить из верхних мочевыводящих путей (затрудняется поступление мочи из почек в орган) это приводит к развитию хронической почечной недостаточности. В этом случае биохимический анализ крови покажет повышенное содержание мочевины и креатина.
Причины
Медики не пришли к общепризнанной этиологии данной болезни, но выявили источники риска, способствующие опухолеобразованию:
Редкое мочеиспускание и продолжительный стаз мочи. Повышенное содержание метаболитов в моче обладает опухолегенным действием, которое может спровоцировать злокачественное изменение переходных эпителий.
Инфекционные заболевания. Влияние папилломавирусных инфекций в качестве причины новообразований остаётся под вопросом. Из паразитарных инфекций мочеполовой бильгарциоз провоцирует активный канцерогенез.
Профессиональный фактор. Этому риску подвержены люди регулярно контактирующие с такими веществами, как производные ксилола, фенолы, фталаты, противораковые лекарства и пр. Зачастую это маляры, медработники, рабочие предприятий химического, нефтегазодобывающего и перерабатывающего сектора.
В некоторых случаях опухолеобразование может быть обусловлено генетически и вызвано наследственными факторами.
Рак МП: диагностика
Терапия
Опухолеобразование в мочевом пузыре можно условно разгруппировать.
Терапия на начальной стадии течения болезни может обойтись без хирургических методов. В этом случае применяется химиотерапия с применением одного или группы цитостатиков; лечение иммунологическими препаратами. Назначение препаратов этих групп зависит от величины, локации и прогрессии злокачественного образования.
Немышечно-инвазивный рак: лечение
Трансуретральная резекция мочевого пузыря (ТУР). Хирургическая операция, при которой специальное оборудование вводится через уретру. Воздействие на опухоль производится путём резекции, лазером, электрокоагуляцией.
Внутрипузырная (местная) химическая терапия. Метод заключается во введение в полость органа противоопухолевого препарата. Курс местной химической терапии от 6 до 8 еженедельных внутрипузырных инсталляций. Является эффективной методикой для профилактики возобновления данного онкозаболевания.
Проникающий рак мочевого пузыря: методы терапии
Цистэктомия. Это хирургическая операция по иссечению фрагмента мочевого пузыря или органа целиком. Степень вмешательства обуславливается протеканием рака.
Радикальная цистэктомия. Методика предусматривает комплексную эктомию органов, а именно: мочевого пузыря; фрагмента серозной оболочки брюшной полости или клетчатки пристеночного пространства таза; простаты; парного органа мужской половой системы. У женщин проводится комплексная эктомия мочевого пузыря; матки и её шейки, придатков; передней стенки влагалища. Обязательной процедурой при цистэктомии является удаление тазовых лимфатических узлов.
При необходимости эктомия усиливается дистанционным или контактным лазерным лечением, химиотарапией, общей или интравезикальной терапией иммунологическими препаратами. При отказе пациента от оперативного вмешательства назначается радикальное лечение с помощью ионизированного излучения.
Рак МП: профилактические меры
Профилактика онкологии мочевого пузыря включает в себя широкий ряд мер. Это: полное исключение спиртосодержащих напитков и сигарет; повышенная физическая активность — увеличение ходьбы; здоровое питание с включением необходимого количества овощей и фруктов; исключение из рациона хлорированной воды и прочих канцерогенов; максимальное ограничение уф-излучения.
При малейших намёках на признаки заболевания, например: участилось мочеиспускание, необходимо сразу же обратиться к квалифицированному специалисту и пройти диагностическое обследование. Злокачественное новообразование необходимо выявить на ранних этапах — от этого напрямую зависит эффективность и успех лечения. Раннее диагностирование в ряде случаев помогает избежать хирургического вмешательства. Помните: рак — сложнейшее заболевание, которое необходимо выявить своевременно.
Симптомы, лечение и удаление опухолей мочевого пузыря
Опухоль мочевого пузыря – новообразование, которое возникает в полости или на стенке органа. Болезнь может протекать как с яркими симптомами, так и без особых признаков, что часто приводит к поздней диагностике. По основной классификации опухоли бывают доброкачественными и злокачественными. Именно тип образования, его размеры и место определяют схему лечения опухоли мочевого пузыря и прогноз выздоровления.
Причины появления опухоли
Механизм развития опухолей заключается в активном делении клеток. Такие процессы могут быть запущены разными факторами, которые провоцируют мутацию генетического клеточного материала. В случае с мочевым пузырем особенно опасны курение, неблагоприятная экология и работа, связанная с химическими веществами. Эти факторы могут вызывать разные виды опухолей мочевого пузыря:
Доброкачественные опухоли часто диагностируются у рабочих, занятых в лакокрасочной, бумажной, химической и резиновой промышленности. Провоцировать заболевание может застой мочи. Чем выше ее концентрация и чем дольше она задерживается в пузыре, тем более сильным оказывается опухолегенное действие веществ в ее составе. У мужчин причинами опухолей выступают заболевания мочеполового тракта:
Ввиду особенностей анатомического строения мужчины больше подвержены риску возникновения новообразований. Злокачественные опухоли мочевого пузыря могут развиваться по тем же причинам:
Симптомы опухолевых заболеваний
Рассматривая симптомы опухоли мочевого пузыря, стоит отметить, что на раннем этапе она никак себя не проявляет. Признаки возникают, когда новообразование достигает таких размеров, при которых оно может раздражать стенки органа. В такой ситуации у человека могут быть следующие жалобы:
Методы диагностики опухоли мочевого пузыря
Поскольку опухоль может носить доброкачественный или злокачественный характер, особое значение приобретает дифференциальная диагностика. Она направлена на то, чтобы определить тип новообразования, поскольку от этого зависит схема лечения. Исходя из этого, в инструментальную и лабораторную диагностику опухоли мочевого пузыря включают:
Роль маркеров воспаления и пролиферации в диагностике резистентного гиперактивного мочевого пузыря у женщин
Хроническое воспаление мочевого пузыря сопровождается инфильтрацией стенки мочевого пузыря мононуклеарами (макрофагами, лимфоцитами, тучными и плазматическими клетками), приводящей к необратимым изменениям в его тканях фиброзу, гиперактивности детрузора и гипералгезии [1].
Слизистая оболочка мочевого пузыря, постоянно подвергающаяся растяжению и сокращениям, покрыта уротелием, который содержит многочисленные рецепторы и уроплакины, и выполняет защитную функцию [2, 3].
В структуре уротелия имеется слой гликозаминогликан–хондроитин сульфатов, гиалуроната натрия, гликопротеинови муцинов для защиты от повреждающих факторов и предотвращения адгезии уропатогенов к уротелию. Его повреждение сопровождается кровоизлиянием и продукцией цитокинов, запускающих пролиферацию и активацию тучных клеток [4, 5, 6, 7].
В последнее время как в отечественной, так и в зарубежной литературе большое внимание уделяется изучению цитокинов – биологически активных веществ белковой природы, выполняющих медиаторные функции в развитии ряда патологических процессов, в том числе воспаления. Некоторые цитокины, в частности интерлейкин 1β (ИЛ-1β), интерлейкин 8 (ИЛ-8), фактор некроза опухоли α (ФНО-α), имеют доказанную провоспалительную активность, повышение их концентрации в крови и биологических жидкостях является маркером воспалительного процесса. ИЛ – 8, секретируемый клетками мочевого пузыря и почек, играет важную роль в активации миграции нейтрофилов при внедрении уропатогенов [8, 9]. Пик экспрессии большинства цитокинов и хемокинов достигается примерно через 24 ч после внедрения уропатогена, и возвращается к исходным показателям через 2 недели [9]. ИЛ-8 относится к СХС-хемокинам и является мощным хемотаксическим и активирующим фактором для нейтрофилов. Это самый ранний провоспалительный цитокин, продуцируемый многими клетками, включая моноциты, макрофаги, Т-клетки, нейтрофилы, фибробласты, эндотелиальные клетки, кератиноциты, гепатоциты, астроциты и хондроциты. Наряду с другими цитокинами, ИЛ-8 участвует в процессах стимуляции и дегрануляции лейкоцитов, ангиогенезе, способствует миграции фагоцитов в очаг воспаления и, по мнению ряда авторов [4, 6, 7, 9], может иметь диагностическое значение при инфекциях урогенитального тракта.
Повышение концентрации ИЛ – 8 в моче может являться маркером воспаления не только при хроническом цистите, но и латентного воспаления у пациентов с симптомами гиперактивного мочевого пузыря (ГМП). По мнению некоторых исследователей, определение уровня данного интерлейкина целесообразно включать в алгоритм обследования пациенток с ГМП для выбора оптимальной и эффективной патогенетически обоснованной терапии [10].
В последние годы появляется все больше данных, подтверждающих инфекционную этиологию ГМП. Впервые в исследовании Khasriya RK. et al. [11], а затем другими исследователями, было выявлено, что внутриклеточная бактериальная колонизация может быть причиной ГМП.
В настоящее время многими исследователями [15, 16, 17, 18, 19] также предлагается рассматривать мочевой фактор роста нервов (м – ФРН) в качестве биомаркера ГМП. М – ФРН – это нейротрофический фактор, продуцируемый уротелием и гладкомышечными клетками. Хроническое воспаление сопровождается повышением секреции м-ФРН у пациентов с ГМП и детрузорной гиперактивностью, приводящим к морфологическим изменениям в системе чувствительных и двигательных нейронов мочевого пузыря и, следовательно, к детрузорной гиперактивности [12, 13, 14].
Считается, что м-ФРН играет ключевуюроль в корреляции между воспалением и болевой импульсацией, так как он продуцируется клетками уротелия, гладкомышечными и тучными клетками, при этом активируя их дегрануляцию и пролиферацию [15].
В многочисленных исследованиях повышенный уровень м-ФРН обнаружен при таких заболеваниях, как ГМП, интерстициальный цистит и простатит [8, 16, 17, 18, 19].
Некоторыми авторами [8, 16, 17] высказано мнение о том, что уровень м-ФРН может играть важную роль во взаимосвязи между субуротелиальными чувствительными волокнами и гиперчувствительностью детрузора. Также м-ФРН является медиатором в модуляции уротелиального ответа на воспаление и порога восприятия ургентности.
В последнее время в медицинской литературе все чаще появляется термин «резистентный гиперактивный мочевой пузырь», характеризующийся сохранением симптоматики после проведения пациенткой лечения более, чем двумя М –холиноблокаторами с тренировкой мочевого пузыря в течение более 1 года [20].
Liu HT. et al. [19] исследовали уровень м-ФРН в сыворотке крови и моче 34 женщин, страдающих резистентным ГМП. Было выявлено значительное повышение уровня м-ФРН в сыворотке и моче по сравнению с контрольной группой (31 здоровая женщина). Значимых отличий в уровне м-ФРН среди женщин с «сухим» и «мокрым» типами ГМП не выявлено. Также после трехмесячного курса лечения солифенацином уровень м-ФРН оставался стабильно высоким, вследствие чего авторы сделали предположение, что резистентный ГМП может быть вызван хронической инфекций.
Исходя из изложенного, целью нашего исследования было изучить роль маркеров воспаления и пролиферации (ИЛ-8 и м-ФРН) в диагностике резистентного ГМП.
МАТЕРИАЛЫ И МЕТОДЫ
В проспективное рандомизированное сравнительное открытое исследование были включены 79 женщин, из которых у 32 подтвержден диагноз резистентного ГМП, а у 47 – был хронический неспецифический бактериальный цистит. С использованием таблицы случайных чисел была проведена блочная рандомизация, вследствие чего пациентки были разделены на 4 группы:
I группа – 19 женщин с хроническим циститом, которым был проведен 10-дневный курс антибактериальной терапии с учетом чувствительности микроорганизма, после которого произведены 4 внутрипузырные инстилляции гиалуроната натрия по 1 процедуре в неделю. При этом 7 (36,8%) пациенток получали левофлоксацин по 500 мг 1 раз в день внутрь, 11 (57,9%) – цефиксим по 400 мг 1 раз в день внутрь и 1 (5,3%) – монурал 3,0 г внутрь однократно в сочетании с нитрофурантоином по 100 мг 2 раза в день в течение 7 дней (в связи с наличием микст-инфекции и разной чувствительности микроорганизмов).
II группа – 28 женщин с хроническим циститом, которым был проведен только 10-дневный курс антибактериальной терапии с учетом чувствительности микроорганизма: 11 (39,3%) пациенток принимали левофлоксацин по 500 мг 1 раз в день внутрь и 16 (57,1%) – цефиксим по 400 мг 1 раз в день внутрь.
III группа – 17 женщин с резистентным ГМП, которым была проведена комплексная терапия антибактериальными препаратами и курс из 4-х внутрипузырных инстилляций гиалуроната натрия. 7 (41,2%) пациенткам был назначен 10-дневный курс левофлоксацина по 500 мг 1 раз в день внутрь и 10 (58,8%) – 10-дневный курс цефиксима по 400 мг 1 раз в день внутрь.
IV группа – 15 женщин с резистентным ГМП получили только 10-дневный курс антибактериальной терапии с учетом чувствительности микроорганизма. При этом 6 (40%) принимали левофлоксацин по 500 мг 1 раз в день внутрь и 9 (60%) – цефиксим по 400 мг 1 раз в день внутрь.
Всем 36 пациенткам I и III групп назначали курс из 4-5 внутрипузырных введений раствора гиалуроната натрия по 50 мл 1 раз в неделю. После самостоятельного опорожнения мочевого пузыря и обработки наружных половых органов 0,2% раствором октенисепта проводили катетеризацию мочевого пузыря стерильным уретральным катетером. После введения раствора гиалуроната натрия пациенткам рекомендовали не опорожнять мочевой пузырь в течение 1 – 2-х часов для увеличения времени экспозиции препарата.
Во всех группах проводилось динамическое наблюдение через 2 недели, 6 и 12 мес после проведенного лечения.
Для количественного определения м-ФРН и ИЛ-8 было отобрано 313 образцов мочи, из них 80 образцов мочи женщин контрольной группы (средний возраст 36,5±13,3 лет), не имеющих в анамнезе и в момент обследования заболеваний урогенитального тракта и признаков инфекции мочевыводящих путей по данным экспресс-теста; 79 образцов мочи женщин исследуемых групп до начала терапии и затем через 2 недели и 6 мес после лечения (4 пациентки не явились на 3-й визит), (всего 233 пробы). Забор мочи осуществлялся в стерильную пробирку объемом 10 мл, после чего полученные биообразцы на льду в течение 15-20 мин доставлялись в лабораторию.
Образцы центрифугировались в течение 10 мин при 3000 об/мин и температуре 4оС. Для хранения супернатанты разливали в пробирки типа «Эппендорф» по 1мл, хранили до анализа при температуре минус 80 оС.
Для количественного определения м-ФРН в моче использовали набор Human beta-NGF (beta nerve growth factor) ELISA, RayBio (США).
Для определения ИЛ-8 в моче использовали набор реагентов для иммуноферментного определения концентрации интерлейкина-8 в сыворотке крови и моче, ВекторБест (Россия).
Измерение оптической плотности (ОП) в обоих случаях проводилось с помощью планшетного спектрофотометра Expert plus (Австрия).
При описании полученных результатов определяли среднее арифметическое (М), ошибку среднего (m), среднее квадратичное отклонение (σ), частоты встречаемости качественных признаков (%, доли единицы), ассиметрию и эксцесс с их ошибками, моду, медиану, квантили и 10-й с 90-м персентилем. Показатели асимметрии и эксцесса позволили оценить характер распределения, в первую очередь, его принадлежность к нормальному.