Опыт применения Финлепсина для подавления патологического влечения к алкоголю
С. Л. Кравченко, Н. В. Чередниченко,
Научный Центр наркологии МЗ РФ
Финлепсин (карбамазепин) отличается от всех других антиконвульсангов своим широким терапевтическим диапазоном. Он применяется не только для лечения судорожных и психомоторных (так называемых «височных») форм эпилепсии, но и при тригеминальной невралгии, при дисфорических состояниях, при острых шизофренических психозах с полиморфной аффективной симптоматикой, при алкогольном делирии и алкогольном абстинентном синдроме, а также в качестве антидепрессанта. Последнее связано с его воздействием на эмоциогенные зоны мозга — лимбические структуры. Именно здесь локализуется эпилептиформная активность, которая, по данным ряда авторов, является нейрофизиологической основой патологического влечения к алкоголю у больных алкоголизмом.
Мы назначали финлепсин больным алкоголизмом для купирования обострений первичного патологического влечения к алкоголю, возникших у них в процессе стационарного лечения, когда полностью миновали постинтоксикационные и абстинентные нарушения. На этапе активной терапии финлепсином использовался метод плацебо-контроля. Суточные дозы препарата колебались в зависимости от эффекта и переносимости от 200 до 1000 мг. Максимальные дозы назначались лишь в редких случаях. В ходе поддерживающего прогиворецидивного лечения, которое проводилось после выписки больных из стационара, использовались, как правило, минимальные суточные дозы.
Терапевтическое действие финлепсина было изучено у 87 больных (66 женщин и 21 мужчины). Плацебо-терапия назначалась 27 больным (16 женщинам и 11 мужчинам). Давность заболевания у всех была в пределах от 2 до 20 лет, но преобладали средние сроки — от 6 до 10 лет.
Самыми постоянными признаками обострения влечения к алкоголю были относительно малоспецифичные психопатоподобные и аффективные нарушения, сопровождающиеся более специфическими признаками — «алкогольными» сновидениями, представлениями и размышлениями. Все вместе они образуют симптомокомплекс, включающий идеаторный, поведенческий, аффективный и вегетативный компоненты. Выраженность и динамика терапевтического эффекта оценивались по оригинальной методике. В ее основу легло клиническое описание отдельных симптомов, составляющих каждый из компонентов. Каждый симптом в зависимости от его значимости наделен определенным «весом» (от «О» до «3»); сумма «весов» служит количественным выражением влечения и его компонентов.
В целом из 87 больных с обострением первичного патологического влечения к алкоголю, принимавших финлепсин в процессе стационарного лечения, явный положительный эффект, подавление или ослабление влечения, наблюдался у 81 бального (93,6%). При этом у большей части (около 60%) больных этот эффект наступал быстро — в течение 1-2 суток (34,5 %) и 5 суток (6,1%).
Наиболее рельефно благоприятные сдвиги проявлялись в сфере аффективных нарушений, которые находятся как бы «на фасаде» патологического влечения к алкоголю. Так, перед назначением финлепсина малая интенсивность аффективного компонента, оцененная в 1 балл, была у 37,8% больных, средняя (2 балла) — у 29% и большая (3 балла) — у 16,2%; спустя 2 дня соотношение интенсивностей аффективного компонента стало соответственно 16,2% — 5,4% — 0%; на 5-й день соотношение стало 8,1%—0%—0%.
Поведенческий компонент симптомокомплекса патологического влечения к алкоголю (стремление к досрочной выписке, уклонение от лечения, просьбы о дополнительном лечении, недовольство режимом, конфликтность, враждебность к тем, кто навязывает трезвость, смакование алкогольных сюжетов, попытки выпить спиртное, взбудораженность, суетливость и др. ) наблюдался гораздо реже — всего лишь у 40% больных. Его терапевтическая динамика отличается от динамики аффективного и вегетативного компонентов: в первую очередь устраняются легкие формы поведенческих нарушений и лишь затем — тяжелые и средние. Процентные соотношения больных р разной интенсивностью поведенческого компонента а) до, б) на 3-й день 150 и в) на 5-й день лечения финлепсином таковы: а) 17,5%—11,1%— 11,1%; б) 0% — 7,4% — 4,7%; в) 0% — 4,7% — 0%. Объяснением тому может служить известная клиническая закономерность: патологическое влечение к психоактивным веществам оформляется и реалипуется через личность бального.
Это особенно касается поведенческих аспектов влечения, которые, следовательно, отражают также и относительно стойкие личностные особенности. По-видимому, сравнительно лелсие поведенческие нарушения, наблюдавшиеся у ваших бальных, в меньшей мере коренятся в личностной структуре и потому быстрее уступают средствам подавления патологического влечения к алкоголю.
Идеаторная составляющая пагологаческого влечеиня к алкоголю (суждения в пользу потребления спиртного, игнорирование очевидных фактов и последствий пьянства, мнение о ненужности и вреде лечения, сомнения в будущей трезвости и др. ) оказалась более податливой к терапии. Этот компонент довольно часто отсутствовал в структуре влечения (он выявлен лишь у 58,6% больных, принимавших финлепсин). Кроме того, его принадлежность к симптоматике влечения далеко не всегда бесспорна и может быть установлена только на основе сочетания с другими признаками целого синдрома. Динамику идеаторного компонента влечения отражают следующие балльные оценки его (% % больных с интенсивностью 1,2 и 3 балла до и на 3-й день приема финлепсина): а) 40,5% — 18,1% —0% б) 23,5%— 0% —0%. Отсюда следует, что «алкогольное мышление», если оно является компонентом патологоческого влечения к алкоголю, обнаруживает большую податливость в отношении лечебного действия финлепсина, т. е. быстро наступают благоприятные перемены в точках зрения и суждениях о пьянстве, отражающих наличие тяги к алкоголю.
Оценив одним из трех баллов интенсивность компонентов патологического влечения к алкоголю у каждого больного, а затем помножив эти баллы на число бальных — «носителей» каждого балла и сложив полученные цифры, мы определим суммарную оценку интенсивности каждого компонента. Разделив на общее количество изучаемых больных, получаем среднюю интенсивность данного компонента. Разделив ее на общее количество изучаемых бальных, получаем среднюю интенсивность данного компонента в данной группе больных на данный день. Это в свою очередь позволяет графически изобразить динамику и структуру патологического влечения к алкоголю в процессе терапии определенным препаратом.
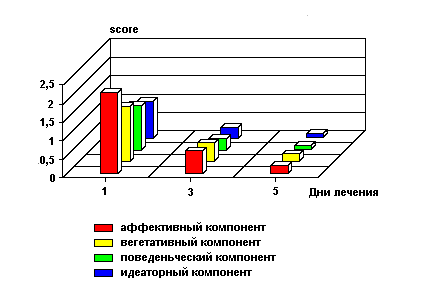
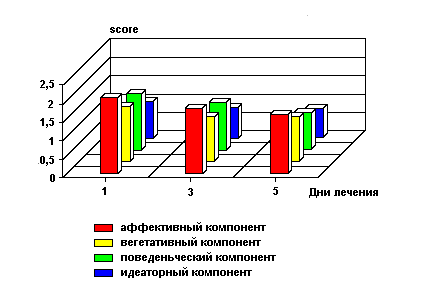
На рисунках 1 и 2, которые относятся к применению соответственно финлепсина и плацебо отражены все эти изменения. Здесь отчетливо видны групповые различия между больными в динамике компонентов влечения, при этом в группе финлепсина она весьма благоприятна.
Результаты клинических наблюдений были дополнены электроэнцефалографическим обследованием. Применяли так «называемое топографическое картирование мозга (Brain-Mapping). Этот метод компьютерной обработки позволяет извлечь из нативной ЭЭГ информацию, недоступную для рутинного анализа. Так, исследователями уже получены паттерны (карты распределения) мозговых волн, коррелирующие с шизофренией, депрессией, слабоумием; изучаются различные уровни активности психической деятельности и эффективность психофармакотерапии (Аршавский В. В., 1994, Стрелец В. Б., 1990, Уварова Л. Г., 1991, К. Maurer, 1988).
В свете этих данных с помощью топографического картирования мы сделали попытку дополнительно верифицировать эффективность подавления патологического влечения к алкоголю.
Были обследованы 15 пациентов (5 мужчин и 10 женщин) с давностью алкоголизма от 5 до 10 лет. Возраст испытуемых колебался от 20 до 53 лет. Изучаемая группа состояла из пациентов, у которых обострение влечения к алкоголю возникло в период пребывания в стационаре. В работе использовалась компьютерная программа «Нейрокартограф» научно-медицинской фирмы «МБН» (Москва).
Больному при закрытых глазах поочередно предъявляли неспецифический и специфический «алкогольный» (запах спирта) обонятельный раздражители. Проводился частотный анализ ЭЭГ в 6 стандартных диапазонах (дельта, тета-1, тета-2, альфа, бета-1 и бета-2) до и после предъявления стимулов. Изучали топографические карты распределения волновой активности головного мозга (спектр мощности частот). Исследование проводили до и после курса лечения финлепсином.
Особое внимание мы уделили анализу ритмов низких частот, которые, как известно, могут быть отражением эпилептиформной активности мозга, сопровождающей обострение патологического влечения к алкоголю.
У подавляющего большинства больных (11 из 15) в фоновой ЭЭГ были обнаружены выраженные в той или иной степени медленные колебания в дельта и тета диапазонах. Топография зон активности тяготела к затылочным и париетальным отделам полушарий.
Предъявление стимулов разнонаправленно меняло мощность и топографию медленных колебаний в зависимости от раздражителей у разных больных. Исчезновение симптомов влечения к алкоголю сопровождалось уменьшением выраженности медленных колебаний и ослаблению его реактивности. У больных без признаков патологического влечения паттерн мозговых волн практически не отличался от такового у здоровых лиц.
Полученные данные являются предварительными. Они демонстрируют достаточную чувствительность топографического картирования как инструмента для поиска электрографических коррелятов патологического влечения к алкоголю и его динамики под влиянием терапии.
Рис.1
Компоненты патологического влечения к алкоголю при лечении финлепсином
Рис. 2
Компоненты патологического влечения к алкоголю при лечении плацебо
Топ-10 лекарств, несовместимых с алкоголем
Поделиться:
О том, что спиртные напитки «не дружат» со многими лекарствами, известно давно. А вот информация, какие именно препараты не следует совмещать с алкоголем «в одном бокале», зачастую противоречива и запутанна. В рамках самообразования и подготовки к «щедрым» российским праздникам — Новому году и Рождеству — восполним пробелы в знаниях и определимся со списком наиболее распространенных лекарств, требующих исключительно трезвого образа жизни.
Сразу скажем, что «совмещать» — это вовсе не значит запивать препарат бокалом шампанского или вина. Период полувыведения лекарств может достигать 10–12 часов, поэтому, принимая лекарство утром, а «на грудь» — вечером, вы тоже совмещаете его с алкоголем.
1. Парацетамол
Мало кто знает, что один из наиболее популярных жаропонижающих и обезболивающих препаратов может быть опасен, если его сочетать с алкогольными напитками. В присутствии спиртного парацетамол метаболизируется в организме с образованием токсичных веществ, которые могут вызывать повреждение печени. Опасность наиболее велика, если совмещать длительный прием алкоголя (например, 90 мл водки или больше в сутки на протяжении нескольких дней) с высокими дозами парацетамола (3000 мг и выше).
2. Противоаллергические и противопростудные средства
Алкоголь, употребленный в тот же день с некоторыми антигистаминными препаратами, в том числе с популярными цетиризином и лоратадином, усиливает воздействие лекарств на центральную нервную систему. Это проявляется повышенной сонливостью, заторможенностью и снижением двигательной активности. Следует учитывать, что в состав многих комбинированных противопростудных лекарств входят противоаллергические компоненты и, кстати, парацетамол.
Читайте также:
Антибиотики и алкоголь: последствия
Непременно откажитесь от алкоголя, если вы принимаете Антигриппин (парацетамол + хлорфенамин + аскорбиновая кислота), АнтиФлу или Колдакт Флю Плюс (парацетамол + фенилэфрин + хлорфенамин).
3. Нестероидные противовоспалительные препараты
Они популярны и порой почти незаменимы. Ибупрофен, кетопрофен, напроксен, диклофенак и другие НПВП пьют при зубной и головной боли, разыгравшемся артрите или воспалении мышц. И нередко потребители не подозревают, что принятый на фоне лечения НПВП алкоголь многократно увеличивает риск желудочно-кишечных кровотечений. Напомню, что препараты этой группы и без того не очень лояльны к пищеварительному тракту и могут быть причиной гастропатий — заболеваний желудка. Алкоголь же способен превращать НПВП в агрессивные вещества, грозящие настоящей бедой.
4. Противокашлевые средства

Лечение довольно широко применяющимися лекарствами от сухого кашля, в том числе декстрометорфаном, входящим в состав комплексных противокашлевых средств (Терасил-Д), а также препаратами с кодеином (Терпинкод) в сочетании с алкоголем может привести к появлению сонливости, головокружения и слабости.
5. Антибиотики
Вопреки расхожему мнению, не все антибактериальные препараты категорически несовместимы с алкоголем, а только некоторые из них, в частности:
При использовании этих антибиотиков в комплексе с алкоголем происходит блокирование фермента, ответственного за разложение токсичного ацетальдегида. Последний, накапливаясь, вызывает затруднение дыхания, тахикардию, появление чувства страха, озноба или жара, падение артериального давления, рвоту. Кстати, именно так работают препараты, которые применяют для «кодирования» от алкоголизма, в частности, дисульфирам (Тетурам).
6. Средства для лечения сахарного диабета 2-го типа
Диабетикам вообще нужно быть крайне осторожными с алкоголем — ведь он способствует повышению уровня сахара в крови. Тем более если налегать на спиртное, принимая сахароснижающие лекарства, в частности метформин («золотой стандарт» для лечения диабета): резко повышается риск крайне опасного осложнения — лактоацидоза. Он характеризуется повышением уровня молочной кислоты в крови, которое становится смертельным почти в 50 % случаев.
7. Препараты, снижающие артериальное давление

Гипертоники, которые пытаются контролировать давление с помощью лекарств и при этом не отказывают себе в рюмочке-другой, также рискуют пасть жертвой несовместимости препаратов с алкоголем. Врачи не рекомендуют сочетать прием квинаприла, верапамила, доксазозина, празозина, клонидина (Клофелина), лозартана, амлодипина, лизиноприла, эналаприла и гидрохлортиазида со спиртными напитками. В противном случае могут появиться головокружение, сонливость, обморочное состояние, а также нарушения работы сердца, включая аритмию.
8. Средства, снижающие уровень холестерина в крови
Препараты, предназначенные для нормализации содержания липопротеинов (холестерина) в крови, также нельзя совмещать с алкогольными напитками во избежание поражения печени. Следует отказаться от спиртного, если вы принимаете статины — препараты первой линии для борьбы с дислипидемией, а именно аторвастатин, ловастатин, розувастатин, симвастатин.
9. Антидепрессанты
Крайне осторожно нужно подходить к алкогольным возлияниям больным депрессией, получающим медикаментозное лечение. Трициклические антидепрессанты (например, амитриптилин) в комбинации с алкоголем дают мощный седативный эффект. Сочетание незначительных доз спиртного с современными ингибиторами обратного захвата серотонина (например, пароксетином, флуоксетином, эсциталопрамом и др.) еще может пройти для выпивающего безнаказанно. Однако регулярные алкогольные нагрузки на фоне антидепрессантной терапии грозят ухудшением состояния: усилением тревоги и чувства безнадежности, снижением двигательных функций.
10. Седативные
Алкоголь оказывает седативное, т. е. успокоительное действие. Если же вы принимаете успокоительные препараты и при этом позволяете себе «принять на грудь», будьте уверены: эффект седативных средств под действием доз этанола непременно увеличится, что проявится заторможенностью, снижением двигательной активности, сонливостью и потерей концентрации внимания. Поэтому категорически не рекомендуется предаваться зеленому змию тем, кто лечится снотворными (золпидемом, зопиклоном, доксиламином), успокоительными средствами (в том числе и растительными, к примеру, тем же экстрактом валерианы) и тем более транквилизаторами (феназепамом, диазепамом и т. п.).
Опасное сочетание: лекарство и алкоголь
Алкоголь противопоказан фактически при любых болезнях. И дело не только в том, что содержащийся в нем этанол сам по себе токсичен. Он вступает во взаимодействие с действующими веществами лекарств, что может привести к опасным побочным эффектам.
Конечно, не все лекарства в сочетании со спиртным становятся опасны. Однако есть определенные группы препаратов, которые совместимы только с трезвостью. При этом некоторые из них могут выводиться из организма до 10-12 часов, а порой иметь накопительный эффект в течение нескольких дней. Проконсультируйтесь с врачом и внимательно прочитайте инструкцию перед приемом препаратов, чтобы знать о противопоказаниях.
В преддверии праздников рекомендуем ознакомиться с этим списком!
Какие лекарства несовместимы с алкоголем?
Антибиотики
Важно понимать, что, если вам прописали антибиотики, то дело серьезное! Прием таких препаратов во время болезни оказывает сильное влияние на организм, поэтому алкоголь только увеличит нагрузку на печень и другие органы. Есть ряд антибиотиков, которые, соединяясь с этанолом, становятся токсичными. Употребив их вместе со спиртными напитками, вы можете почувствовать жар, озноб, тошноту, падение давления. Кроме того, многие антибиотики под воздействием спиртного просто теряют свои свойства, что может отсрочить выздоровление.
Парацетамол
В сочетании с алкоголем образует токсичные вещества, небезопасные для печени. Кстати, парацетамол входит в состав многих противопростудных средств. Так что, если вы решили “подлечить” простуду спиртным, то убедитесь, что не употребляли в этот день парацетамол ни в какой форме.
Нестероидные противовоспалительные препараты
Эти лекарства, эффективные при боли и воспалениях, не безобидны для пищеварительного тракта. При частом применении они могут даже вызывать заболевания желудка. Алкоголь же только усиливает их действие, что может привести к опасным последствиям вплоть до желудочно-кишечных кровотечений.
Препараты для понижения давления
При перепадах давления организм очень уязвим. В сочетании с алкоголем такие лекарства могут вызвать слабость, головокружение, сердечную аритмию и даже обморок.
Успокоительные и снотворные средства
Алкоголь усиливает их действие, приводя к таким побочным эффектам, как заторможенность, сонливость, потеря концентрации. В тяжелых случаях возможно угнетение дыхания и обмороки.
Препараты для понижения уровня холестерина
Дополненные алкоголем, они создают небезопасную нагрузку на печень.
Антигистаминные средства
Алкоголь усиливает их нагрузку на ЦНС, что приводит к заторможенности и сонливости. Опьянение будет намного сильнее обычного, а это может быть очень опасно.
Какие лекарства можно употреблять с алкоголем?
Сорбенты
Всасывают токсичные вещества и выводят их из организма. Будьте осторожны! Если принять сорбент до застолья, вы рискуете выпить больше алкоголя, так как опьянение будет наступать медленнее. А вот сорбенты перед сном или утром после праздника значительно снизят похмельный синдром.
Ферменты
Помните, что злоупотребление спиртными напитками в любом случае вредит Вашему здоровью! Соблюдайте меру во время праздников и будьте здоровы!
Диагностика и лечение алкогольного абстинентного синдрома
Наиболее часто встречающимся состоянием, требующим неотложной терапии в наркологической клинике, является абстинентный синдром (АС). Абстинентный синдром — группа симптомов различного сочетания и степени тяжести, возникающих при полном прекращении прием
Наиболее часто встречающимся состоянием, требующим неотложной терапии в наркологической клинике, является абстинентный синдром (АС).
Абстинентный синдром — группа симптомов различного сочетания и степени тяжести, возникающих при полном прекращении приема вещества или снижении его дозы после неоднократного, обычно длительного и/или в высоких дозах употребления данного вещества [9]. АС считается одним из проявлений синдрома зависимости, поэтому дифференциальный диагноз обязательно должен проводиться не только с другими синдромами, возникновение которых связано с употреблением психоактивных средств, но и с тревожными состояниями, депрессивными расстройствами.
Симптоматику АС разделяют на неспецифическую (резкое усиление тяги к употребляемому веществу, быстро нарастающую астенизацию, тревогу, депрессивный эффект, вегетативные нарушения и др.), характерную для всех видов нарко- и токсикоманий, так и специфическую, характерную только для определенного вида наркотизации.
Алкогольный абстинентный или похмельный синдром (ААС) — явления психического и физического дискомфорта, включающие комплекс расстройств, возникающие вслед за прекращением регулярного употребления алкоголя на фоне выраженного влечения к нему.
Впервые термин «абстиненция» был применен Ф. Е. Рыбаковым (1916), назвавшим так «истинно похмельные расстройства» [12]. Однако четкое определение термина ААС, систематизация его симптомов безусловно принадлежат С. Г. Жислину [3].
В англоязычной литературе под абстиненцией (absatinence) обычно понимается полное воздержание от алкоголя (т. е. трезвость, в том числе и после лечения), а для обозначения АС используется термин «синдром отнятия» (withdraqal syndrome).
ААС, как правило, формируется после 2–7 лет злоупотребления алкоголем, а клинически отчетливо проявляется во II стадии алкоголизма, в отдельных случаях, при крайне интенсивной алкоголизации ААС, сроки сокращаются до 1-1,5 лет. В последнее время прослеживается тенденция резкого сокращения сроков формирования ААС (наследственная предрасположенность к алкоголизму, раннее начало употребления алкоголя и т. д.). При возобновлении употребления алкоголя в случае многолетнего воздержания от него (например, длительная ремиссия) похмельные явления наблюдаются вновь, на фоне рецидива алкоголизма с клиническими признаками той же стадии, на которой началась ремиссия [8].
Оценку степени развития (табл. 1) и выраженности клинических проявлений проводят по шкале F. Iber (1993).
Основными целями лечения ААС являются: устранение возникших симптомов и предупреждение их дальнейшего развития (смягчение симптомов, возникающих вследствие прекращения поступления этанола, и детоксикация — нормализация гомеостаза) (табл. 2), профилактика возможных осложнений, а также лечение сопутствующих алкоголизму заболеваний, отягощающих течение АС.
Проявления ААС могут смягчаться другими супрессорами ЦНС, сходными с этанолом по действию на мозговые рецепторные системы. Препаратами выбора являются транквилизаторы бензодиазепинового ряда: диазепам, клоразепат (транксен), лоразепам (лорафен, ативан, трапекс и др.) и хлордиазепоксид (элениум, хлозепид), обладающие анксиолитическим (противотревожным), седативным, снотворным, миорелаксирующим, вегетостабилизирующим и противосудорожным действием, а также снотворные средства — нитразепам (берлидорм, нитросан, радедорм, эуноктин и др.), флунитразепам (рогипнол, сомнубене) и феназепам [2, 4, 10]. Бензодиазепины быстро снижают аффективное напряжение, устраняют тревогу, тремор, гипергидроз, лабильность гемодинамики и другие вегетативные проявления ААС. Средствами выбора из числа производных бензодиазепина при абстинентных судорожных припадках и эпилептическом статусе являются диазепам и лоразепам [10].
Существует методика введения диазепама с учетом показаний шкалы CIVA-Ar, с добавлением 5 мг препарата каждый раз, когда состояние пациента оценивается выше, чем в 8 баллов [7].
При лечении ААС необходимо помнить о том, что бензодиазепины могут:
Производные барбитуровой кислоты (фенобарбитал, гексенал, тиопенталнатрий) способны смягчать проявления ААС, благодаря седативному и снотворному (а также противосудорожному) действию. Парентеральное введение барбитуратов рекомендуется только в специализированных отделениях с реанимационным оснащением.
Другим препаратом выбора в лечении ААС является карбамазепин (карбатол, тегретол, финлепсин и др.), обладающий антиабстинентным действием и усиливающим соответствующие эффекты других нейротропных средств. Карбамазепин оказывает благоприятное влияние на аффективное состояние, купирует дисфорические проявления (нормотимическое действие), уменьшает влечение к приему алкоголя и снижает судорожную готовность.
Значительно повышают эффективность лечения ААС β-адреноблокаторы — пропранолол (анаприлин, индерал, обзидан), обладающие выраженным нейротропным (вегетостабилизирующим и анксиолитическим) действием, благоприятно воздействующие на гемодинамику (снижая АД и ЧСС), потенцирующие действие супрессоров ЦНС, позволяющие уменьшать дозы производных бензодиазепина.
Пропранолол не следует применять без предварительного обследования, поскольку он противопоказан при обструктивных заболеваниях легких, нарушениях сердечной проводимости, брадикардии.
Способностью смягчать проявления ААС обладает препарат ГОМК (натрия оксибутират) в связи с выраженной нейропротективной активностью, а также способностью снижать порог судорожной готовности. Сочетанное введение натрия оксибутирата и диазепама (в отдельных случаях — барбитуратов) позволяет достичь оптимального их комплексного (седативного, снотворного, анксиолитического и миорелаксируюшего) воздействия, предупреждающего возникновение судорожных состояний.
В настоящее время нет единого мнения о целесообразности применения нейролептиков и антидепрессантов при ААС. В большей степени это связано с тем, что недифференцированное применение нейролептиков, особенно с выраженными холинолитическими свойствами — хлорпромазина (аминазин, ларгактил и др.) и левомепромазина (нозинан, тизерцин и др.), а также принадлежащего к категории антигистаминных препаратов — прометазина (авомин, дипразин, пипольфен), и антидепрессантов, особенно трициклических — амитриптилина (амизол, дамилен, триптизол, эливел), имипрамина (имизин, мелипрамин и др.), кломипрамина (анафранил, гидифен, кломинал, хлоримипрамин), может приводить к развитию делирия (особенно у больных с явлениями энцефалопатии), повышает риск развития судорожных припадков и является наименее обоснованным в патогенетическом отношении.
Применение антидепрессантов при АС может быть оправдано в тех случаях, когда в структуре психопатологического синдрома заметное место занимают аффективные нарушения, и при склонности к развитию депрессивных состояний, когда удается купировать наиболее острые симптомы ААС (третий-четвертый день активной детоксикационной терапии).
Определенный интерес для лечения ААС представляет антидепрессант тианептин (коаксил), а также обладающий тимоаналептическим действием гепатопротектор — адеметионин (гептрал), механизм действия которого отличается от моноаминергического влияния обычных антидепрессантов.
Лечение ААС включает детоксикацию и меры по метаболической коррекции. Клиренсовая детоксикация обычно проводится методом форсированного диуреза с внутривенным введением плазмозамещающих растворов — кристаллоидов (солевых растворов), декстрозы (глюкоза, глюкостерил) и препаратов поливинилпирролидона (гемодез), так и экстракорпоральными способами. Обычно при купировании неосложненного ААС необходимая детоксикация достигается путем введения солевых растворов при достаточной коррекции водно-электролитного баланса, и для инфузии препаратов поливинилпирролидона (в том числе гемодеза) показаний не возникает. Она оправдана лишь при выраженной алкогольной интоксикации и развитии алкогольного делирия с грубыми метаболическими сдвигами, обусловленными соматическими нарушениями (например, пневмонией).
Суточный объем вводимой жидкости варьирует от 400 до 2000 мл [10], поэтому проводить его рекомендуется под контролем объема циркулирующей крови, поскольку превышение индивидуально определяемой дозы может вызывать гипергидратацию, приводить к повышению внутричерепного давления, избыточной нагрузке на миокард и ряду других неблагоприятных последствий. При необходимости мочеотделение может усиливаться благодаря назначению мочегонных салуретиков — фуросемид (лазикс), а при повышенном внутричерепном давлении и судорожном синдроме — осмотических диуретиков — маннитол. Следует избегать назначения салуретиков в прекоматозных и коматозных состояниях, а также при гипокалиемии, в связи с возможностью усугубления последней.
Декстрозу не следует вводить при отсутствии информации о толерантности к углеводам у конкретного больного, учитывая, что длительное употребление алкоголя приводит к гипогликемии, а введение декстрозы на фоне ААС может привести к резкому истощению церебрального запаса тиамина витамина (В1) и способствовать развитию острой энцефалопатии и провокации острого алкогольного делирия. Поэтому введение декстрозы у больных алкоголизмом должно предваряться введением не менее 100 мг тиамина. Весьма существенную роль в развитии и течении психопатологических и неврологических проявлений острых алкогольных расстройств играет дефицит витаминов — пиридоксина (витамина В6), рибофлавина (витамина В2), цианокобаламина (витамина В12), кислоты аскорбиновой (витамина С), кислоты никотиновой (витамина РР), кислоты фолиевой (витамина Вс), ионов магния (Mg+) и калия (K+), натрия (Na+), а в отдельных случаях избыток последнего. Уже на начальных этапах клиренсовой детоксикации необходимо внутривенное введение препаратов калия и магния (магния сульфат). Следует предостеречь от внутривенного введения детоксикационных растворов без предварительного приема (в том числе внутрь) нейротропных лекарственных средств с антиабстинентным действием.
Наиболее удачным и сбалансированным сочетанием витаминов, из имеющихся ампулированных форм, является мильгамма (2 мл в ампуле содержат: В1 — 100 мг; В6 — 100 мг; В12 — 1 мг). Препарат назначается парентерально. Драже мильгаммы, в отличие от раствора для иньекций, содержат бенфотиамин, биодоступность которого в 5-7 раз выше обычного тиамина (использование которого per os мало эффективно). Поэтому, дальнейшая пероральная терапия мильгаммой (драже) позволяет достичь хороших клинических результатов. Прием 1 драже мильгаммы (100 мг бенфотиамина и 100 мг пиридоксина) из расчета 200–300 мг бенфотиамина в сутки позволяет не только успешно лечить ААС, но и оказывается эффективным при алкогольной нейропатии.
Ионный дисбаланс (Mg+, K+, Са+, Na+) необходимо корригировать под контролем их содержания в плазме крови. Недостаток ионов магния лучше восполнять кормагнезином, в 10% или 20% растворе для инъекций (в 10 мл — 1 или 2 г магния сульфата соответственно), дополнительно уровень магния можно повышать, добавляя перорально магнерот (в 1 драже — 500 мг магния оротата).
Дополняющим компонентом лечения ААС является пирацетам (луцетам, ноотропил и др.), который не следует назначать больным с судорожной готовностью. С этой же целью перспективным может оказаться использование препарата семакс, который, благодаря легкости введения (закапывание в носовые ходы), может найти применение в различных ситуациях, особенно на догоспитальном этапе.
Существует [6] методика купирования ААС метадоксилом (900 мг разводят в 500 мл изотонического раствора декстрозы или натрия хлорида, вводят в/в капельно 1 раз в сутки в течение как минимум 3 дней).
При ААС неотложные меры на догоспитальном этапе включают:
Подбор необходимого перечня препаратов, а также разовых и суточных доз производится строго индивидуально, зависит от тяжести ААС, психического и соматоневрологического состояния пациента и может широко варьировать (табл. 3). Правильная оценка состояния больного с ААС и знание принципов его лечения являются залогом успешного лечения и профилактики возможных осложнений.
По вопросам литературы обращайтесь в редакцию.
В. Г. Москвичев, кандидат медицинских наук
МГМСУ, ННПОСМП, Москва

 Читайте также:
Читайте также: 