НОРМОТИМИКИ: ПРОТИВОСУДОРОЖНЫЕ ПРЕПАРАТЫ КАК СТАБИЛИЗАТОРЫ НАСТРОЕНИЯ
Нередко перед пациентами после рекомендованных врачом назначений и прочтении инструкции к препарату возникает тревожащий вопрос «Мне назначили противосудорожный препарат. У меня эпилепсия?». В этот момент очень важно грамотно объяснить широкое действие противосудорожного препарата. Ведь чаще всего, если не всегда, в психиатрии они используются с иными целями, одна из которых – достижение состояния эутимии, или как говорят пациенты – ровного комфортного настроения без колебаний и резких перепадов.
Почему противосудорожные препараты нормализуют настроение?
Чтобы понять применение противосудорожных препаратов в сфере нарушений настроения и эмоций, следует обратиться к известной нейробиологической гипотезе, которая носит сложное название «феномен амигдалярного киндлинга». Киндлинг от английского кindle — зажигать; амигдала — зона головного мозга, отвечающая за эмоциональные реакции. Сущность процесса заключается в том, что различные химические, психологические и другие раздражители, воздействуя на амигдалу и лимбическую систему, которая отвечает за регуляцию вегетативного, поведенческого, инстинктивного, в том числе эмоционального поведения, накапливаются в этих зонах мозга и, доходя до сверхпорогового уровня, как бы разряжаются. Именно эта разрядка и приводит к эмоциональным всплескам, если мы говорим только о нарушениях эмоций. Подобный процесс происходит и при развитии эпилептических приступов. Именно поэтому противосудорожные препараты одинаково эффективны как при эпилепсии, так и при нарушениях настроения, эмоций и поведения.
Противосудорожные препараты со свойством стабилизации настроения носят различные синонимичные названия: стабилизаторы, нормотимики, тимоизолептики.

Противосудорожные препараты, которые являются одновременно стабилизаторами настроения: препараты вальпроевой кислоты (конвулекс, депакин), карбамазепин (финлепсин), ламотриджин, окскарбамазепин (трилептал), топирамат, габапентин, прегабалин, левитерацитам.
Карбамазепин — препарат, обладающий противотревожным, антидепрессивным эффектом и слабым антиманиакальным эффектом, что делает его универсальным стабилизатором настроения. Карбамазепин в контексте влияния на настроение повышает психическую активность, улучшает настроение, смягчает раздражительность и вспыльчивость, эффективен при депрессии с тревогой, усталостью, плаксивостью, вялостью.
Кроме стабилизации настроения, препарат эффективен при:
Окскарбамазепин — препарат, отличающийся более слабым седативным эффектом по сравнению со схожим по структуре карбамазепином, чаще применяется при маниакальных состояниях.
Эсликарбамазепин — активная форма окскарбамазепина. В настоящее время проводятся исследования как потенциального стабилизатора настроения.
Препараты вальпроевой кислоты — эффективны при лечении острой маниакальной фазы, при профилактике возникновения рецидива, менее эффективны при депрессивных состояниях. При смешанных состояниях, когда депрессия вплетается в манию, вальпроаты обладают большей эффективностью. Возможные побочные явления (сонливость, тошнота, аллергические реакции) носят строго временный характер.

Ламотриджин — препарат с доказанной эффективностью в отношении депрессивных фаз при БАР, но менее эффективен, и даже не одобрен, при маниакальных состояниях.
Топирамат — противосудорожный препарат, который обладает слабыми тимостабилизирующими свойствами и применяется в качестве вспомогательного средства при биполярном аффективном расстройстве, которое сопровождается бессонницей, тревогой, повышением массы тела, злоупотреблением ПАВ.
Габапентин и прегабалин — препараты с незначительным нормотимическим действием, особенно эффективные при тревоге, бессоннице и боли. Если и назначаются пациентам с БАР, то только с целью облегчить состояние.
Таким образом, наиболее часто используемые с подтвержденной эффективностью стабилизаторы настроения — карбамазепин и вальпроаты, которые, кроме того, не влияют на память и когнитивные функции. В результате при лечении сохраняется умственная работоспособность, профессиональная активность, у детей не ухудшаются показатели обучения. Показательно, что карбамазепин и вальпроаты эффективны в отношении любого заболевания, в структуре которого развиваются нарушения настроения (биполярное расстройство, шизофрения, невроз, депрессия и т.д.).
Побочные эффекты
Подбор оптимальной дозировки должен осуществляться непосредственно врачом. Побочные эффекты, являющиеся неотъемлемой частью любой медикаментозной терапии, развиваются в ответ на прием препарата, носят временный характер и корректируются вместе с дозой лекарства врачом. К их числу относятся тошнота, сонливость, вялость, мышечная слабость, смазанность речи, головокружение, двоение в глазах. Важное условие во избежание неприятного опыта применения препарата – постепенное наращивание дозы под контролем врача клиники.
На этапе подбора дозы препарата важно регистрировать такие симптомы как:
Возникновение данных явлений — свидетельство достаточного фармакологического действия.
Во избежание негативных эффектов можно снизить дозу нормотимика и добавить другой препарат с тем же эффектом. В таком случае будет достигнута стабилизация настроения и исключены побочные эффекты. При этом следует учитывать, что назначение любого психотропного препарата, в особенности нормотимиков носит персонифицированный характер. И несмотря на стремительное развитие психофармакологии, лечение стабилизаторами настроения, так необходимых в стратегии ведения пациентов с любой психической патологией, становится не строгой научной тактикой, а индивидуальным искусством доктора.
Применение финлепсина как адъювантного средства при психических и психосоматических расстройствах
Доклад на симпозиуме НЕЙРОПСИХОТРОПНЫЕ ПРЕПАРАТЫ, Москва, ноябрь 1994 г.
В. Н. Краснов,
Московский НИИ психиатрии МЗМП РФ
Современная стратегия психофармакотерапии строится на приоритете безопасности применяемых средств. Достижение собственно терапевтического эффекта подчиняется этому основному требованию и предполагает соблюдение баланса терапевтической активности тех или иных фармакологических воздействий и индивидуального ресурса их переносимости. В то же время, несмотря на все расширяющийся диапазон психотропных средств, практически ни одно из них не лишено побочного действия. Особые трудности в осуществлении активной психофармакотерапии связаны с появлением неспецифических вегетативных и нейротоксических побочных эффектов, в отношении которых традиционные корректоры малоэффективны. Это выдвигает задачу поиска средств адаптогенного действия, предупреждающих негативные эффекты психофармакотерапии и вместе с тем не препятствующих реализации собственно лечебного эффекта основного терапевтического агента. В этом отношении специального внимания заслуживает карбамазепин, обладающий сочетанием различных психотропных и соматотропных свойств, в частности антипароксизмальных, тимо- и вегетостабилизирующих, анальгетических. Между тем возможности использования карбамазепина в качестве дополнительного, адъювантного средства, потенцирующего или модулирующего клинические и биологические эффекты других психотропных средств, в настоящее время полностью еще не оценены. Терапевтические исследования такого рода практически отсутствуют, по-видимому, в силу определенных методических трудностей дифференцированной оценки результатов сочетанной терапии по сравнению с достаточно хорошо разработанными методическими принципами клинических испытаний лекарственных средств, применяемых в форме монотерапии.
Результаты собственных клинических наблюдений позволяют выделить некоторые особенности терапевтической динамики ряда психических заболеваний при присоединении карбамазепина (финлепсина) к основной терапии и наметить перспективы сочетанной (включающей финлепсин) психофармакотерапии. Отдельные эмпирически найденные факты успешного применения финлепсина в первую очередь были связаны с его включением в тот или иной терапевтический курс в качестве тактического приема, направленного на купирование и предупреждение дисфорических реакций, вегетативных кризовых состояний, мигренеподобных головных болей и других острых алгических сенсаций, пароксизмально возникающих деперсонализационно-дереализационных феноменов, нарушений схемы тела в структуре психических расстройств экзогенно- органической природы, а также эндогенных и психогенных заболеваний, развивающихся на органически измененной почве (С. Г. Жислин, 1965). Такого рода положительные эффекты финлепсина в целом соответствовали его известной антипароксизмальной активности. Между тем в процессе все более широкого применения финлепсина, в том числе в качестве средства систематической профилактической терапии при аффективных расстройствах, накапливающиеся данные давали основание предполагать наличие у финлепсина уникальных свойств своеобразного корректора самых разных (неврологических, вегетативно-соматических, психопатологических) реакций патологически измененной почвы. Имеются в виду проявления декомпенсации органически и соматически измененной, «уязвимой» почвы в ответ на различные экзогенные неблагоприятные факторы. В этот круг могут быть включены и некоторые формы патологического реагирования на активные терапевтические воздействия. Здесь в первую очередь следует назвать явления диссоциированной лекарственной толерантности, характеризующейся расхождением между темпом развития терапевтического эффекта и опережающими его проявлениями побочного действия лекарственных средств.
Диссоциированная лекарственная толерантность нередко создает существенные трудности в терапии эндогенных аффективных и бредовых расстройств, сочетающихся с резидуальными или текущими (в частности сосудистыми) церебрально-органическими поражениями. В строгом смысле слова низкая курабельность таких состояний не может быть отнесена к категории резистентности, хотя и подпадает под ее формальный критерий неэффективности условно адекватной терапии. Собственно биологическая чувствительность к фармакологическим агентам сохраняется, однако порог терапевтической чувствительности оказывается выше порога чувствительности к побочному действию психотропных средств. Соответственно затруднено или оказывается невозможным использование терапевтически активных доз психотропных средств из-за раннего выявления и выраженности различных побочных эффектов, риска развития осложнений психофармакотерапии. Следует особо подчеркнуть разнообразие патологических реакций на терапию при эндогенных психозах, развивающихся на органически и соматически измененной почве, значительную частоту неспецифических нарушений, выходящих за рамки известных холинолитических побочных эффектов антидепрессантов и экстрапирамидных проявлений побочного действия нейролептиков. Это прежде всего различные нарушения вегетативной, вегетативно-сосудистой регуляции (тошнота, алгии, парестезии и более сложные телесные сенсации с общим физическим дискомфортом, гиперсаливация, субфебрилитет, озноб или ощущение жара в области лица и прилива крови к голове), а также аллергические реакции (зуд, сыпь, отечность век, лица). Среди неврологических нарушений, наряду с типичными паркинсоноподобными и гиперкинетическими экстрапирамидными расстройствами (в том числе нередко в ответ на применение антидепрессантов, что гакже нельзя отнести к специфическим эффектам), выявляются тики, тремор, атаксия, нарушение координации движений, дизартрия, диплопия, т. е. явления нейротоксического типа. В непосредственной связи с терапевтическими воздействиями психопатологическая структура основного синдрома может усложняться за счет эмоциональной и сенсорной гиперестезии, дисфорического сдвига настроения, тягостных ярких сновидений, затруднений концентрации внимания и других интеллектуально-мнестических нарушений, элементарных сенсорных обманов, расстройств схемы тела и пространственного восприятия, эпизодов дезориентировки, а также генерализованных нарушений, характеризующих изменения уровня бодрствования (типа резкой седации с сонливостью либо ощущением «одурманенности», «опьяненности»). Подобного рода сложные побочные эффекты (по существу смыкающиеся с осложнениями) относительно чаще встречаются при комбинированной психофармакотерапии, что в большинстве случаев делает предпочтительной монотерапию, а при адаптации к избранному препарату или явлениях терапевтической резистентности — последовательную смену курсов монотерапии с использованием различающихся по химической структуре средств либо применение альтернативной терапии. В конечном итоге задача оптимизации терапии состоит не только в достижении безусловно положительного эффекта, но и в минимизации побочных эффектов и риска осложнений, избежать которые особенно трудно при повышенной лекарственной чувствительности и наличии церебральной органической недостаточности.
Возможность возникновения нейротоксических явлений известна и при сочетании карбамазепина с другими лекарственными средствами, прежде всего с солями лития, серотонинергическим антидепрессантом флуоксетином, ингибиторами МАО. К тому же карабамазепин сам по себе не лишен побочных эффектов (в частности преходящей лейкопении, аллергических реакций, сонливости, тошноты, преимущественно в первые дни приема препарата). Однако, как будет показано ниже, рассматриваемое здесь применение карбамазепина (финлепсина) в качестве адъювантного средства принципиально отличается от общепринятых приемов комбинированной терапии, обычно оперирующей сочетанием двух или нескольких препаратов в терапевтически активных дозах. Суточные дозы финлепсина составляли 150-300 мг; в случаях предшествующего систематического профилактического приема препарата его дозы на период активной терапии также снижались до указанных выше. Это диктовалось, во-первых, соображениями безопасности, во-вторых, стремлением избежать чрезмерного седативного эффекта, который может препятствовать достижению собственно терапевтической реакции на тот или иной избранный в качестве основного терапевтического средства препарат. Такого рода «терапия прикрытия» обычно позволяла провести интенсивный курс с применением адекватного состоянию нейролептика или антидепрессанта, избегая осложнений и выраженных побочных эффектов.
Наряду с диссоциированной лекарственной толерантностью определенные трудности в терапии психических расстройств вызывает общая низкая толерантность к психотропным средствам, т. е. относительно соразмерная повышенная чувствительность как к их побочному, так и собственно терапевтическому действию. Чаще всего это имеет отношение к расстройствам невротического уровня — дистимическим, тревожным, психовегетативным, патохарактерологическим, как эндогенной, так и неэндогенной природы. Применение малых или средних доз психотропных средств обычно приводит к достаточно быстрому, но нестойкому улучшению, в то же время попытки увели- чения доз или даже их сохранения на прежнем уровне сопряжены с появлением разнообразных побочных эффектов, включая описанные выше. Кроме того, особенностью реакции на психофармакотерапию является не только объективная выраженность проявлений побочного действия, но и их субъективная непереносимость, что можно связать с астено-гиперестетическими компонентами структуры психопатологических расстройств. При этом обнаруживаются признаки общего повышения чувствительности к любым внешним воздействиям, колебания состояния в зависимости от ситуационно-средовых влияний, что создает особые трудности в поддержании достигнутого улучшения.
Опыт применения финлепсина в малых дозах при наличии такого рода условий терапевтического процесса позволяет говорить о его предпочтительности по сравнению с транквилизаторами, при применении которых компенсация реакций измененной почвы нередко сопровождается снижением собственно терапевтической чувствительности. Разумеется, речь не идет о несомненных преимуществах транквилизаторов при их однократном введении или кратковременном применении для купирования и предупреждения различных вегетативно-сосудистых реакций, особенно симпатикотонической направленности. Непосредственный симптоматический эффект финлепсина в малых дозах, напротив, незначителен. Его положительное действие обеспечивается лишь достаточно продолжительным приемом препарата: в лучшем варианте — при предшествующем активной терапии систематическом профилактическом применении финлепсина либо при его назначении одновременно с началом основного терапевтического курса.
Не всегда столь отчетливы, но в существенной мере подчиняются сходным закономерностям изменения толерантности к терапии в динамике развития и редукции аффективно-бредовых приступов шизофрении и маниакальных фаз аффективных психозов. Целесообразность адъювантного использования финлепсина при нейролептической терапии этих состояний определяется не столько предупреждением экстрапирамидных расстройств, сколько снижением риска неспецифических побочных эффектов нейротоксического типа. Т. е. речь идет скорее о реакциях измененной почвы в условиях низкой толерантности к психотропным средствам. В их предупреждении, по-видимому, реализуются неспецифические вегетостабилизирующие свойства финлепсина.
Ниже приводятся некоторые конкретные данные, касающиеся особенностей действия финлепсина как адъювантного терапевтического средства. Статистический анализ по причинам методического порядка ограничен выбором репрезентативных групп наблюдений, сопоставимых по клинической однородности, а также идентичности основной терапии, но различающихся по наличию или отсутствию финлепсина в терапевтической схеме. В качестве примера в таблице 1 отражены результаты изучения терапевтической динамики циркулярных депрессий (повторных депрессивных фаз). В таблице представлены проявления побочных эффектов, наблюдаемых к концу второй недели активной терапии мелипрамином (с преимущественно парентеральным его введением, в условиях стационара). В первой группе наблюдений мелипрамин применялся в форме монотерапии, во второй группе — в сочетании с финлепсином в дозе 200 мг/сут. Дозы мелипрамина составляли к 14-му дню терапии 125-175 мг/сут, бездостоверных различий между группами (усредненные показатели соответственно145±3,76 мг/сут и 144,7±3,22 мг/сут). Сравниваемые группы не различались по возрасту пациентов (усредненные показатели соответственно 40,0±2,02 г. в первой группе и 41,2±1,74 г. во второй).
Таблица 1.
ЧАСТОТА ПОБОЧНЫХ ЭФФЕКТОВ НА ВТОРОЙ НЕДЕЛЕ ТЕРАПИИ ДЕПРЕССИВНЫХ СОСТОЯНИЙ: 1-я группа наблюдений — монотерапия мелипрамином (М), 2-я группа наблюдений — применение мелипрамина в сочетании с финлепсином (М + Ф).
Эффективность применения Mексидола при судорожном синдроме абстинентного и посттравматического генеза
Опубликовано в журнале:
Бюллетень экспериментальной биологии и медицины, 2006, приложение 1
В.А.Бределев
Архангельская областная клиническая психиатрическая больница
Мексидол является эффективным, экономичным средством для комплексного лечения судорожного синдрома абстинентного генеза, предотвращает рецидив судорожных приступов, достоверно улучшает общее самочувствие и когнитивные функции за более короткий период времени, чем другие ноотропные препараты.
Ключевые слова: абстиненция, травма, судорожный синдром, когнитивные функции, мексидол
В клинической неврологической практике широко используется ноотропный препарат «Мексидол» (оксиметилэтилпиридина сукцинат), относящийся к нейролептическим средствам и транквилизаторам. Мексидол оказывает антиоксидантное, антигипоксическое, мембраностабилизирующее, ноотропное, анксиолитическое, стресспротективное, антиамнестическое, противосудорожное и гиполипидемическое действие. Препарат показан при остром нарушении мозгового кровообращения, дисциркуляторной энцефалопатии, вегетососудистой дистонии, легких когнитивных нарушениях атеросклеротического генеза, тревожных расстройствах при невротических и психоорганических состояниях, абстинентном синдроме при алкоголизме, черепно-мозговой травме, сенильных и атрофических процессах, острой интоксикации антипсихотическими средствами.
МЕТОДИКА ИССЛЕДОВАНИЯ
Клиническое неврологическое обследование проведено на базе наркологических (1-я и 2-я группы) и психиатрических (3-я и 4-я группы) отделений Архангельской областной клинической психиатрической больницы.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Больные с судорожным синдромом абстинентного и посттравматического генеза подбирались без сопутствующих заболеваний. Половой и возрастной состав в сравниваемых группах был одинаковым. Анализ жалоб исследуемых не выявил существенных различий между группами.
Динамика объективных показателей у пациентов с судорожным синдромом абстинентного и травматического генеза после лечения мексидолом (%)
| Показатель | До лечения | После лечения |
| Самочувствие | 41.5 | 43.5 |
| Судорожный синдром | 3.7 | 0 |
| Возбуждение | 37.2 | 24.7 |
| Слуховая память | 4.5 | 5.6 |
| Зрительная память | 8.1 | 9.1 |
| Головная боль | 32.4 | 21.8 |
| Головокружение | 4.2 | 2.4 |
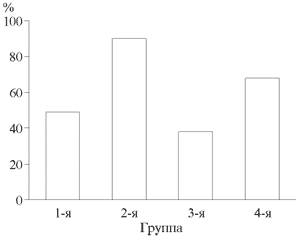
Мексидол является эффективным средством для комплексного лечения судорожного синдрома абстинентного и травматического генеза (рис. 1).
Рис. 1. Эффективность применения мексидола при судорожном синдроме.
Рецидивов судорожного синдрома в основных группах не было, в группах сравнения рецидивы отмечены дважды у травматологических пациентов.
Хорошая переносимость мексидола отмечена у 92-94% больных. Нежелательные эффекты (тошнота, дурнота) не являлись поводом к отмене препарата и купировались после уменьшения суточной дозы мексидола. Клинически доказано преимущественно регредиентное течение многоочаговых расстройств функций головного мозга при терапии мексидолом в сравнении с традиционными ноотропными препаратами (фенибутом, пирацетамом).
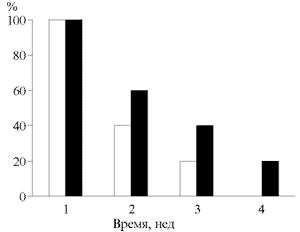
Мексидол достоверно улучшал общее самочувствие, когнитивные функции, уменьшал судорожную готовность и психические симптомы, купировал вегетососудистые нарушения быстрее, чем другие ноотропные препараты (рис. 2).
Рис. 2. Регресс судорожного синдрома абстинентного и посттравматического генеза при терапии мексидолом (светлые столбики) и другими ноотропными препаратами (темные столбики).
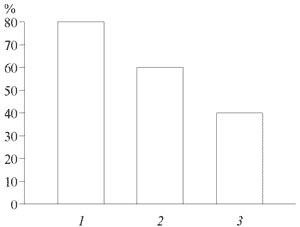
Судорожный синдром и психоневрологические проявления на фоне терапии мексидол+финлепсин значительно регрессировали по сравнению с сочетанием финлепсина и других ноотропных средств (рис. 3).
Рис. 3. Эффективность медикаментозной терапии мексидолом+финлепсином (1), фенибутом+финлепсином (2), пирацетамом+финлепсином (3) при купировании судорожной готовности и психоневрологических патологических проявлений.
Отмечен экономический эффект применения мексидола, позволяющий уменьшить суточную дозировку антиконвульсантов (финлепсин с 600 до 400 мг/сут) и заменить применение других ноотропных базисных средств.
Экономическая и клиническая эффективность ноотропного и противосудорожного препарата мексидола с антиамнестическим и антигипоксическим действием при терапии судорожного синдрома абстинентного и посттравматического генеза позволяет назвать мексидол препаратом выбора при лечении данной актуальной патологии и предупреждения ее прогредиентного инвалидизирующего течения.
Замена одного нейролептика на другой
Смена нейролептика из-за отсутствия эффективности
Смена нейролептика из-за побочных эффектов
Проблема переносимости одна из основных причин смены нейролептика : экстрапирамидные побочные эффекты, не поддающиеся противопаркинсонической терапии ( поздняя дискинезия, постоянные когнитивные нарушения, стойкая седация, нарушения обмена веществ, увеличение QT, другие раздражающие побочные эффекты, например, сексуальная дисфункция.
Следующие побочные эффекты являются наиболее раздражающими для пациентов (или наиболее клинически значимыми для психиатра) : экстрапирамидные симптомы, увеличение веса, когнитивные расстройства, седативный эффект, расстройства, связанные с гиперпролактинемией, сексуальная дисфункция, депрессия, агранулоцитоз и метаболические нарушения. Побочные эффекты являются важной причиной перехода при лечении детей и подростков, где такие эффекты более выражены, чем у взрослых. В этой популяции особенно значительны побочные эффекты, связанные с гиперпролактинемией и увеличением веса.
Другие причины смены нейролептика
Осложнения при смене нейролептика
Как часто меняют один нейролептик на другой
Противопоказания для смены нейролептика
Бег по кругу
Фармакокинетика и фармакодинамика при смене нейролептиков
Антипсихотические препараты метаболизируются в основном в печени системой цитохрома p450, поэтому они могут взаимодействовать с другими лекарственными средствами, которые действуют как ингибиторы их основного метаболического пути или сами являются его субстратами, поскольку может происходить взаимодействие из-за конкурентного ингибирования.
Единственным атипичным антипсихотиком, от которого не ожидается серьезных проблем взаимодействия на уровне цитохрома p450, является палиперидон. Этот препарат продемонстрировал in vitro, что он существенно не ингибирует изоферменты CYP1A2, CYP2A6, CYP2C8 / 9/10, CYP2D6, CYP2E1, CYP3A4 и CYP3A5. Палиперидон также не является субстратом CYP1A2, CYP2A6, CYP2C9 или CYP2C19, и, похоже, CYP2D6 и CYP3A4 лишь минимально участвуют в его метаболизме. например). Можно также также использовать этот путь (например, рисперидон, арипипразол и клозапин) или путь изофермента 1A2 (например, клозапин и оланзапин).
Почти незаменимый клозапин
Смена нейролептиков с аналогичной активностью по отношению к рецепторам
Стратегии преход с одного нейролептика на другой
Традиционно используют три схемы переключения с одного нейролептика на другой. Резкое переключение; немедленное прекращение приема предыдущего антипсихотического средства и начало приема нового нейролептика в обычных дозировках. Поперечное сужение; начало постепенного увеличения дозировки нового нейролептика с одновременным постепенным прекращением приема предыдущего антипсихотического средства. Перекрытие и прерывание; поддержание дозировки предыдущего антипсихотического средства и в то же время постепенное введение нового антипсихотического средства; как только будет достигнута эффективная дозировка нового нейролептика, предыдущий антипсихотик постепенно отменяется.
Какая стратегия перехода лучше
Как менять конкретные нейролептики?
Что делать с негативной симптоматикой?
Как бороться с экстрапирамидной симптоматикой?
По моему мнению, переход на кветиапин значительно улучшает симптомы паркинсонизма и акатизии, но не симптомы поздней дискинезии. И респиридон и оланзапин ослабляют паркинсонизм и позднюю дискинезию, но не акатизию, и не было обнаружено различий между двумя препаратами с точки зрения их воздействия на оцениваемые экстрапирамидные симптомы ( оба препарата вызывают дозозависимые экстрапирамидные побочные эффекты, но респиридон более ). Кроме того, результаты двух метаанализов показывают, что использование противопаркинсонических препаратов значительно меньше связано с кветиапином, чем с рисперидоном, оланзапином и зипразидоном. Другим вариантом переключения у пациентов с поздней дискинезией может быть клозапин, который доказал свою эффективность, несмотря на отсутствие рандомизированных клинических испытаний в этой области, и некоторые авторы считают его лечением выбора в этих случаях.
Сбросить лишний вес
Снизить пролактин
В рандомизированном клиническом исследовании пациентов с шизофренией и гиперпролактинемией, которые лечились рисперидоном или обычными нейролептиками, переход на оланзапин сопровождался возвращением к нормальному уровню пролактина через 4 месяца у 90% пациентов, по сравнению с ни одним из пациентов, которые продолжали принимать предыдущий антипсихотик. Считается, что оланзапин имеет очень небольшую тенденцию вызывать гиперпролактинемию, но краткосрочные клинические испытания на взрослых показали, что уровень пролактина повысился с нормального до повышенного у 30% пациентов, получавших оланзапин, по сравнению с 10% пациентов, получавших плацебо ; у подростков эти показатели были увеличены до 47% и 7% для оланзапина и плацебо соответственно. Согласно метаанализу, оланзапин повышал уровень пролактина несколько больше, чем арипипразол, клозапин и кветиапин. Эти данные позволяют предположить, что оланзапин следует рассматривать как вторичный вариант для замены антипсихотических препаратов у пациентов с гиперпролактинемией.
Зачем нужны сексуальные расстройства
В единственном рандомизированном клиническом исследовании, проведенном на сегодняшний день, пациенты с сексуальной дисфункцией, связанной с терапией рисперидоном, были переведены на кветиапин; Через 6 недель не было значительных различий между пациентами, которые перешли на другой прием, и теми, кто продолжал принимать рисперидон, с точки зрения сексуальной функции. Если оставить в стороне эти обескураживающие результаты, кветиапин и оланзапин являются антипсихотиками, которые оказались наиболее устойчивыми и последовательными, то есть в рандомизированных клинических испытаниях, в отношении более низкой частоты сексуальной дисфункции. Другие авторы обнаружили, что кветиапин, зипразидон и арипипразол были лекарствами, связанными с более низкой частотой сексуальной дисфункции как в целом, так и в большинстве измерений. Таким образом, кветиапин, оланзапин, зипразидон и арипипразол можно считать лучшими вариантами замены антипсихотических препаратов у пациентов с сексуальной дисфункцией.
Смена нейролептика в нашей клинике