Теломеры и фиброз почек
Фиброз почек приводит к почечной недостаточности – заболеванию, которое требует пожизненного диализа. Частота возникновения фиброза растет из-за старения населения. Лабратория Telomeres и Telomerase Group в Испанском Национальном Центре онкологических исследований (Centro Nacional de Investigaciones Oncológicas, CNIO) разрабатывает методы лечения фиброза почек, воздействуя на одну из причин старения – укорочение теломер.
Старение – причина многих болезней. Ранее исследователи предположили, что можно лечить их, воздействуя на связанные со старением процессы, в частности, на укорочение теломер. Им уже удалось вылечить легочный фиброз и инфаркт у мышей путем удлинения теломер. Теперь они сосредоточили внимание на фиброзе почек, так как все данные указывают на то, что укорочение теломер лежит в основе этого заболевания.
Фиброз почек сопровождается чрезмерным рубцеванием почечной ткани, которая замещается фиброзной тканью и теряет свои функции. Подсчитано, что 11% людей старше 65 лет страдают хронической почечной недостаточностью средней тяжести. Согласно результатам исследования, короткие теломеры усиливают в почках процесс эпителиально-мезенхимального перехода (epithelial-to-mesenchymal transition, EMT), который имеет важное значение для регенерации и нормального функционирования организма, а также лежит в основе патологического рубцевания тканей при фиброзе и раке. При всей новизне, открытие не стало неожиданностью, так как было известно, что сверхэкспрессия генов, участвующих в EMT, может приводить к почечному фиброзу.С другой стороны, уже описано, что пациенты с фиброзом почек имеют более короткие теломеры. Поэтому авторы намеренно искали изменения в экспрессии генов, участвующих в EMT у мышей с короткими теломерами и почечным фиброзом.
Группа исследователей создала две мышиные модели фиброза почек, либо сочетая дефицит теломеразы для индуцирования укорочения теломер и пониженное потребление фолиевой кислоты (витамина B9) для ухудшения функции почек, либо блокируя в почках экспрессию белка Trf1, компонента защитного комплекса теломер.
Первая модель продемонстрировала, что одного укорочения теломер недостаточно, чтобы вызвать фиброз почек, и это логично, ведь болезнь не затрагивает 100% пожилых людей. Однако, если мыши с короткими теломерами подвергались воздействию низких доз фолиевой кислоты, у них развивался фиброз почек.
Вторая модель помогла определить, действительно ли теломеры играют причинную роль в фиброзе. Отсутствие белка Trf1, который участвует в регуляции функций теломер, также привел к развитию фиброза почек у мышей.
В качестве еще одной демонстрации роли теломер в развитии фиброза почек авторы культивировали клетки почек с суперэкспрессией гена фермента теломеразы, который удлиняет теломеры. В этих клетках с восстановленными теломерами программа перехода эпителия в мезенхиму нормализовалась, и клетки вернули свой здоровый вид до фиброза.
Поскольку по мере старения теломеры в клетках организма укорачиваются, можно предположить, что патологические программы EMT, активные при раке и различных типах тканевого фиброза, могут быть запущены, по крайней мере частично, наличием коротких теломер.
Эпигенетическая регуляция фиброза почек при диабетической нефропатии: в фокусе – модификации гистонов
1 Научно-исследовательский институт молекулярной биологии и медицины при Национальном центре кардиологии
и терапии МЗ КР; Бишкек, Киргизия;
2 Кыргызская государственная медицинская академия им. И.К. Ахунбаева; Бишкек, Киргизия;
3 Национальный центр кардиологии и терапии им. акад. Мирсаида Миррахимова при МЗ КР; Бишкек, Киргизия;
4 Центр семейной медицины № 7; Бишкек, Киргизия;
5 ФГБОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова»; Москва, Россия
Одной из наиболее распространенных причин развития терминальной стадии почечной недостаточности является диабетическая нефропатия (ДН). Фиброз почек, характеризующийся накоплением белков внеклеточного матрикса (ВКМ) в клубочковых базальных мембранах и тубулоинтерстиции, служит конечным проявлением ДН. Сигнальный путь TGF-β (Transforming growth factor beta) запускает эпителиально-мезенхимальный переход (ЭMП), который играет ключевую роль в накоплении ВКМ-белков при ДН. В исследованиях показано, что, несмотря на гликемический контроль, ДН продолжает прогрессировать. Это явление получило название «метаболическая память» и означает, что эпигенетические факторы, в частности модификации гистонов, изменяют экспрессию генов фиброза почек и белков ВКМ, индуцированную TGF-β1, а также участвуют в почечном фиброзе благодаря своим свойствам регулировать процесс ЭМП, вызванный сигналами TGF-β. В связи с этим в настоящее время исследователи предпринимают усилия по разработке агентов, влияющих на модификацию гистонов, с целью задержки, остановки или даже обратного развития ДН. В этом обзоре мы изложим результаты самых последних исследований по регулированию гистоновых модификаций, вовлеченных в патогенез ДН.
Введение
В последние годы заболеваемость хронической болезнью почек растет угрожающими темпами. Если эта тенденция сохранится, то не только у бедных, но даже и у богатых стран не хватит ресурсов для адекватного лечения этого заболевания [1]. Хотя почка обладает способностью к регенерации и восстановлению после острого и хронического повреждения, часто патологический процесс приобретает необратимый характер, что приводит к кратковременному почечному коллапсу, требующему диализа или почечной трансплантации [2]. В целом через 10–15 лет после постановки диагноза прогрессирующей нефропатии у 30–40% людей развивается значительная почечная недостаточность [3]. По оценкам, в настоящее время от 1 до 2 млн человек лечат заместительной почечной терапией (ЗПТ) [3–5], причем более 90% этих пациентов живут в развитых странах, т.к. доступность ЗПТ в развивающихся странах ограничена, а в слаборазвитых странах невелика или отсутствует вследствие того, что ЗПТ представляет собой дорогостоящую нагрузку на национальные бюджеты здравоохранения [3].
Одной из основных причин развития почечной недостаточности является диабетическая нефропатия (ДН), которая развивается примерно у 20–40% пациентов с диабетом [6]. Точная причина ДН неизвестна, однако установлено, что ее развитию способствуют высокий уровень глюкозы в крови, дислипидемия, артериальная гипертензия и протеинурия [7]. Все это стимулирует продукцию различных факторов роста/цитокинов и активных форм кислорода (АФК), которые вызывают повреждение подоцитов и воспаление интерстиция. В результате этих событий происходит избыточное осаждение белков внеклеточного матрикса (ВКМ) и развитие гломерулосклероза, что в конечном итоге приводит к дисфункции клубочков и почечной недостаточности [7, 8].
Фиброз почек при ДН характеризуется непрерывным осаждением ВКМ-белков – коллагена, фибронектина и ламинина в мезангиальном матриксе, клубочковых базальных мембранах и тубулоинтерстиции [9]. Известно, что даже после контроля гипергликемии у пациентов с диабетом может продолжаться развитие клубочкового и тубулоинтерстициального фиброза [10]. Эти данные свидетельствуют о том, что эпигенетика может играть существенную роль в патобиологии ДН [11].
Роль фиброза почек при ДН
Избыточное накопление ВКМ-белков является отличительной чертой ДН [9, 12]. Это подтверждается наблюдениями, демонстрирующими осаждение в повышенных количествах коллагенов, фибронектина и ламинина в клубочковой базальной мембране и мезангиальном ВКМ уже на ранних стадиях ДН (микроальбуминурия), что приводит к развитию диабетического диффузного гломерулосклероза [9, 13–15]. На стадиях выраженной нефропатии осаждение коллагенов I и III типов сильно возрастает [16, 17]. Кроме того, продемонстрировано повышение содержания коллагена IV типа в сыворотке и моче на ранних и поздних стадиях ДН [18–20]. Таким образом, накопление белков ВКМ при ДН происходит на протяжении всего процесса почечного фиброза.
TGF-β1 (Transforming growth factor beta), цитокин широкого спектра действия [21, 22], индуцируемый гипергликемией, конечными продуктами усиленного гликозилирования, митоген-активируемой протеинкиназой и протеинкиназой C [23], играет решающую роль в прогрессировании гипертрофии клубочков и избыточном осаждении матричных белков при ДН [24, 25]. Индуцируемое гиперликемией увеличение осаждения матричных белков, приводящее к гломерулосклерозу, связано с повышенной экспрессией и активацией TGF-β1 в клубочковых клетках, подоцитах [26] и мезангиальных клетках [27]. Кроме того, TGF-β1 может также стимулировать действие альфа-актин гладких мышц (α-SMA – α-smooth muscle actin), экспрессию коллагена I типа и гипертрофию клеток [28, 29]. Другой цитокин, фактор роста соединительной ткани CTGF (connective tissue growth factor), также является весьма важным профибротическим фактором роста, участвующим как в TGF-β-зависимых, так и в TGF-β-независимых фибротических процессах [30–32]. Было показано, что профибротическое действие TGF-β1 может быть блокировано антисмысловыми олигонуклеотидами CTGF [33]. Также установлено, что активация CTGF может увеличивать экспрессию фибронектина и коллагенов IV, III и I, а также способствовать осаждению и скоплению белков ВКМ [34, 35].
По сообщениям, активированные миофибробласты – это основные эффекторные клетки при ДН, а их число коррелирует с избыточным осаждением белков ВКМ [36]. Однако точные механизмы их возникновения и активации в фиброзных почках остаются неясными. Исследования P. Galichon и А. Hertig [37] показали, что в процессе почечного фиброза миофибробласты могут возникать из трубчатых эпителиальных клеток через эпителиально-мезенхимальный переход (ЭМП). Обычно принято считать, что трансформация нарушенных трубчатых эпителиальных клеток в мезенхимальные является наиболее вероятным механизмом, связанным с развитием фиброза при ДН [36]. Как in vitro-, так и in vivo-исследования показали, что ЭМП может быть инициирован рядом агентов, стимулирующих процессы, в которых основным участником яв.
Фиброз почек
Фиброз почек — что это такое? Ответ на данный вопрос интересует пациентов, которые впервые столкнулись с таким редким диагнозом. Современная медицина постоянно развивается, но все еще до конца не изучила данную патологию. Впервые недуг был научно описан врачом Ормондом, и с тех пор носил его имя.
Фиброз почек нельзя считать самостоятельным заболеванием, а только осложнением, протекающим на фоне сильного инфекционного воспалительного процесса. При прогрессировании фиброзных нарушений части органа расширяются, моча не может нормально выходить, и у пациента очень быстро может развиться почечная недостаточность.

Данное заболевание принято классифицировать на несколько категорий. Недуг может быть:
Медики все еще не могут точно определить причины развития фиброза почек. На этот счет существует несколько версий, но большинство специалистов склоняются именно к воспалительной гипотезе. Воспаление в близлежащих к почке органах инфекционного типа – главный провоцирующий фактор. Чаще всего такое заболевание диагностируется у пациентов с пиелонефритом, туберкулезом костей, хроническими патологиями ЖКТ, эндометритом или венерическими заболеваниями.
Некоторые специалисты утверждают, что фиброз может развиваться после сильной механической травмы или после химиотерапии онкологии.
Фиброз почек имеет свои особенности. Чаще эта патология поражает представителей сильного пола, в возрасте 30-50 лет. Нередко врачи обнаруживают образование фиброзных узлов одновременно на обеих почках.
Развивается недуг в несколько этапов. Сначала прогрессирует воспалительный процесс, который распространяется на почки. Паренхима постепенно сменяется соединительной тканью, а затем начинает морщиться и сжиматься. При этом функционирование почек сильно нарушается, уплотненная ткань сдавливает мочевые каналы, и урина не может нормально выходить из организма. Кровообращение в органе также нарушается из-за сдавливания сосудов, развиваются ишемические процессы.
Симптомы
На начальном этапе по симптоматике распознать заболевание практически невозможно. Оно длительное время может вообще никак не проявляться. Постепенно у пациента появляется тупая боль и неприятные ощущения в пояснице, которые возникают периодически.
Вторая стадия фиброза почек сопровождается серьезными нарушениями фильтрационных функций, и, как следствие, интоксикацией организма. На этом этапе у пациента возникает следующая симптоматика.
Если заболевание не начать лечить своевременно, он перейдет в запущенную фазу. При этом у пациента развиваются серьезные нарушения работы сердечно-сосудистой системы, ЖКТ, дыхания, вплоть до отека легких.
Методы диагностики
Из-за отсутствия характерной симптоматики фиброз почек своевременно обнаружить практически невозможно. Как правило, недуг диагностируется на поздней стадии или обнаруживается случайно, во время комплексного обследования организма пациента.
Чтобы медик мог поставить точный диагноз, больному нужно сдать урину и кровь для лабораторного исследования (общего и биохимического). Дополнительно назначается УЗИ почек, КТ или МРТ. Врач во время такого осмотра может изучить состояние внутренних органов, и выявить наличие каких-либо отклонений. Чтобы изучить работоспособность почек, проводится сцинтиграфия или экскреторная урография.
Лечение
Лечение фиброза почек подбирается индивидуально для каждого пациента, и зависит от того, на какой стадии было выявлено заболевание. Рассмотрим несколько наиболее распространенных методик.
В ежедневном рационе больного не должно быть слишком острой, жирной и соленой пищи. Также рекомендуется отказаться от копченостей, консервации. Обязательно следите за своим питьевым режимом. Чем больше вы пьете жидкости, тем быстрее устраняется воспаление, и нормализуется процесс мочевыведения.
Операция
Если фиброз почек приводит к нарушению функционирования органа, пациенту назначается хирургическая операция. Медицинский специалист удаляет пораженную патологией часть мочеточника, и устанавливает искусственную трубку или отрезок собственной тонкой кишки пациента. Также во время оперативного вмешательства может образовываться новая оболочка вокруг мочевого канала.
Такое радикальное лечение требует длительного восстановления и реабилитации. Пациенту назначается курс гормональных препаратов и антибиотиков. Чтобы новые фиброзные узлы не образовывались, нужно принимать кортикостероиды. Для оценки состояния почек нужно проходить комплексное обследование не реже 1 раза в 6 месяцев.
Прогноз и профилактика
Из-за того, что причины фиброза почек так до конца и не выяснены, никакой профилактики этого заболевания не существует. В определенной степени обезопасить себя от развития патологии можно при помощи своевременного лечения и защиты от инфекционных недугов, повышения иммунной защиты. Медики рекомендуют всем вести здоровый образ жизни, избегать вредных пристрастий, и ответственно относиться к своему здоровью.
Точный прогноз развития фиброза почек может составить только лечащий врач, в соответствии с индивидуальными особенностями организма пациента. Здесь многое зависит от наличия сопутствующих патологий, возраста и пр. консервативные методы терапии позволяют добиться только временного улучшения состояния. Чтобы навсегда забыть о недуге, необходимо проведение операции.
Однако никто не может полностью исключить развитие рецидива. Если моча будет выводиться неправильно, у пациента будет развиваться интоксикация организма, повышение давления и почечная недостаточность. Отсутствие своевременных экстренных мер нередко приводит к сепсису и летальному исходу. Тот же финал ждет пациентов с почечной недостаточностью. Своевременная диагностика и постановка точного диагноза крайне важна, и позволяет добиться желаемого эффекта почти в 60% случаев.
Доброкачественные и злокачественные опухоли почки
Рак почки
Впервые подробно рак почки был описан P.Gravitz в 1883 г. Вследствие внешнего сходства опухоли с тканью надпочечника, раньше для обозначения рака почки часто употреблялся термин «гипернефроидный рак», или «гипернефрома». В современной медицинской литературе чаще всего используется понятие «почечно-клеточный рак».
Рак почки занимает третье место среди всех новообразований органов мочевой системы, при этом опухоль почки составляет около 3% всех новообразований, диагностируемых у взрослого человека. Заболеваемость раком почки в среднем составляет 4 человека на 100000 населения. В последнее время отмечен рост заболеваемости раком почки, который объясняется не только повышением качества диагностики, но и истинным ростом числа заболевших. Заболеваемость почечно-клеточным раком зависит от возраста и достигает максимума к 70 годам. Мужчины страдают данным заболеванием в два раза чаще, чем женщины. Пик заболеваемости приходится на возраст 40 – 60 лет. В структуре смертности населения от онкологических заболеваний рак почки среди мужчин составляет 2,7%, среди женщин – 2,1%.
Рак почки – причины
Наличие совокупности ожирения и артериальной гипертензии у курящих лиц достоверно повышает риск развития почечно-клеточного рака почти на 50%. Роль факторов питания, профессиональных вредностей и генетических альтераций активно изучается.
Унификация классификации болезни необходима для сравнения результатов лечения заболевания, а также для определения его прогноза. Двумя наиболее известными и широко используемыми классификациями рака почки являются TNM классификация и классификация Robson, которая более распространена в США.
Сегодня в России используется классификация TNM, предложенная Международным противораковым союзом (International union against cancer (UICC)). Применение данной системы стадирования дает возможность проводить адекватное сравнение результатов лечения в разных медицинских центрах, а также сопоставлять данные научных и клинических исследований. Классификация применима только для рака почечной паренхимы. При использовании этой классификации обязательно гистологическое подтверждение диагноза.
Для оценки категорий T, N и M применяются следующие методы: физикальный осмотр и различные методики медицинской визуализации.
TNM – клиническая классификация почечно-клеточного рака
T – первичная опухоль
Tx – недостаточно данных для оценки первичной опухоли
T0 – первичная опухоль не определяется
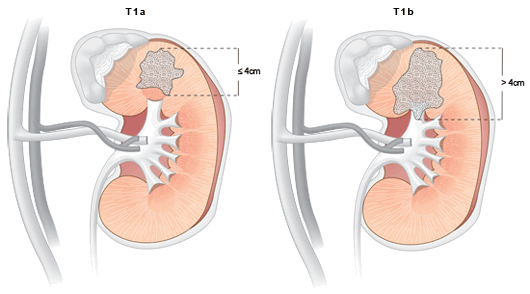
T1 – опухоль до 7 см в наибольшем измерении, ограниченная почкой
T1a – опухоль менее 4 см
T1b – опухоль более 4, но менее 7 см
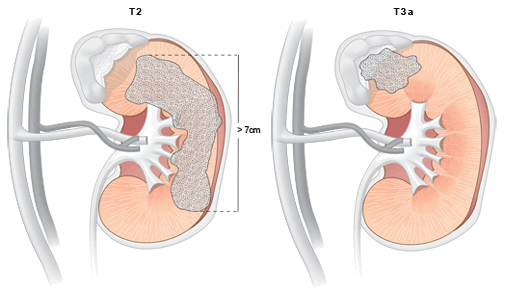
T2 – опухоль более 7 см в наибольшем измерении, ограниченная почкой
T3 – опухоль распространяется на крупные вены или надпочечники или околопочечные ткани (включая жировую ткань почечного синуса), но в пределах фасции Герота
T3a – опухоль распространяется на надпочечники или околопочечные ткани, но в пределах фасции Герота
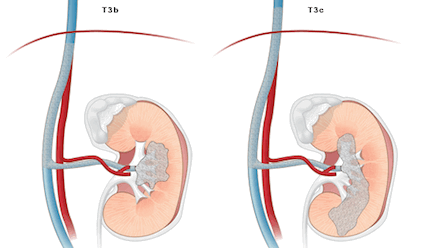
T3b – инвазия опухоли в почечную (включая сегментарные (с мышечной стенкой) ветви) или полую вены до диафрагмы
T3c – распространение опухоли на полую вену выше диафрагмы
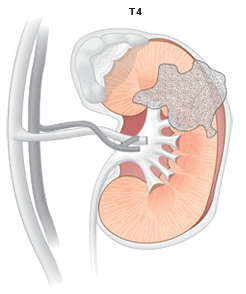
T4 – опухоль распространяется за пределы фасции Герота.
N – регионарные лимфатические узлы
Nx – недостаточно данных для оценки состояния регионарных лимфатических узлов
N0 – нет признаков поражения метастазами регионарных лимфатических узлов
N1 – имеются метастазы в одиночном регионарном лимфатическом узле
N2 – множественные метастазы в регионарных лимфатических узлах
М – отдаленные метастазы
Mx – отдаленные метастазы не могут быть оценены
M0 – нет отдаленных метастазов
M1 – отдаленные метастазы
G – степень дифференцировки опухоли.
G – гистопатологическая дифференцировка
Gx – степень дифференцировки не может быть оценена
G1 – высокодифференцированная опухоль
G2 – умеренно-дифференцированная опухоль
G3-4 – низкодифференцированная/недифференцированная опухоль
Существуют также классификации рака почки на основе его гистологической структуры. Согласно ее выделяют: светлоклеточный, хромофильный, папиллярный, хромофобный и нейроэндокринный рак, а также онкоцитому и рак из протоков Беллини.
Опухоль почки может иметь в своей структуре массивные зоны некроза и кровоизлияния, т.е. при визуализации может иммитироваться полостная структура. Кроме того, возможно изначально самостоятельное развитие опухоли почки в стенке кисты (кистозная форма рака почки). С внедрением современных систем медицинской визуализации (МСКТ, МРТ), сформулировано множество дополнительных критериев, характеризующих кистозные образования почек. Для их систематизации в практической деятельности используется классификация, предложенная Bosniak М.А. (1986):
Типичная картина одиночной (солитарной) кисты почки с четкими ровными контурами, внутренние структуры отсутствуют.
Киста имеет диаметр не более 30 мм, в ее структуре отмечаются одна или две перегородки с толщиной не более 1 мм; могут быть единичные кальцинаты в стенках или перегородках; или киста имеет более плотное содержимое вследствие повышенного содержания в кистозной жидкости белка или крови. Накопление контрастного вещества элементами образования отсутствует.
Жидкостное образование с толстыми стенками неоднородной структуры, возможно увеличение плотности после внутривенного контрастирования; отмечается неравномерная их кальцификация; единичные пристеночные дополнительные структуры; мультилокулярные кисты.
Неоднородные по составу кистозные структуры с необычно толстыми, накапливающими контрастный препарат стенками, имеющие дополнительные солидные включения.
При кистозном образовании с характеристиками III и IV группы необходимо исключать рак почки. По результатам научных исследований около 40% кист, имеющих признаки III группы, в итоге были представлены злокачественными новообразованиями.
Доброкачественные опухоли почки
Самыми частовстречаемыми и наиболее значимыми для клинической практики доброкачественными опухолями почек являются ангиомиолипомы. Причины их появления и развития во многом остаются неясными. Однако, возникновение данного вида опухолей часто ассоциировано с имеющейся наследственной патологией, называемой туберозным склерозом.
Ангиомиолипомы составляют примерно 0,3% от всех объемных образований почек. Женщины болеют в 2,5 раза чаще мужчин. В 13–30% случаев ангиомиолипомы носят множественный характер, а у 15% больных бывает двустороннее поражение. Размеры опухолевого узла могут составлять от 5–7 мм до 20 см и более.
Гистологически данная доброкачественная опухоль почки обычно представлена зрелой жировой тканью, кровеносными сосудами и гладкомышечными структурами в различных пропорциях.
Несмотря на то, что ангиомиолипомы обычно четко отграничены и растут, раздвигая и сдавливая окружающие ткани, известны случаи их роста, как в направлении лоханки, так и с прорастанием почечной капсулы и околопочечной клетчатки. Метастазирования при типичной ангиомиолипоме не бывает. По данным научной литературы, известны всего три наблюдения развития саркомы почки на фоне ангиомиолипомы, однако имеются описания случаев развития рака почки на фоне ангиомиолипомы как параллельного процесса.
Солитарная фиброзная опухоль при клиническом обследовании может быть ошибочно принята за почечноклеточную карциному или саркому почки, так как имеет большие размеры, сходные рентгенологические признаки и часто сопровождается «безболевой» макрогематурией – примесью крови в моче.
К числу редких доброкачественных опухолей почки принадлежат также метанефрогенная аденома и метанефрогенная аденофиброма.
Наиболее распространенными доброкачественными новообразованиями почек эпителиального генеза являются онкоцитома и папиллярная аденома. Однако, они составляют всего 5% от общего числа всех опухолей почки.
Опухоль почки – симптомы
В настоящее время многими учеными отмечается бессимптомность течения данного заболевания. По видимому, это связано, в первую очередь, с улучшением диагностики, широкому внедрению ультразвукового сканирования, которое является основным скрининг-методом в выявлении многих патологических процессов.
Выделяют местные и общие симптомы раковой опухоли почки. К местным симптомам относятся:
Боль в поясничной области
Боль в поясничной области. Причиной ее является прорастание опухолью фиброзной капсулы почки, компрессия сосудов почечной ножки с нарушением кровообращения в органе, а также структур чашечно-лоханочной системы, что приводит к нарушению уродинамики. Кроме того, опухоль в процессе своего роста инвазирует околопочечную клетчатку, мышцы и соседние органы, что также может являться причиной болевого синдрома. Интенсивность боли варьирует в довольно широком диапазоне. Может носить постоянный характер.
Определяется при локализации опухоли в нижнем сегменте почки. Имеет плотную консистенцию, подвижность определяется степенью распространения на окружающие органы. Также может пальпироваться неизмененный нижний сегмент почки при отдавливании последней вниз объемным образованием, локализующимся в ее верхнем сегменте.
При появлении примеси крови в моче необходимо срочно обратиться к врачу. Возникнув однажды, гематурия может прекратиться сама и возникнуть снова через достаточно продолжительный промежуток времени. Пациент успокаивается и откладывает свой визит к врачу. Но болезнь продолжает развиваться! Помните об этом!
Данная группа симптомов ранее обозначалась как «классическая» триада. При одновременном наличии всех ее компонентов, как правило, имела место одна из поздних стадий заболевания. В настоящее время встречается редко.
Группа общих (другое название – экстраренальных) симптомов опухоли почки включает в себя следующие:
Повышение температуры тела
Является наиболее частым неспецифическим признаком наличия опухолевого процесса. Как правило, лихорадка носит субфебрильный характер (диапазон Т тела от нормальной до 37,9 С), длительная, постоянная. Причиной ее является постоянное попадание в кровь продуктов жизнедеятельности и распада опухолевых клеток.
Данный симптом регистрируется примерно у пятой части пациентов с опухолью почки. Причина кроется в нарушении кровообращения в пораженном органе в результате компрессии почечных сосудов разрастающейся опухолью, что в свою очередь запускает каскад ренин-ангиотензиновой системы. Как правило, плохо поддается лечению стандартными препаратами.
Потеря аппетита, похудание, слабость являются неспецифическими проявлениями опухоли почки, но часто наиболее ранними и порой единственными.
При обнаружении у себя одного из вышеуказанных признаков показано срочное обращение к врачу. Я буду искренне рад, если выясниться, что Ваша повышенная утомляемость или потеря аппетита обусловлены всего лишь кратковременным стрессом на работе.
Опухоль почки – диагностика
Современный алгоритм обследования пациента с подозрением на опухоль почки включает в себя следующие основные пункты:
На сегодняшний день является общедоступным, массовым, неинвазивным и безвредным методом обследования. Позволяет визуализировать опухоль, уточнить ее размеры, локализацию, отношение к основным структурам почки и окружающим тканям. Кроме того, в режиме цветного допплеровского картирования позволяет оценить параметры кровотока в опухолевом узле, состояние почечных сосудов, в частности почечной вены для исключения наличия в ней признаков опухолевого тромбоза.
Компьютерная томография (КТ)
Компьютерная томография (КТ). В настоящий момент является основным диагностическим и визуализирующим методом при опухоли почки. По возможности, цеелесообразно выполнять исследование на мультиспиральном томографе (МСКТ). Данная методика позволяет получать срезы с шагом до 1 мм, за счет количества и скорости оборота детекторов появляется возможность качественного выполнения сосудистой фазы исследования. Кроме того, имеется возможность получать изображения высокого качества в режимах 3D-реконструкции и мультипланарной реформации, что важно для детальной визуализации всех аспектов патологического процесса и тщательного планирования предстоящего лечения. Исследование, при отсутствии противопоказаний, должно быть выполнено с внутривенным контрастированием. Противопоказаниями являются хроническая почечная недостаточность, аллергия на йодсодержащие контрастные препараты.
Магнитно-резонансная томография (МРТ)
Является методом выбора у пациентов при наличии противопоказаний для МСКТ с контрастированием, а также уточняющей методикой в сложных диагностических случаях, когда МСКТ не дает однозначной трактовки полученных результатов, в том числе при наличии образований почки с жидкостным компонентом и при подозрении на ангиомиолипому. Исследование целесообразно выполнять с контрастированием. Йод в контрастных препаратах для МРТ отсутствует.
Позволяет выяснить функциональное состояние почек. Это важно в свете планирования оперативного лечения и предварительной оценки резервных возможностей здоровой почки в случае выполнения нефрэктомии.
Используется для поиска костных метастазов при подозрении на их наличие.
Рентгенография органов грудной клетки или компьютерная томография легких
Позволяет исключить наличие метастатического поражения легких.
Хирургическое вмешательство до настоящего времени остается основным и единственным радикальным методом лечения локализованного и местнораспространенного рака почки. В случае удовлетворительного функционального состояния здоровой почки, операцией выбора в большинстве случаев является радикальная нефрэктомия (удаление почки), которая предполагает при ее выполнении обязательное соблюдение следующих принципов:
В настоящее время видеоэндоскопические методики получили широкое применение в хирургии. Многолетний опыт показал преимущества видеоэндоскопического лечения многих заболеваний перед традиционным открытым способом. В настоящий момент происходит широкое внедрение этой технологии при выполнении операций по поводу объемных образований почек.
Предоперационная подготовка не отличается от таковой при открытых операциях. Более подробно ее основные этапы изложены на отдельной странице.
При накоплении достаточного опыта время операции при лапароскопической нефрэктомии соответствует времени открытой операции сопоставимого объема при значительно меньшей травматичности эндоскопического доступа. Потребность в наркотических анальгетиках практически отсутствует, а при оценке качества жизни в послеоперационном периоде лапароскопическая нефрэктомия имеет значительное преимущество по сравнению со стандартным пособием.
Онкологические результаты операций у пациентов, пролеченных лапароскопическим доступом, полностью сопоставимы с результатами открытых операций. Общая и специфическая 5-ти летняя выживаемость пациентов составляет около 98 и 81% соответственно.
Дискутабельным остается вопрос — с какой стадией онкопроцесса в почке может быть оперирован пациент лапароскопическим доступом? По мнению большинства хирургов это больные со стадией процесса T1-2N0. Собственный опыт позволяет констатировать успешность лечение в подавляющем большинстве случаев у пациентов со стадией опухоли почки pT3a.
Лапароскопическая резекция почки
Значительно реже лапароскопический метод применяется при выполнении органосберегающих операций при опухоли почки. Опубликованные в последние годы исследования отдаленных результатов показали, что при выполнении органосохраняющей операции по поводу рака почки в пределах здоровых тканей, 5-летняя онкоспецифическая выживаемость составляет 78-90,5% против 66-79% при радикальной нефрэктомии.
Актуальным остается вопрос: «Какова оптимальная тактика при локализованном (pT1a, pT1b и pT2 стадии), а также местнораспространенном (pT3a стадия) раке почки и сохранном противоположном органе?» Полностью поддерживаю принципы, сформулированные академиком Н.А. Лопаткиным : «При технической возможности, достаточной функциональной значимости оставшейся части паренхимы и эффективной чашечно-лоханочной системе, целесообразно выполнение резекции почки даже при интактной контралатеральной почке. Данное вмешательство является не менее радикальным, чем нефрэктомия». Для хирурга важно осознание того, что «лишних» органов у человека не бывает.
Резекция почки, каким бы доступом она не выполнялась (лапароскопическим или открытым) может быть проведена по абсолютным, относительным или элективным показаниям, сформулированным член-корр. РАМН, профессором Аляевым Ю.Г.
Абсолютные показания к органосохраняющей операции при опухоли почки:
Относительные показания к органосохраняющей операции:
Элективным показанием является ситуация, когда противоположная почка сохранна, а новообразование монофокальное и имеет стадию pT1bNoMo.
Органосохраняющая операция не показана если противоположная почка сохранна, а новообразование мультифокальное или монофокальное в стадии pT1bNoMo и размер его больше 4 см, а также при отсутствии техничекой возжности осуществления ее в пределах здоровых тканей.
В качестве одного из аргументов сторонники органосохраняющих операций приводят тот факт, что качество жизни пациентов выше после органосохраняющих операций нежели после органоуносящих.
И так, удаление почки или ее резекция в сочетании с преимуществами лапароскопического доступа? Решение вопроса требует индивидуального подхода и строго персонифицированного решения.