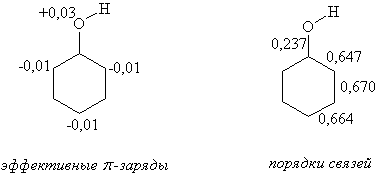
Фенолы более сильные кислоты чем алифатические спирты потому что
О полярности фенолов позволяют судить величины дипольных моментов.
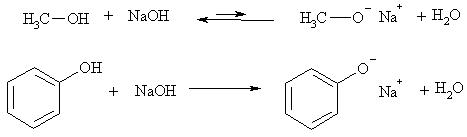
Следствие повышенной кислотности фенола – реакция со щелочами, в которую не вступают алифатические спирты. Однако фенол более слабая кислота, чем карбоновые кислоты и угольная кислота, поэтому он, в отличие от них, не реагирует с раствором гидрокарбоната натрия. Это простейший тест на различие спиртов, фенолов и карбоновых кислот.
Заместители в бензольном кольце фенолов влияют на кислотность следующим образом: электроноакцепторные заместители повышают, а электронодонорные понижают кислотность. Наибольшее влияние оказывают заместители, расположенные в орто— и пара-положениях кольца относительно гидроксила. Так, нитрогруппа (электроноакцептор), расположенная в орто— или пара-положениях, участвует в делокализации отрицательного заряда, стабилизируя тем самым фенолят- анион.
С увеличением числа нитрогрупп кислотность фенолов повышается до такой степени, что 2,4,6-тринитрофенол (рКа 0,42) по силе приближается к минеральным кислотам. По этой причине тринитрофенол называют пикриновой кислотой
Таблица. Значения рКа некоторых спиртов и фенолов.
Фенолы можно рассматривать в качестве оснований по причине наличия на атоме кислорода двух несвязывающих электронных пар. По сравнению со спиртами основные свойства фенола ослаблены из-за сопряжения фенольного гидроксила с бензольным кольцом.
Фенолы более сильные кислоты чем алифатические спирты потому что
Фенолы превращаются в соли под действием водных растворов щелочей, но не водных растворов бикарбонатов. При действии водных минеральных кислот, карбоновых кислот или угольной кислоты из солей получаются свободные фенолы
Из этого следует, что фенолы — значительно более сильные кислоты, чем вода, но гораздо более слабые кислоты, чем карбоновые кислоты. Большинство фенолов имеют 


Хотя фенолы значительно слабее карбоновых кислот, они несравненно более сильные кислоты, чем спирты, для которых 

Рассмотрим структуры реагентов и продуктов при ионизации спиртов и фенолов. Как спирт, так и алкоголят-ион могут быть удовлетворительно представлены единственной структурой. Фенол и фенолят-ион содержат бензольное кольцо и поэтому должны быть гибридами структур Кекуле I и II, III и IV соответственно. Этот резонанс предположительно стабилизует и молекулу, и ион в одинаковой степени. Его влияние снижает энергию образования как молекулы, так и иона на одинаковую величину и тем самым не влияет на разность в энергиях их образования, т. е. не влияет на 
Поэтому, если не рассматривать другие факторы, то следовало бы ожидать, что фенол будет иметь такую же кислотность, как и спирт.
Однако необходимо учитывать также дополнительные структуры. Поскольку кислород является основным атомом, он может обобществлять более чем одну пару электронов с кольцом; это учитывается вкладом структур V—VII для фенола и VIII—X для фенолят-иона.
Рассмотрим теперь, будут ли вклады этих двух рядов структур одинаково существенными. Структуры V—VII для фенола несут как положительный, так и отрицательный заряд; структуры VIII—X для фенолят-иона несут лишь отрицательный заряд.
Рис. 25.1. Структура молекулы и положение равновесия. Фенол дает резонансно-стабилизованный анион и является более сильной кислотой, чем спирт.
Поскольку для разделения противоположных зарядов необходимо затратить энергию, то структуры для фенола богаче энергией и, следовательно, менее устойчивы, чем структуры для фенолят-иона. (Мы уж 

Как было показано в разд. 23.3, ароматические амины — более слабые основания, чем алифатические амины, поскольку резонанс стабилизует свободный амин в большей степени, чем соответствующий ион. В рассматриваемом случае мы встречаемся с обратной ситуацией: фенолы являются более сильными кислотами, чем их алифатические аналоги — спирты, поскольку резонанс стабилизует фенолят-ион в большей степени, чем свободный фенол. (В действительности, резонанс с участием кольца оказывает одинаковое влияние в обоих случаях: он стабилизует и таким образом ослабляет основание — амин или фенолят-ион.)
Анализ производных фенолов, хинонов, ароматических кислот
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Глава 9. Анализ производных фенолов, хинонов, ароматических кислот, фенолокислот, ароматических аминокислот и их производных
ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА ГРУППЫ ФЕНОЛОВ
Фенолы можно рассматривать как ароматические спирты, у которых одна или несколько гидроксильных групп связаны непосредственно с ароматическим ядром. Этим обусловлены главные отличия фенолов от алифатических спиртов.
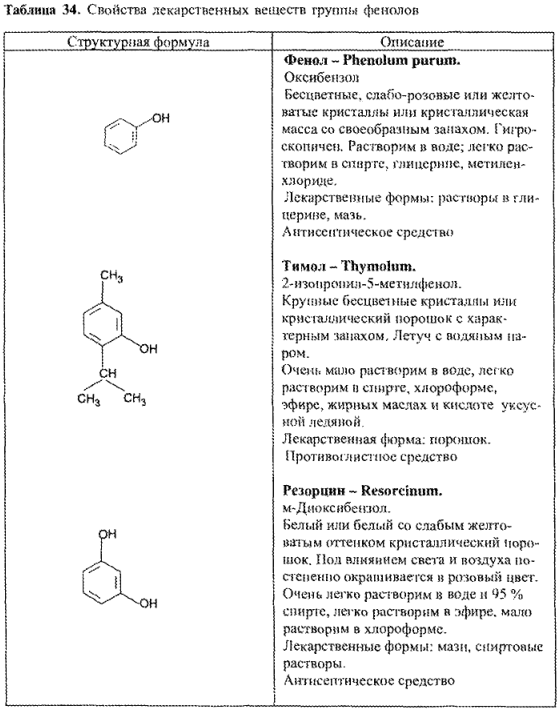
Простые фенолы, т.е. вещества, не содержащие в молекуле никаких функциональных групп, кроме ароматического ядра и одного или более фенольных гидроксилов (оксибензол, резорцин, тимол), применяют в качестве антисептических средств. Среди лекарственных веществ гомологом фенола (оксибензола) является –тимол. К производным фенолов (по химической классификации) можно отнести синтетические аналоги эстрогенов нестероидной структуры – гексэстрол (синэстрол), диэтилстильбэстрол. Один или несколько фенольных гидроксилов содержатся в лекарственных веществах как природного, так и синтетического происхождения с различным фармакологическим действием (морфина гидрохлорид, рутозид, синэстрол. Пиридоксина гидрохлорид и др.).
Общие свойства лекарственных веществ группы фенолов приведены в табл. 34.
Химические свойства и анализ качества
Фенолы проявляют значительно большую кислотность, чем спирты и вода, однако они слабее угольной и карбоновых кислот, не окрашивают лакмус.
Значения рКа следующие: фенол — 9,89, уксусная кислота – 4,76, угольная кислота — 6,12.
Кислотность определяется наличием в структуре фенольного гидроксила и образованием соответствующего аниона:
Чем стабильнее анион, тем сильнее кислота.
Внутри данной группы кислотность различна и зависит от заместителей, количества гидроксильных групп.
Фенолы хорошо растворяются в водных растворах щелочей с образованием фенолятов, однако данную реакцию нельзя использовать для количественного определения из-за гидролиза образующейся соли.
Фенолы не взаимодействуют с гидрокарбонатами щелочных металлов, потому что слабее угольной кислоты и не могут вытеснять ее. По реакции взаимодействия с гидрокарбонатами щелочных металлов различаются фенолы и карбоновые кислоты.
Характерной качественной реакцией на фенолы является образование окрашенных комплексов [Fe(OR)6] 3- с солями трехвалентного железа. Окраска зависит от количества гидроксильных групп, их расположения, наличия других функциональных групп (табл. 35).
Комплекс неустойчив, разрушается при действии на него органических и минеральных кислот.
Реакция используется, кроме определения подлинности, и при анализе чистоты. Так, примесь пирокатехина в резорцине определяется по реакции осаждения с ацетатом свинца, а примесь фенола в тимоле — по окраске с железа (III) хлоридом.
Образование сложных эфиров
При фармацевтическом качественном и количественном анализе часто используются реакции ацетилирования. Образующийся сложный эфир идентифицируется по характерной Тпл:
Количественное определение синэстрола и диэтилстильбэстрола проводится методом ацетилирования.
Восстановительные свойства
Фенолы легко окисляются лаже кислородом воздуха, поэтому при их хранении возможно появление оттенков (розового, желтого, бурого).
Двухатомные фенолы окисляются быстрее, чем одноатомные. Скорость окисления зависит также от pH среды, В щелочной среде окисление идет быстрее. Вследствие легкости окисления фармакопея вводит показатель: цветность.
Реакция окисления фенолов протекает сложно, и характер продуктов во многом зависит от природы заместителей.
Схему окисления фенола можно представить таким образом:
Резорцин окисляется с образованием сложной смеси продуктов, но без м-хинонов.
На способности препаратов окисляться основана такая реакция подлинности, как индофеноловая проба. В качестве окислителя используют хлорную известь, хлорамин, бромную воду:
Образующийся индофенол амфотерного характера и может образовывать хорошо диссоциируемые соли как с кислотами, так и с основаниями. Соли имеют различную окраску (табл. 36):
Реакции идут легко, если о- и n-положения не заняты.
Реакции электрофильного замещения
Гидроксильная группа, связанная с ароматическим ядром, 8 щелочном растворе – сильнейший орто- и пара-ориентант. В связи с этим для фенолов легко проходят реакции галогенирования, нит- розирования, нитрования и др.
Бромирование и йодирование широко применяются при анализе фенолов. Образование трибромфенола в виде осадка используется для подтверждения подлинности фенола:
При избытке бромной воды образуется желтого цвета 2,4,4,6- тетра-бромциклогексадиен-2,5-он:
Наиболее легко идет галогенирование фенолов в щелочной среде, но в сильнощелочной среде происходит окисление фенола. Резорцин бронируется в кислой среде, образуя трибромрезорцин, который в воде растворим. Если одно из положений занято (как у тимола), образуется дибромпроизводное:
Реакции галогенирования используются также для количественного определения фенолов.
Нитрозирование (нитрозореакция Либермана)
Реакция нитрозирования является разновидностью индофеноловой реакции:
Нитрозогруппа усиливает подвижность водорода у фенольного гидроксила, происходит изомеризация. Образующийся хиноноксим конденсируется с фенолом:
Данные об окраске образующихся при нитрозореакции Либермана индофенолов представлены в табл. 37.
Фенолы нитруются кислотой азотной, разбавленной при комнатной температуре, с образованием о- и n-нитрофенола:
Добавление раствора натрия гидроксида усиливает окраску вследствие образования хорошо диссоциируемой соли:
Реакция сочетания фенолов с солью диазония в щелочной среде
Фенолы легко вступают в реакцию замещения с солями диазония в щелочной среде с образованием азокрасителей, имеющих в указанной среде окраску от оранжевой до вишнево-красной:
Это общая реакция на фенолы, не имеющие заместителей в орто- и пара-положении. Легче сочетание происходит в пара-положении из-за образования длинной цепи сопряженных связей.
Соль диазония из-за нестойкости готовят непосредственно перед проведением реакции, используя соединения с первичной ароматической аминогруппой:
При образовании азокрасителя pH среды не должна быть выше 9,0—10,0, так как в сильнощелочной среде соль диазония образует не способный к азосочетаиию диазогидрат:
Реакции окисления и конденсации
Эти реакции широко используются в анализе для подтверждения подлинности как открытого, так и заблокированного фенольного гидроксила.
Образование арилметановых красителей происходит при конденсации фенолов с альдегидами, ангидридами кислот, кетонами:
Для тимола предлагается реакция конденсации с хлороформом в щелочной среде. Продукт реакции окрашен в красно-фиолетовый цвет:
Для фенолов со свободным п-положением характерна реакция конденсации с 2,6-дихлорхинонхлоримидом, при этом образуется индофенол:
Образование производного индофенола возможно при нитровании тимола в среде уксусного ангидрида и концентрированной серной кислоты:
Часто используются реакции конденсации фенолов с лактонами (фталевый ангидрид). С фенолом продукт конденсации называется фенолфталеином и используется как индикатор, имеющий в щелочной среде малиновую окраску:
С тимолом образуется тимолфталеин
индикатор, окрашенный в щелочной среде в синий цвет:
Резорцин сплавляют в фарфоровом тигле с избытком фталевого ангидрида в присутствии нескольких капель концентрированной Н2SО4. Полученный плав желто-красного цвета после охлаждения выливают в разбавленный раствор щелочи. Появляется интенсивно-зеленая флюоресценция образующегося в результате реакции флюоресценна:
Анализ чистоты
В резорцине определяют примесь пирокатехина по реакции с аммония молибдатом. При наличии примеси появляется окраска, интенсивность которой сравнивают с эталонной.
Другая примесь в препарате резорцина – фенол. Примесь фенола определяют по запаху, для этого препарат с небольшим количеством воды нагревают на водяной бане при температуре 40—50 °С.
В тимоле определяют примесь фенола по реакции с железа (III) хлоридом. По условию методики ГФ концентрация тимола вследствие малой его растворимости составляет 0,085 %. Окраска комплекса тимола с железа хлоридом при такой концентрации не воспринимается, а при наличии примеси фенола появляется фиолетовая окраска. Примесь фенола в препарате недопустима.
Количественное определение
Для количественного определения фенолов используется броматометрия: как прямой (тимол), гак и обратный (фенол, резорнин, синэстрол) способ, В склянку с притертой пробкой помещают препарат, избыток титрованного раствора калия бромата и калия бромида. Подкисляют серной кислотой:
Выделившийся в результате реакции бром идет на галогенирование фенола:
Реакция протекает в течение 10—15 мин; на это время склянку оставляют в темном месте. Затем к смеси прибавляют раствор калия иодида и оставляют еще на 5 мин:
Прямое, титрование принято ГФ для количественного определения тимола. В прямом титровании избыточная капля йода изменяет окраску индикаторов (метилового оранжевого, метилового красного), В обратном титровании выделившийся йод оттитровывают раствором тиосульфата натрия. Индикатор — крахмал.
Следует помнить, что на процесс бромирования влияют условия определения: длительность реакции, концентрация кислоты.
Молярная масса эквивалентов, обозначаемая как М(1/z) следующая:
В обратном способе обязательно проводят контрольный опыт.
Ацетилирование применяется для количественного определения синэстрола и диэтилстильбэстрола, Навеску препарата помещают в колбу с избытком уксусного ангидрида и нагревают в течение 45 мин в присутствии пиридина (реакцию — см, выше). Затем в реакционную среду добавляют воду, непрореагировавший уксусный ангидрид гидролизуется. Уксусную кислоту оттитровывают стандартным раствором натрия гидроксида:
Проводят контрольный опыт, М(1/z)= ½ М препарата.
Спирты и фенолы
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Классификация спиртов
По числу гидроксильных групп:
Двухатомные спирты с двумя и тремя гидроксогруппами у одного атома углерода R‒CH(OH)2 или R-C(OH)3 неустойчивы, от них легко отрывается вода и образуется карбонильное соединение.
Классификация по числу углеводородных радикалов у атома углерода при гидроксильной группе
Классификация по строению углеводородного радикала
Непредельные спирты, в которых гидроксильная группа соединена с атомом углерода при двойной связи (алкенолы), неустойчивы и изомеризуются в соответствующие карбонильные соединения.
Строение спиртов и фенолов
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому спирты – жидкости с относительно высокой температурой кипения (температура кипения метанола +64,5 о С). Температуры кипения многоатомных спиртов и фенолов значительно выше.
Таблица. Температуры кипения некоторых спиртов и фенола.
| Название вещества | Температура кипения |
| Метанол | 64 |
| Этанол | 78 |
| Пропанол-1 | 92 |
| Бутанол-1 | 118 |
| Этиленгликоль | 196 |
| Фенол | 181,8 |
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Низшие спирты (метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин) смешиваются с водой в любых соотношениях.
Номенклатура спиртов
Нумерация ведется от ближайшего к ОН-группе конца цепи.

Например: СН3ОН – метиловый спирт, С2Н5ОН – этиловый спирт и т.д.
Например, пропандиол-1,2 (пропиленгликоль):
Изомерия спиртов
Структурная изомерия
Для спиртов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета характерна для спиртов, которые содержат не менее четырех атомов углерода.
| Например. Ф ормуле С4Н9ОН соответствуют четыре структурных изомера, из них два различаются строением углеродного скелета |
| Бутанол-1 | 2-Метилпропанол-1 |
 |  |
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С2Н6О этиловый спирт СН3–CH2–OH и диметиловый эфир CH3–O–CH3 |
| Этиловый спирт | Диметиловый эфир |
| СН3–CH2–OH | CH3–O–CH3 |
Изомеры с различным положением группы ОН отличаются положением гидроксильной группы в молекуле. Такая изомерия характерна для спиртов, которые содержат три или больше атомов углерода.
| Например. Пропанол-1 и пропанол-2 |
| Пропанол-1 | Пропанол-2 |
 |  |
Химические свойства спиртов
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н + соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
| Таким образом, для спиртов характерны следующие свойства: 1. Кислотные свойства
1.1. Взаимодействие с раствором щелочейПри взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой. Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому спирты не взаимодействуют с растворами щелочей. Многоатомные спирты также не реагируют с растворами щелочей. 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)Спирты взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты. Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
Многоатомные спирты также реагируют с активными металлами: 1.3. Взаимодействие с гидроксидом меди (II)Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли (качественная реакция на многоатомные спирты).
2. Реакции замещения группы ОН2.1. Взаимодействие с галогеноводородамиПри взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
|