Тенофовир и энтекавир – наиболее эффективные антивирусные средства
при хроническом гепатите В
Tenofovir and Entecavir are Most Effective Antiviral Agents for Chronic Hepatitis B; A Systematic Review and Bayesian Meta-Analyses
Woo G, Tomlinson G, Nishikawa Y, Kowgier M, Sherman M, Wong DK, Pham B, Ungar WJ, Einarson TR, Heathcote EJ, Krahn M
Опубликовано: Gastroenterology. 2010 Jun 20.
В рандомизированных исследованиях (РИ) до сих пор не изучалась относительная эффективность лицензированных противовирусных средств у лиц с хроническим гепатитом В (ХГВ) без лечения. В настоящем исследовании изучили относительную эффективность в течение первых 12 месяцев лечения ХГВ. Используемыми лекарствами были ламивудин, пегинтерферон, аденовир, энтекавир, телбивудин и тенофовир в качестве монотерапии или комбинированной терапии у ранее не леченных больных. Базы данных исследованы на РИ терапии в первые 12 месяцев у HBeAg-позитивных и/или негативных лиц с ХГВ в Англии с 31 октября 2009. У HBeAg-позитивных пациентов тенофовир оказался наиболее эффективным в индуцировании неопределяемых уровней ДНК ВГВ (вероятность 88%), нормализации АЛТ (66%), HBeAg сероконверсии (20%) и элиминации HBsAg (5%); он оказался третьим в улучшении гистологической картины печени (53%). Энтекавир оказался наиболее эффективным в улучшении гистологии печени (56%), вторым в индуцировании неопределяемых уровней ДНК ВГВ (61%) и нормализации уровней АЛТ (70%), и третьим в элиминации HBsAg (1%). У HBeAg-негативных пациентов, тенофовир оказался наиболее эффективным в индуцировании неопределяемых уровней ДНК ВГВ (94%) и улучшении гистологии печени (65%); он оказался вторым по нормализации уровня АЛТ (73%). В течение первого года лечения ХГВ, тенофовир и энтекавир оказались наиболее эффективными оральными агентами для HBeAg-позитивных пациентов; тенофовир наиболее эффективен у HBeAg-негативных пациентов.
Подготовил Р. Ханвердиев,




Copyright © 2008 
Энтекавир или тенофовир что лучше
Межрегиональная общественная организация
содействия пациентам с вирусными гепатитами
Наши партнеры
Горячая линия правовой помощи
По будням с 13:00-17:00 мск.
Горячая линия по раку печени
По будням с 10:00-19:00 мск.
Записаться к врачу
в Московской области
Горячая линия для онкобольных
Горячая линия Росздравнадзора
Горячая линия Роспотребнадзора
Сразу два исследования, представленных на Международном конгрессе по заболеваниям печени в Вене, возможно, указывают, что среди людей, получающих тенофовир, реже развивается рак печени, чем среди пациентов на терапии энтекавиром.
Согласно исследованию, проведенному в Китайском университете Гонконга, люди, которые проходят лечение гепатита B с применением энтекавира, больше рискуют заболеть раком печени, чем пациенты, принимающие тенофовира дизопроксил фумарат (TDF) или тенофовира алафинамид фумарат (TAF).
Ученые проанализировали данные по пациентам всех гонконгских государственных больниц и клиник за 10-летний период. Недостающие данные заменялись методом множественного восстановления. Затем ученые использовали вариант "взвешивания" метода псевдорандомизации для уравновешивания клинических характеристик между двумя группами пациентов.
В общей сложности было выделено 29 350 пациентов. Средний возраст составлял 53 года, около 60% были мужчинами. Свыше 95% начинали лечение гепатита B с препарата энтекавир. На медианном сроке наблюдения 6 лет рак печени развился у 8 пациентов (0,6%), получавших тенофовир, по сравнению с 1 386 пациентами (4,9%) на энтекавире. 5-летняя кумулятивная заболеваемость раком печени составляла 7% в группе пациентов на энтекавире против 1,1% в группе пациентов на тенофовире.
Кроме того, на Конгрессе был представлен абстракт группы южнокорейских ученых, которые также пришли к выводу, что рак печени реже развивается среди пациентов на тенофовире, чем среди пациентов на энтекавире.
Дор указывает на еще одно исследование, представленное на Конгрессе, которое показало, что риск развития рака печени у пациентов, получающих терапию энтекавиром или тенофовиром, может различаться в зависимости от расы. Так, этот риск был ниже среди пациентов азиатской расы, что согласуется с выводами китайских и корейских ученых.
Риск развития гепатоцеллюлярной карциномы на фоне тенофовира и энтекавира у больных гепатитом В
Актуальность
Гепатит В является одной из распространенных инфекций во всем мире.
В лечении инфекции активно используют тенофовир и энтекавир. В ранее проводимых исследованиях, сравнивающих препараты в отношении риска развитая гепатоцеллюлярной карциномы, получены противоречивые результаты.
С целью обобщить результаты выполненных ранее исследований проведен систематический обзор и мета-анализ.
Методы
Выполнен поиск исследований, в которых оценивали риск развития гепатоцеллюлярной карциномы после лечения у пациентов с хроническим гепатитом В. Пациенты получали терапию энтекавиром или тенофовиром. Наблюдение за пациентами продолжали на протяжении как минимум 1 года.
Поиск исследований проводили в базах данных PubMed, Embase, Web of Science и Cochrane library (публикации с 2006 по апрель 2020 года).
Результаты
Заключение
Согласно результатам систематического обзора и мета-анализа не найдено достоверных различий между тенофовиром и энтекавиром в отношении заболеваемости гепатоцеллюлярной карциномой у больных с хроническим гепатитом В.
Источник: Cheng-Hao Tseng, Yao-Chun Hsu, Tzu-Haw Chen, Fanpu Ji, I-Sung Chen, Ying-Nan Tsai, et al. Hepatocellular carcinoma incidence with tenofovir versus entecavir in chronic hepatitis B: a systematic review and meta-analysis. The Lancet Gastroenterology and Hepatology. September 2020.
Безопасность и приверженность длительной терапии нуклеозидными и нуклеотидными аналогами у больных хроническим гепатитом В
Изучение безопасности и приверженности длительной терапии нуклеозид(т)ными аналогами хронического гепатита В (ХГВ)
Материалы и методы
В исследование включены 101 больной ХГВ, которые получали лечение тенофовиром, энтекавиром или телбивудином в течение не менее трех лет. Оценивали динамику сывороточного уровня креатинина и расчетной скорости клубочковой фильтрации (СКФ), активности креатинфосфокиназы (КФК), другие нежелательные явления, а также приверженность к терапии.
При лечении тенофовиром в течение 5 лет отмечено увеличение креатинина сыворотки в среднем на 14 мкмоль/л (на 12,2%) и снижение СКФ в среднем на 12,3 мл/мин (на 13,5%). При лечении телбивудином в течение 8 лет СКФ увеличилась в среднем на 6,2 мл/мин (на 5,9%), а при лечении энтекавиром в течение 8 лет она практически не изменилась. У 5 (21,7%) пациентов, принимавших телбивудин, наблюдалось выраженное повышение активности КФК с клиническими признаками миопатии, у 3 из них терапия была прекращена. При лечении энтекавиром и тенофовиром клинически значимых изменений КФК и развития миопатии не отмечено. Частота “сохранения на терапии” при лечении телбивудином была ниже (48% к 8 году лечения), чем при применении тенофовира (72% к 5 году лечения) и энтекавира (89% к 8 году лечения). Хорошая приверженность к лечению при приеме энтекавира (91%) и тенофовира (92%) отмечалась чаще, чем при приеме телбивудина (70%)
Энтекавир и тенофовир – наиболее безопасные препараты при длитель- ном лечении ХГВ и характеризуется высоким уровнем “сохранения на терапии” и приверженности. При длительном лечении тенофовиром необходим контроль функции почек.
Вмире около 260 млн человек страдают хроническим гепатитом В (ХГВ) [1]. В России заболеваемость ХГВ достигает 12,6 на 100 тыс населения, а число больных составляет от 3 до 5 млн [2]. В настоящее время для лечения ХГВ применяют пегилированный интерферон-α или аналоги нуклеозидов и нуклеотидов (АН), главным образом, энтекавир, тенофовир дизопроксил фумарат, тенофовир алафенамид и реже телбивудин 4. В последние годы чаще применяют АН, которые подавляют репликацию вируса, что, как правило, сопровождается нормализацией активности печеночных ферментов и улучшением гистологической картины печени (в том числе, регрессом фиброза) [5]. Лечение ХГВ предполагает длительный прием АН (не менее 3–5 лет), а в некоторых случаях, в частности, при циррозе печени, может потребоваться и пожизненное лечение, что определяет актуаль ность оценки безопасности и приверженности к терапии 8. Низкая приверженность снижает эффективность лечения, увеличивает риск осложнений, а также способствует селекции резистентных штаммов вируса 11.
Целью исследования было изучение безопасности и приверженности длительной терапии АН.
Материалы и методы
Для оценки безопасности терапии, наряду с опросом и осмотром, каждые 6 мес оценивали активность аминотрансфераз, креатинфосфокиназы (КФК) и сывороточный уровень креатинина. Для оценки почечной безопасности определяли скорость клубочковой фильтрации (СКФ) по формуле Cockcroft-Gault (в мл/мин).
На основании анкетирования и подсчета количества таблеток проводились оценка нежелательных явлений, приверженности пациентов к лечению и "сохранение на терапии". Анкетирование осуществлялось каждые 3-6 месяцев при встрече с пациентом или во время телефонного звонка. Приверженность к лечению оценивали на основании количества пропусков приемов препарата за один месяц (0-1 – хорошая; 2-3 – удовлетворительная; более 3 – плохая). "Сохранение на терапии" определяли как % от числа пациентов, продолжавших лечение исходно назначенным препаратом.
Статистический анализ был выполнен с использованием программы MedCalc (версия 11.2, 2011 MedCalcSoftwareb vba, Ostend, Belgium). Для определения различий количественных показателей между группами использовали ранговые тесты Манна-Уитни, Крускала-Уоллиса или критерий Джонкхиера-Терпстры. Оценка приверженности к лечению проводилась по результатам U-теста Манна-Уитни при сравнении медианы наблюдений количества принятых таблеток в группе каждого препарата за 3 месяца. Оценка мощности производилась методом Монте-Карло. Средние значения креатинина сыворотки и СКФ представлены как медиана и интерквартильный диапазон (IQR).
Результаты
За период с 2008 по 2017 г. 101 больной ХГВ получал противовирусную терапию АН в течение не менее трех лет (максимально в течение 9 лет). У 12 пациентов было отмечено развитие резистентности к препарату, а один АН был заменен на другой, поэтому число наблюдений составило 113. В 65 случаях пациенты принимали энтекавир в дозе 0,5 мг/сут, в 25 – тенофовир дизопроксил фумарат в дозе 300 мг/сут и в 23 – телбивудин в дозе 600 мг/сут. Исходная характеристика пациентов приведена в (табл. 1).
| Показатели | Тенофовир (n=25) | Энтекавир (n=65) | Телбивудин (n=23) | Всего (n=113) |
|---|---|---|---|---|
| Возраст, годы | 43±13 | 44±14 | 35±12 | 42±14 |
| Мужчины, n (%) | 21 (84) | 45 (69) | 4 (17) | 85 (75) |
| Масса тела, кг | 75±13 | 76±15 | 77±13 | 76±14 |
| Цирроз, n (%) | 5 (20%) | 5 (8%) | 0 | 10 (9%) |
| АСТ, МЕ/мл | 75±53 | 93±75 | 79±34 | 86±64 |
| АЛТ, МЕ/мл | 121±83 | 100±69 | 110±52 | 108±70 |
| Длит. лечения, мес | 43±10 | 68±28 | 64±31 | 61±30 |
Почечная безопасность. Сывороточ ный уровень креатинина при лечении энтекавиром, телбивудином и тенофовиром оставался в пределах референсных значений на протяжении всего периода лечения. При лечении тенофовиром он увеличился в среднем на 14,0 мкмоль/л (7,0;27,0) за 5 лет (p=0,0034), или на 12,2% (8,0;27,5) от исходного (рис. 1).
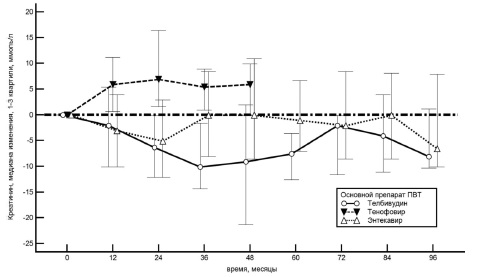
Увеличение сывороточного уровня креатинина на 10% и более от исходного наблюдалось у 17 (68%) пациентов, от 5 до 10% – у 6 (24%). При лечении энтекавиром сывороточный уровень креа тинина снизился в среднем на 6,6 мкмоль/л (-10,1;7,9) к 8-му году лечения, или на 7,5% (–11,5;8,2) от исходного. Увеличение уровня креатинина на 10% и более от исходного отмечено у 11 (17%) пациентов, от 5 до 10% – у 10 (15%). При лечении телбивудином сывороточный уровень креатинина снизился на 8,1 мкмоль/л (-10,4;1,4) к 8-му году лечения, или на 9,8% (-11,6;1,5). Увеличение сывороточного уровня креатинина сыворотки от 5 до 10% от исходного наблюдалось у 3 (13%) пациентов. Случаев более значительного повышения сывороточного уровня креатинина не было.
| Степень повышения КФК | n=23 |
|---|---|
| 1 (до 3 норм) | 6(26,1) |
| 2 (от 4 до 7 норм) | 3 (13,0) |
| 3 (от 8 до 10 норм | 2 (8,7) |
| 4 (более 10 норм) | 1 (4,4) |
При лечении тенофовиром СКФ в среднем снизилась на 12,3 мл/мин (–21,8;–6,8) к 5-му году (p=0,008), или на 13,5% (–24,0;–7,5) (рис. 2). У 4 (16%) пациентов наблюдалось снижение СКФ на 15% и более от исходной. При лечении телбивудином СКФ в среднем увеличилась на 6,2 мл/мин (-7,3;19,7) к 8-му году (p=0,023), или на 5,9% от исходной. При лечении энтекавиром СКФ практически не изменилась (+0,2 мл/мин; –5,8;+15,2) к 8-му году, что составило +0,21% (–6,1;16,0).
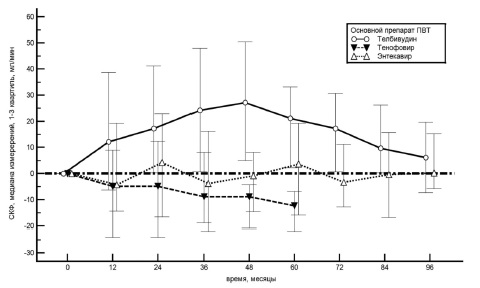
Другие нежелательные явления. Большинство нежелательных явлений в ходе терапии АН были легкими или умеренно выраженными и транзиторными (табл. 3). Наиболее частые нежелательные явления, которые, вероятно, были связаны с АН, включали повышение активности АЛТ и/или АСТ (19,8%), головную боль (9,8%), тошноту (20,7%) и астенический синдром (13,8%). Повышение активности АЛТ и/или АСТ за весь период наблюдения отмечено в 20 (19,8%) случаях в среднем через 13±5 мес терапии. При этом, у 8 пациентов повышение активности АЛТ и/или АСТ было преходящим, у 12 пациентов было обусловлено разви тием резистентности к препарату и рецидивом гепатита В (2 пациента исходно получали энтекавир и 10 – телбивудин). Во всех случаях развития резистентности и вирусологического прорыва терапия была изменена (10 пациентов начали прием тенофовира и 2 – прием энтекавира).
| Нежелательные явления | Тенофовир (n=25) | Энтекавир (n=65 | Телбивудин (n=23) | Всего (n=113) |
|---|---|---|---|---|
| Миалгия | 5 (21,7) | 0 | 0 | 5(4,9) |
| Новообразования | 1 (4,3) | 1 (1,5) | 0 | 2 (1,9) |
| Дискомфорт и боль в правом подреберье | 2 (8,7) | 2 (3,0) | 1 (4,0) | 5 (4,9) |
| Тошнота | 6 (23,0) | 12 (18,4) | 3 (12,0) | 21 (20,7) |
| Головная боль | 12 (52,1) | 5 (7,6) | 3 (12,0) | 20 (19,8) |
| Повышение АЛТ и/или АСТ | 12 (52,1) | 6 (9,2) | 2 (8,0) | 20 (19,8) |
| Желудочно-кишечные нарушения | 1 (4,3) | 1 (1,5) | 1 (4,0) | 3 (2,9) |
| Астенический синдром | 5 (21,7) | 5 (7,7) | 4 (16,0) | 14 (13,8) |
| Смерть | 1 (4,3) | 1 (1,5) | 0 | 2 (1,9) |
Два (1,9%) пациента умерли. Один случай смерти не был связан с гепатитом В и лечением, у второго пациента без цирроза печени, достигшего авиремии, причиной смерти было гепатоцеллюлярная карцинома.
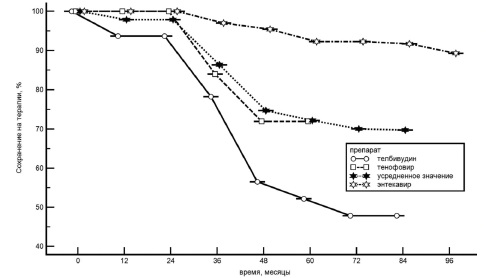
Лечение телбивудином прекратили 12 (52,1%) из 23 пациентов. К 8-му году лечения частота "сохранения на терапии" составила 47,9%. Причинами прекращения лечения были неэффективность (вирусологический прорыв) в 8 случаях, неэффективность лечения и развитие миопатии одновременно в 2, развитие миопатии в 1, немедицинские показания в 1. Лечение энтекавиром прекратили 7 (10,7%) пациентов, а частота "сохранения на терапии" в течение 8 лет составила 89,3%. Два пациента прекратили лечение вследствие его неэффективности (вирусологический прорыв), трое – по причине, не связанной с препаратом или заболеванием, и двое – умерли. Лечение тенофовиром прекратили 6 (24,0%) пациентов (во всех случаях по причине, не связанной с препаратом или заболеванием), а частота "сохранения на терапии" в течение 5 лет составила 76,0%. При этом, в первые 3 года все пациенты продолжали лечение энтекавиром и тенофовиром. Всего 10 пациентов самостоятельно (не по медицинским показаниям) прекратили лечение АН, 1 (4,3%) из них получал телбивудин, 3 (4,6%) – энтекавир и 6 (24%) – тенофовир. Причинами прекращения лечения оказались отсутствие возможности покупать препарат (n=7) и планирование беременности (n=3).
Приверженность к терапии. При лечении энтекавиром хорошая приверженность к терапии (>97%) отмечена у 59 (91%) пациентов, удовлетворительная (90-97%) – у 2 (3%) и плохая (
Обсуждение
Лечение АН, как правило, безопасно и хорошо переносится. В редких случаях, особенно у больных с декомпенсированным поражением печени, возможно развитие тяжелой миопатии, невропатии, почечной недостаточности и лактат-ацидоза вследствие повреждения митохондриальной ДНК [14]. В нашем исследовании ни у одного пациента не отмечено развитие этого тяжелого и часто фатального осложнения. Среди других нежелательных явлений АН описаны поражение почек, мышц и костной ткани.
Известно, что у больных ХГВ, особенно на стадии цирроза печени, чаще, чем в популяции, встречается нарушение функции почек. В одном исследовании СКФ у 20% больных ХГВ до начала терапии составляла 60-89 мл/мин/1,73 м2 [15]. В связи с этим, вопросы почечной безопасности при лечении АН приобретают особую актуальность. При лечении тенофовиром встречается поражение почек (включая синдром Фанкони) и костей (остеопения и остеопороз) вследствие тубулопатии [16,17]. В одной из работ показано, что терапия тенофовиром в течение 2 лет сопровождается уменьшением СКФ в среднем на 4,8 мл/мин, при этом у 18% пациентов отмечено снижение СКФ на 25% и более, а у 1,2% – ниже 50 мл/мин [18]. В исследовании Wu и соавт. СКФ при лечении тенофовиром в течение 3 лет снизилась в среднем на 6,5 мл/мин [22]. Мы также отметили снижение СКФ (в среднем на 12,3 мл/мин) и повышение уровня креатинина сыворотки (в среднем на 14 мкмоль/л) при лечении тенофовиром в течение 5 лет. У 16% пациентов наблюдалось снижение СКФ на 15% и более и лишь у 1 (4%) – на 25% от исходного. Ни у одного пациента не отмечено снижения СКФ менее 50 мл/мин. В связи с небольшим количеством пациентов (n=25) мы не выявили статистически достоверных факторов риска снижения СКФ при лечении тенофовиром. В литературе факторами риска повреждения почек при лечении тенофовиром считают наличие сахарного диабета, низкую концентрация витамина D в крови и исходное заболевание почек. Поэтому в настоящее время у пациентов с исходными признаками или факторами риска повреждения почек рекомендуется применять энтекавир или новую форму тенофовира (тенофовир алафенамид) [19]. Мы не обнаружили статистически достоверного изменения уровня креатинина сыворотки (–6,6 мкмоль/л) и СКФ (+0,2 мл/мин) при лечении энтекавиром в течение 8 лет. В исследовании Wu и соавт. также не отмечено клинически значимого изменения СКФ (в среднем +2,0 мл/мин/1,73м2) при лечении энтекавиром в течение 3 лет [22].
В нашем исследовании при лечении телбивудином (в среднем в течение 5 лет) наблюдалось снижение сывороточного уровня креатинина (в среднем на 8,1 мкмоль/л) и увеличение СКФ (в среднем на 6,2 мл/мин). Другие авторы также отмечают улучшение показателей азотовыделительной функции почек при лечении телбивудином, механизм которого остается неясным [20]. В частности в исследовании GLOBE показано, что СКФ увеличилась в среднем на 8,5% от исходной при лечении телбивудином в течение 2 лет. Более значительное повышение СКФ отмечено у пациентов с исходными факторами риска почечного повреждения: исходная СКФ в пределах 60-89 мл/мин/1,73 м2 (на 17,2%), возраст старше 50 лет (на 11,4%), компенсированный (на 7,2%) и декомпенсированный цирроз печени (на 2,0%) [21]. Могут ли эти данные рассматриваться как основание для применения телбивудина у больных с исходным нарушением функции почек или факторами риска ее развития остается неясным, особенно с учетом более высокой частоты развития резистентности при длительном приеме телбивудина по сравнению с энтекавиром и тенофовиром.
В нашем исследовании у 52% пациентов, получавших телбивудин, наблюдалось повышение активности КФК в среднем через 19±3 мес от начала лечения. У 5 (21,7%) пациентов отмечены признаки миопатии (боли и слабость в мышцах), а у 3 из них – прогрессирование поражения мышц. В работе Zou и соавт. незначительное повышение активности КФК (
Заключение
Длительная терапия энтекавиром и тенофовиром безопасна и характеризуется высокой частотой "сохранения на терапии" и хорошей приверженностью к лечению. При длительной терапии тенофовиром необходим мониторинг функции почек. Лечение телбивудином ассоциируется с высокой частотой преждевременного прекращения терапии вследствие развития резистентности к препарату и поражения мышц. Плохая приверженность к лечению телбивудином наблюдалась у лиц молодого возраста и сопровождалась более высоким риском неэффективности терапии.
Опубликовано в журнале:
Клинические перспективы гастроэнтерологии, гепатологии № 2, 2007
М.В. Маевская, А.О. Буеверов (Московская медицинская академия им. И.М. Сеченова)
Данные, приведенные в статье, были получены в исследовании оригинального препарата энтекавира (Бараклюд ® ). Применение несертифицированных противовирусных средств может угрожать вашему здоровью, привести к возникновению мутантных штаммов вируса гепатита В и неэффективности дальнейшей терапии.
Ключевые слова: хронический гепатит В, резистентность HBV, лечение, энтекавир, ламивудин.
M.V. Mayevskaya, А.О. Buyeverov
Keywords: chronic hepatitis B, HBV resistance, treatment, entecavir, lamivudine.
Вирус гепатита В (ВГ В, или HBV) открыт в 1965 г. Однако его активное изучение пришлось на 80-90-е годы, когда было доказано, что эта форма инфекции может приобретать хроническое течение и вызывать такие тяжелые формы повреждения, как цирроз печени (ЦП) и гепатоцеллюлярная карцинома (ГЦК). С разработкой вакцины против этого вируса появилась надежда на быстрое решение данной проблемы.
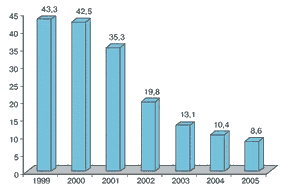
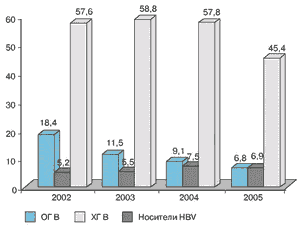
Действительно, заболеваемость острым гепатитом В (ОГ В) в нашей стране снижается с каждым годом (рис.1). Однако количество больных хронической формой инфекции и носителей HBV не уменьшается (рис. 2), что определяет актуальность этой проблемы в России [2].
Рис. 1. Заболеваемость острым гепатитом В в РФ в 1999-2005 гг., поданным официальной регистрации, на 100 000 населения (по И.В. Шахгильдяну и соавт., 2006
Рис. 2. Заболеваемость острым и хроническим гепатитом В и носительство НВV в Москве в 2002-2005 гг. на 100 000 населения (по И.В. Шахгильдяну и соавт., 2006)
В последние годы ВГ В переживает "второе рождение", вновь привлекая к себе пристальное внимание врачей и исследователей. Это связано как с появлением новых данных, позволяющих прогнозировать течение инфекции, так и с открытием новых противовирусных препаратов.
Весьма важное значение придается исследованию C.J. Chen и соавт. [5], в котором было показано, что уровень вирусной нагрузки представляет собой независимый фактор риска развития ГЦК и ЦП. Следует учитывать, что исследование выполнено на Тайване и не может быть механически перенесено на европейскую популяцию. Тем не менее представление о ГЦК как ориентальном раке постепенно изменяется, так как число пациентов с этой формой опухоли постоянно увеличивается, в том числе среди европейцев.
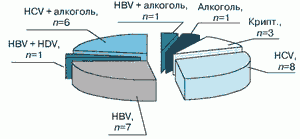
В нашей клинике с 2002 г. по август 2006 г. под наблюдением находился 991 пациент с ЦП различной этиологии. Среди них у 27 выявлена ГЦК, что составило 2,7%. На рис. 3 представлена этиологическая структура ЦП, осложнившегося развитием ГЦК. Подавляющее большинство (85%) составляют вирусные ЦП, которые приблизительно в равных пропорциях вызваны вирусами гепатитов В и С.
Рис. 3. Этиологическая структура ЦП, осложнившегося развитием ГЦК (n=27); вирусная этиология ЦП наблюдалась у 23 (85,2%!) из 27 пациентов с ГЦК
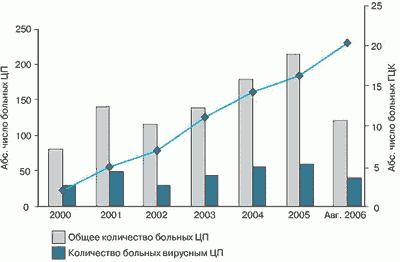
На рис. 4 показана динамика частоты развития ГЦК за 6-летний период. Можно видеть, что при относительно стабильном количестве вирусных ЦП число случаев ГЦК растет. При этом среди вирусных ЦП частота ГЦК составляет 9%, что определяет высокую степень актуальности этой формы опухоли для нашей страны с учетом широкой распространенности инфекции гепатотропными вирусами.
Рис. 4. Общее количество случаев ГЦК в год среди больных ЦП (n=991) с 2000 по август 2006 г.
На животной модели было показано, что энтекавир обладает уникальной способностью уменьшать уровень вирусной сверхскрученной ковалентно замкнутой ДНК (cccDNA). Изучение кинетики препарата показало, что он обладает двухфазным антивирусным эффектом. Ежедневный забор образцов крови на фоне назначения энтекавира в дозе 0,5 мг в день HBeAg-позитивным пациентам с хроническим гепатитом В (ХГ В), ранее не принимавшим аналоги нуклеозидов, показал, что в течение 10 дней быстро уменьшается уровень сывороточной HBV DNA. Далее она снижается уже медленно до 12-й недели лечения.
Результаты этой работы показали, что у энтекавира при его длительном использовании (3 года) очень высокий генетический барьер развития резистентности, особенно при лечении пациентов с ХГ В, ранее не получавших аналоги нуклеозидов.
Это дает основание использовать его как препарат выбора или средство первой линии в лечении этой категории пациентов. У ламивудинорезистентных пациентов энтекавир также показал свою высокую эффективность и может считаться препаратом выбора. Однако необходимо учитывать, что ламивудинорезистентные мутации являются фактором, способствующим развитию резистентности к энтекавиру.