Перивентрикулярная лейкомаляция
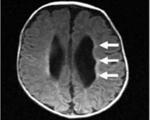
Перивентрикулярная лейкомаляция — это гипоксически-ишемическая энцефалопатия, характеризующаяся поражением белого вещества головного мозга новорожденных. Состояние чаще возникает у недоношенных, провоцируется патологиями течения беременности и родов, неадекватной респираторной поддержкой в постнатальном периоде. Заболевание проявляется мышечной дистонией, судорожным синдромом, задержкой психомоторного развития. Для диагностики болезни назначается КТ или МРТ мозга, ЭЭГ, допплерография церебральных сосудов. Лечение лейкомаляции включает медикаменты (нейропротекторы, инфузионные растворы, антиконвульсанты), индивидуальный комплекс физиотерапии, массажа, ЛФК.
МКБ-10
Общие сведения
По разным данным, перивентрикулярная лейкомаляция (ПВЛ) встречается у 4,8-9% младенцев, причем среди больных преобладают недоношенные новорожденные (78%). Наибольшая вероятность появления болезни у детей, родившихся на сроке 27-32 недели. По данным аутопсии умерших младенцев, признаки ПВЛ регистрируются чаще — у 50-75%. Заболевание имеет большую значимость в детской неврологии, поскольку может вызывать тяжелые отдаленные последствия, считается ведущей причиной ДЦП.
Причины
Основной этиологический фактор перивентрикулярной лейкомаляции — внутриутробная гипоксия, которая выступает следствием осложнений протекания беременности, материнских факторов риска либо негативного экзогенного воздействия. Также состояние может возникать при перинатальной гипоксии, которая развивается во время родов, в первые дни жизни младенца (при синдроме дыхательных расстройств, врожденных аномалиях сердца и легких, неонатальном сепсисе).
В группе риска наибольшую по численности категорию составляют недоношенные младенцы. Зачастую лейкомаляция выявляется у детей, которое были рождены от матерей с сахарным диабетом, хронической анемией, гипертиреозом либо страдавших от преэклампсии и эклампсии. Состояние возникает при выполнении экстренного кесарева сечения, неадекватном родовспоможении (травмирующие акушерские пособия). Высокая частота лейкомаляции (до 22%) отмечается при сочетании длительного безводного периода с хориоамнионитом у матери.
Патогенез
Поражение головного мозга связано со снижением кровотока в церебральных сосудах, недостаточным поступлением кислорода и питательных ингредиентов. Перивентрикулярная область наиболее чувствительна к этим изменениям, что обусловлено особенностями кровоснабжения, несовершенством процессов ауторегуляции, нейроонтогенетическими особенностями головного мозга у младенцев.
Недоношенные намного чаще страдают лейкомаляцией, поскольку у них на фоне гипоксии не увеличивается церебральный кровоток, как это бывает у рожденных в срок младенцев. В результате этого резко уменьшается кровоток в зоне между вентрикулофугальными и вентрикулопетальными артериями, быстро формируется гиперкапния и ацидоз. Расстройства микроциркуляции проявляются стазом, тромбозом, вне- и внутриклеточным отеком белого вещества.
При перивентрикулярной лейкомаляции в конечном итоге происходит некроз отельных участков мозгового вещества, образование кист, избыточное накопление медиаторов воспаления. Поскольку на 28-32 неделях в норме происходит активная миелинизация белого вещества, а в условиях гипоксии этот процесс не может происходить, недоношенные новорожденные впоследствии имеют серьезные органические поражения ЦНС.
Формирование ПВЛ возможно не только при недостатке кислорода, но и при гипероксии — при проведении ИВЛ, оказании других видов респираторной поддержки. При избыточном поступлении кислорода повышается рН крови в мозговой ткани, что вызывает рефлекторный спазм сосудов, затруднение венозного оттока. Также кислород активизирует процессы свободнорадикального церебрального повреждения.
Симптомы
Как правило, перивентрикулярная лейкомаляция формируется антенатально или на протяжении первых часов после рождения ребенка, поэтому начальные признаки заметны уже в родильном доме, особенно если младенец рожден недоношенным. При обширном повреждении белого вещества происходят нарушения сознания по типу летаргии или комы, однако возможна обратная симптоматика — повышенная возбудимость, оживление безусловных рефлексов, судорожный синдром.
Типичным проявлением патологии являются изменения тонуса мышц. На первом месяце жизни преобладает слабость мускулатуры ног в сочетании с нормальным формированием мышц верхних конечностей. У недоношенных новорожденных часто отмечается тотальная мышечная гипотония. Такие нарушения сохраняются в среднем до 6 месяцев, после чего они сменяются спастическими явлениями — повышением тонуса мускулатуры нижних конечностей, оживлением коленных рефлексов.
Течение перивентрикулярной лейкомаляции имеет неравномерный характер: периоды обострения симптоматики сменяются «мнимым благополучием», когда ребенок развивается относительно нормально. Затем происходит задержка формирования моторных навыков, развиваются различные сенсорные нарушения, дизартрия. 66% детей, особенно недоношенные, страдают от снижения остроты зрения вплоть до полной слепоты вследствие атрофии зрительных нервов.
Осложнения
Перивентрикулярные поражения белого вещества — крайне тяжелое состояние. Недоношенные дети с ПВЛ умирают в 50% случаев еще в период новорожденности, у выживших обычно наступает инвалидность с полной дезадаптацией. Пациенты с длительно сохраняющимся судорожными приступами в 85% случаев имеют грубую задержку психомоторного развития. У перенесших ПВЛ в будущем в 1,5 раза чаще встречаются фебрильные судороги, в 27 раз чаще формируется эпилепсия.
При множественных кистах в перивентрикулярной зоне у 80-97% больных (чаще — недоношенных) возникает детский церебральный паралич (ДЦП), который сопровождается глубоким психоречевым отставанием. Развитие заболевания связано с повреждением центральной части внутренней капсулы, средне- и заднелобных сегментов белого вещества полушарий. Также лейкомаляция вызывает микроцефалию (у 42% пациентов), нейросенсорную тугоухость (у 28% больных).
Диагностика
Постановка правильного диагноза в неонатальном периоде затруднена, что объясняется полиморфностью клинической картины, отсутствием патогномоничных симптомов. При физикальном осмотре выявляется асимметрия мышечного тонуса, патологическое усиление рефлексов, на более поздних этапах — спастическая диплегия. Особую настороженность следует проявлять в отношении детей, родившихся недоношенными. В план обследования новорожденных с подозрением на ПВЛ включаются:
Лечение перивентрикулярной лейкомаляции
Терапия перивентрикулярной лейкомаляции представляет собой сложную задачу, учитывая необратимый характер повреждений белого вещества, частое сочетание гипоксически-ишемической энцефалопатии с поражениями других систем организма у недоношенных. Медикаментозное лечение подбирается на основе ведущих синдромов болезни и включает следующие группы препаратов:
Учитывая высокую частоту резидуальных неврологических явлений, рекомендовано восстановительное лечение. Чтобы улучшить двигательные способности, назначаются курсы массажа, физиотерапии, лечебной физкультуры. Для развития речевых навыков требуются коррекционные занятия у логопеда, дефектолога. Детям с поражением органов чувств нужна помощь тифлопедагога, сурдопедагога. Пациентам с ДЦП необходимы специальные ходунки, костыли, инвалидные коляски.
Прогноз и профилактика
В большинстве случаев лейкомаляция отличается неблагоприятным течением, отличается высоким уровнем смертности во время младенчества. Для выживших детей прогноз напрямую зависит от тяжести органического дефекта перивентрикулярной зоны, своевременности и полноты проведенного лечения. Профилактика ПВЛ включает рациональное ведение беременности, предупреждение родового травматизма, соблюдение протоколов при респираторной поддержке в роддоме, усиленный контроль за развитием недоношенных.
Гидроцефалия у детей: только факты
В лекции рассматриваются определение, варианты классификаций, этиология, патогенез, клиническая синдромология гидроцефалии (врожденной и приобретенной) у детей, а также современные подходы к диагностике, методы лечения (фармакологического и нейрохирургиче
Definition, classification variants, etiology, pathogenesis and clinical syndromology of hydrocephalus (congenital and acquired) in pediatric patients are considered, as well as contemporary approaches to diagnostics, methods of management (pharmacological and neurosurgical) and prevention for this type of central nervous system pathology.
Гидроцефалия — болезнь, возникающая вследствие избыточной выработки и чрезмерного накопления ликвора в подоболочечных пространствах и/или желудочках головного мозга (в субарахноидальном или субдуральном пространстве), приводящих к истончению (атрофии) мозгового вещества и расхождению костей черепа [1–4].
В МКБ-10 предусмотрены следующие коды для различных видов гидроцефалии: G91 (G91.0 — сообщающаяся гидроцефалия, G91.1 — обструктивная гидроцефалия, G91.2 — гидроцефалия нормального давления, G91.3 — посттравматическая гидроцефалия неуточненная, G91.8 — другие виды гидроцефалии, G91.9 — гидроцефалия неуточненная).
Классификация гидроцефалии
Существуют несколько вариантов классификации гидроцефалии. Прежде всего, различают врожденную и приобретенную гидроцефалию.
Врожденная гидроцефалия имеется к моменту рождения ребенка и является результатом воспалительных заболеваний центральной нервной системы (ЦНС), пороков развития мозга, а также внутричерепной (родовой) травмы, кровоизлияний в головной мозг.
Приобретенная гидроцефалия развивается после рождения вследствие этиологически и патогенетически разнообразной патологии (нейроинфекции, опухолевые процессы, сосудистые заболевания, черепно-мозговые травмы и т. д.).
Болезнь бывает активной и пассивной. В первом случае имеется повышение внутричерепного давления при наличии дилатации желудочков и субарахноидальных пространств. При пассивной гидроцефалии предполагается, что описываемые изменения отмечаются в отсутствие внутричерепной гипертензии.
Выделяют открытую и закрытую формы гидроцефалии. Открытая (сообщающаяся) гидроцефалия диагностируется при отсутствии нарушений связи желудочковой системы мозга с субарахноидальным пространством, а закрытая (окклюзионная или несообщающаяся) — когда это сообщение нарушено.
Наружная и внутренняя формы гидроцефалии определяются локализацией аккумуляции спинномозговой жидкости (СМЖ); наружная гидроцефалия — скопление СМЖ в подоболочечных пространствах головного мозга, внутренняя гидроцефалия — скопление СМЖ в желудочках головного мозга.
Патогенетическая классификация гидроцефалии: 1) гиперсекреторные формы (избыточное образование СМЖ); 2) арезорбтивные формы (нарушение процессов всасывания СМЖ); 3) окклюзионные формы (наличие препятствия на пути движения СМЖ от источника ее образования к областям ее резорбции).
В зависимости от имеющегося уровня окклюзии ликворных путей рассматривают пять вариантов гидроцефалии: 1) окклюзия одного или обоих отверстий Монро; 2) блокада полости III желудочка; 3) стеноз или окклюзия сильвиева водопровода; 4) окклюзия или нераскрытие отверстий IV желудочка; 5) нарушения проходимости субарахноидальных пространств.
В зависимости от достигнутого уровня контроля над внутричерепной гипертензией принято различать компенсированную, субкомпенсированную или декомпенсированную гидроцефалию.
Отдельный вариант болезни — гидроцефалия нормального давления («симптоматическая»). При ней изначально отмечается повышение внутричерепного давления (следствие избыточного скопления СМЖ в желудочках мозга) — с вентрикуломегалией или без таковой, которое постепенно снижается, но остается умеренно повышенным (150–200 мм водн. ст.). Существуют две разновидности гидроцефалии нормального давления — идиопатическая (причина неизвестна) и вторичная (следствие субарахноидального кровоизлияния, травмы, опухоли и/или инфекции ЦНС, осложнение нейрохирургического вмешательства и т. д.) [1–4].
S. Oi (2010) предложил «мультикатегориальную классификацию гидроцефалии», отражающую современные представления об этой болезни (табл.) [5, 6].
Этиология и патогенез гидроцефалии
Важнейший этиологический фактор гидроцефалии — интра- и перинатальная патология ЦНС. В качестве этиологических причин врожденной гидроцефалии рассматриваются патология беременности, кислородное голодание церебральной ткани; интранатальные факторы, приводящие к гипоксически-ишемическим и/или травматическим повреждениям головного мозга; гестационная незрелость мозговых структур, наиболее подверженных описываемым повреждениям.
К развитию гидроцефалии приводят воспалительные заболевания мозга и его оболочек, а также внутриутробные и нейроинфекции, врожденные пороки развития ЦНС, патология сосудов, опухоли головного и спинного мозга, травматические повреждения (включая внутричерепные родовые травмы), генетические факторы и др.
Описаны случаи гидроцефалии, ассоциированные с дисгенезиями головного мозга, бруцеллезом, паротитной и другими инфекциями, диффузной гиперплазией ворсинок хориоидального сплетения, сосудистыми аномалиями, внутричерепными кровоизлияниями и т. д.
Гидроцефалия посттравматическая (прогрессирующее избыточное накопление СМЖ в ликворных пространствах и веществе головного мозга вследствие черепно-мозговой травмы) обусловлена нарушениями циркуляции и резорбции СМЖ [1–4, 7].
По данным C. Schrander-Stumple и J. P. Fryns (1998) наследственная Х-сцепленная (врожденная) гидроцефалия встречается в 4% всех зарегистрированных случаев болезни (по другим данным в 5–15% наблюдений), до 40% случаев гидроцефалии этиогенетически обусловлены [8]. Гидроцефалия встречается при синдроме Дэнди–Уокера, синдроме Арнольда–Киари и др. Описано не менее 43 мутаций/локусов, связанных с гередитарными формами гидроцефалии (у человека и лабораторных животных); в экспериментальных условиях обнаружены 9 генов, ассоциированных с этой церебральной патологией, а у людей всего один [1–4].
Прогрессирование гидроцефалии сопровождается структурно-морфологическими изменениями головного мозга различной выраженности: 1) истончение коры и белого вещества (вплоть до полной его ликвидации); 2) атрофия сосудистых сплетений; 3) атрофия/субатрофия базальных ганглиев, ствола, мозжечка; 4) выраженные расстройства капиллярного кровотока; 5) утолщение и/или сращение мозговых оболочек; 6) избыточный рост (гипертрофия) глиозной ткани. В тяжелых случаях возможно формирование гидроанэнцефалии, когда имеются только эпендима и тонкий слой мягкой мозговой оболочки.
Наиболее интенсивно функционирующая и высоковаскуляризованная перивентрикулярная область максимально страдает от гипоксии. Следствием атрофии перивентрикулярного белого вещества мозга является пассивное расширение желудочковой системы с формированием вентрикуломегалии.
При посттравматической гидроцефалии патологические процессы в головном мозге морфологически характеризуются расширением желудочковой системы, перивентрикулярным отеком и облитерацией субарахноидальных щелей. Облитерация путей ликворотока определяется следующими патогенетическими факторами: субарахноидальное кровоизлияние, внутричерепные гематомы, очаговые и/или диффузные повреждения мозга, рубцово-спаечные и атрофические процессы (в том числе после обширных краниотомии и резекционных трепанаций), менингоэнцефалиты и вентрикулиты. Сроки развития посттравматической гидроцефалии (нормотензивной, гипертензивной или окклюзионной) обычно варьируют от 1 месяца до 1 года [1–4, 7].
Клиническая синдромология гидроцефалии
Основная симптоматика при гидроцефалии (врожденной и приобретенной) определяется двумя группами факторов: 1) причинами возникновения болезни; 2) непосредственно гидроцефальным синдромом.
К первой группе преимущественно относятся очаговые проявления (чаще в виде спастических парезов восходящего типа в нижних и/или верхних конечностях). Выраженность симптомов группы 2 зависит от формы, стадии и степени прогрессирования гидроцефалии. При врожденной форме болезни признаки гидроцефалии могут присутствовать как при рождении ребенка, так и проявляться позже — к возрасту 3–6 мес.
Чаще первым признаком болезни служит непропорционально быстрый прирост окружности головы. Для ее оценки у детей пользуются специальными таблицами (центильными).
У детей первого года жизни может возникать преобладание «мозговых» отделов черепа над «лицевым» (как следствие — вынужденное положение с запрокидыванием головы назад), усиление венозного рисунка и полнокровие подкожных вен головы, напряжение большого и других родничков, расхождение костей черепа, симптом Грефе. Эти симптомы сопровождаются отставанием в психомоторном развитии (различной выраженности), реже — в физическом. Атрофия сосков зрительных нервов — тяжелое осложнение не леченной или не поддающейся терапии прогрессирующей гидроцефалии.
Цефалгический синдром в большей степени свойственен приобретенной гидроцефалии у детей старше 1 года (когда роднички и черепные швы уже закрыты).
Клинические проявления посттравматической гидроцефалии характеризуются неврологическими и психическими нарушениями, вызванными первичной травмой головного мозга. Частично они являются отражением не столько самой гидроцефалии, сколько следствием перенесенной черепно-мозговой травмы (ЧМТ) или преморбидной патологии.
А. П. Коновалов и соавт. (1999) выделяют три варианта посттравматической гидроцефалии: 1) на фоне разрешившейся или негрубой остаточной симптоматики тяжелой ЧМТ, с доминированием в клинике какого-либо определенного симптомокомплекса; 2) на фоне медленно разрешающейся грубой симптоматики тяжелой ЧМТ с присоединением к ней интеллектуально-мнестических и атактических синдромов; 3) на фоне вегетативного состояния (что препятствует выходу из него). Для гипертензивной и окклюзионной посттравматической гидроцефалии (исключая нормотензивную) характерны головная боль, рвота, головокружение. У всех пациентов выявляется психопатологическая симптоматика (интеллектуально-мнестические расстройства, эйфория или заторможенность, аспонтанность, акинетический мутизм и др.); а также нарушения походки и атаксия (с характерным «прилипанием стоп к полу»), нарушения функций тазовых органов.
При гидроцефалии нормального давления обычно не отмечается классических симптомов, свойственных врожденной или приобретенной гидроцефалии, но, поскольку вентрикуломегалия оказывает негативный эффект на смежные участки корковой ткани, болезнь имеет свои особенности (классическая триада: нарушения походки, недержание мочи, снижение интеллекта различной степени выраженности) [1–4].
Диагностика и методы обследования
Установление диагноза гидроцефалии (помимо физикальных данных) основывается на данных нейровизуализации (нейросонография — при открытом большом родничке, компьютерная и магнитно-резонансная томография головного мозга — КТ и МРТ), которые рассматриваются в совокупности с описанными выше симптомами болезни. Указанные методы нейровизуализации вытеснили используемую ранее рентгенографию черепа. К ней прибегают лишь в редких случаях; обзорная рентгенография черепа позволяет косвенно судить о вторичных изменениях костей черепа (при отсутствии КТ и МРТ).
Особенно важно наблюдение за адекватным функционированием шунтов, установленных в ходе нейрохирургического вмешательства. При малейшем подозрении на несостоятельность шунтов пациент должен быть направлен к нейрохирургу.
Изотопная цистернография с введением радиоактивного изотопа (в ходе люмбальной пункции) и последующим наблюдением за выведением СМЖ из мозга позволяет установить диагноз нормотензивной гидроцефалии.
От диафаноскопии (трансиллюминация черепа) в настоящее время практически отказались. Люмбальная пункция — традиционный метод исследования, позволяющий оценить давление и провести анализ СМЖ. Усиление эхо-пульсации до 70–80% при проведении ультразвукового исследования мозга не является диагностическим признаком гидроцефалии.
Исследование слуховых вызванных потенциалов нередко обнаруживает их нарушения, что указывает на особую чувствительность ствола головного мозга к внутричерепной гипертензии.
Офтальмологический осмотр глазного дна позволяет выявить изменения, характерные для гидроцефалии (застойные явления на глазном дне, атрофические процессы, признаки воспаления, а также кровоизлияния, изменения тонуса и калибра сосудов и пр.), что дает возможность оценить течение патологического процесса.
При подозрении на наличие врожденной инфекции (внутриутробного инфицирования) оправдано проведение серологических и вирусологических исследований.
За рубежом используется метод неинвазивного мониторирования внутричерепного давления через большой родничок у детей первого года жизни, основанный на принципе аппланации. Измерение производится при помощи специального прибора (фонтанометр), а само исследование получило название «фонтограммы» или «фонтанометрии» [1–4, 7].
Дифференциальная диагностика
Гидроцефалию дифференцируют от следующих основных патологических состояний: субдуральные внутричерепные кровоизлияния, мегалэнцефалия (первичная), гидроанэнцефалия, менингит, опухоли головного мозга, семейная (конституциональная) макроцефалия, витамин D-дефицитный рахит, рахит недоношенных детей и др.
Реже встречаются другие виды патологии, от которых необходимо дифференцировать гидроцефалию: ахондроплазия, синдром Сото (церебральный гигантизм), многочисленные так называемые «нейрокожные» синдромы, группа лейкодистрофий (болезнь Александера, Канавана, глобоидная и метохроматическая формы лейкодистрофий), ганглиозидозы, мукополисахаридоз (болезни Тея–Сакса и Сандхоффа), болезнь мочи с запахом кленового сиропа и др. [1–4, 7].
Лечение
Лечебные мероприятия при прогрессирующей гидроцефалии подразделяются на оперативные и терапевтические (медикаментозные и немедикаментозные).
При наличии признаков текущего воспалительного процесса в ЦНС детям показана соответствующая терапия (антибактериальными средствами, специфическими препаратами, а также глюкокортикостероидами и человеческими внутривенными иммуноглобулинами — по показаниям).
Прогрессирующие формы гидроцефалии (окклюзионные), как более серьезный вариант патологии, требуют своевременного нейрохирургического вмешательства (проведение шунтирующей операции). Целью оперативного вмешательства является создание адекватного оттока СМЖ при помощи специальных шунтов (дренирующих систем из синтетических материалов). Различают шунты, отводящие СМЖ из желудочков мозга в различные локусы организма (вентрикулоперитонеальные, люмбоперитонеальные, вентрикулоатриальные). Так, одни шунты транспортируют избыточное скопление ликвора в перитонеальную полость, другие — в правый желудочек сердца. Вентрикулоперитонеальное шунтирование — основной метод нейрохирургического лечения гидроцефалии в РФ и за рубежом.
Существует метод хирургического лечения, получивший название «эндоскопической третьей вентрикулостомии» (перфорация нижней части III желудочка головного мозга для устранения блокирования потока СМЖ и увеличения ее оттока); другое название метода «эндоскопическая вентрикулоцистерностомия дна III желудочка». Целью описываемой операции является создание путей оттока СМЖ из III желудочка в цистерны головного мозга, через пути которых происходит резорбция ликвора.
Другими разновидностями эндоскопического лечения гидроцефалии в различных клинических ситуациях являются акведуктопластика, вентрикулокистоцистерностомия, септостомия, эндоскопическое удаление внутрижелудочковой опухоли, а также эндоскопическая установка шунтирующей системы.
Из нейрохирургических манипуляций у детей грудного возраста может применяться вентрикулярная пункция (выведение СМЖ из желудочков головного мозга через большой родничок). Эта наружная дренирующая манипуляция используется крайне редко, так как может сопровождаться большим числом осложнений (инфицирование и т. д.).
Имеются отдельные сообщения о применении интрадуральной спинальной эндоскопии при лечении гидроцефалии и ассоциированных с ней состояний у детей.
При остром возникновении внутричерепной гипертензии используют препараты, обладающие мочегонным действием. К ним относятся: фуросемид (внутримышечно) — иногда в сочетании с раствором сульфата магния, глицерол (per os), маннитол (внутривенно капельно).
При необходимости в длительном лечении гидроцефалии в первую очередь назначается ацетазоламид (Диакарб) — диуретик из группы ингибиторов карбоангидразы (фермент, катализирующий обратимую реакцию гидратации диоксида углерода и последующую диссоциацию угольной кислоты). Действие ацетазоламида связано с супрессией карбоангидразы в сплетениях желудочков головного мозга и со снижением продукции СМЖ (гиполикворное действие). Побочные эффекты ацетазоламида (ацидоз и одышка) систематически корригируют назначением бикарбоната натрия (0,5 г 3 раза в день).
Пациентам с гидроцефалией в возрасте до 3 лет необходимо назначение препаратов витамина D и кальция. Помимо кальция, из минеральных веществ на фоне терапии ацетазоламидом абсолютно необходима дотация препаратов калия и магния (Аспаркам, Панангин).
Симптоматическое лечение при гидроцефалии определяется индивидуальными показаниями и обычно включает: массаж, лечебную физкультуру, различные виды физиотерапии, метод биологической обратной связи, а также стимулирующую терапию (ноотропные, метаболические, сосудистые препараты и пр.) и т. д. Противосудорожные средства детям с гидроцефалией назначают при наличии соответствующих показаний (симптоматическая эпилепсия и пр.).
Нейродиетологические мероприятия должны быть направлены на поддержание состояния питания, адекватное потребление жидкости, дотацию витаминов и минеральных веществ, при необходимости — питательная поддержка (клиническое питание: энтеральное и/или парентеральное) [2–4].
Профилактика
Поскольку в значительном числе случаев гидроцефалия может быть установлена еще в периоде внутриутробного развития, рекомендуется сонографическое исследование плодов (начиная с 17-й недели гестации). В ряде случаев показано МРТ-исследование, хотя P. Peruzzi и соавт. (2010) указывают, что оно не имеет выраженных диагностических преимуществ по сравнению с ультразвуковыми методами [9].
В целях профилактики гидроцефалии у детей необходимо своевременное выявление и лечение внутриутробных инфекций у их матерей. Необходимо осуществление в полной мере профилактики детского травматизма и нейроинфекций. Для предотвращения миеломенингоцеле показан превентивный прием препаратов фолиевой кислоты [1–4, 7].
Прогноз
Гидроцефалия — церебральная патология, сопряженная со значительным неврологическим дефицитом, потенциальной инвалидизацией и снижением качества жизни. Существует риск формирования необратимых изменений в нервной системе и снижения интеллекта (вплоть до умственной отсталости).
При врожденной и приобретенной гидроцефалии прогноз определяется ранним началом и адекватностью лечения (фармакологического или нейрохирургического).
Серьезным осложнением гидроцефалии может явиться эпилепсия, индуцированная как самой гидроцефалией (структурно-морфологическими изменениями структур мозга), так и установкой дренирующего шунта [1–4, 7].
По данным M. Mataro и соавт. (2001), средние значения IQ у пациентов с гидроцефалией снижены по ряду вербальных и невербальных функций. Среди получавших адекватную терапию пациентов в 40–65% случаев отмечаются нормальные показатели интеллектуальных функций [10].
Литература
В. М. Студеникин, доктор медицинских наук, профессор, академик РАЕ
ООО НПСМЦ «Дрим Клиник», Москва
Гидроцефалия у детей: только факты/ В. М. Студеникин
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 66-69
Теги: цефалгия, головной мозг, ликвор, внутричерепная гипертензия
.gif)